6 AÑOS de mediana desde el inicio de los síntomas hasta el diagnóstico7
- Recurso
- Fuente: Campus Sanofi
- 22 sept 2025
Hablemos de ESO: La EEo y la Inflamación de Tipo 2
%20(1).png)
Transcripción
Soy “EOmilio Fagitis” y voy a hablarte sobre Esofagitis Eosinofílica, una enfermedad crónica y progresiva del esófago impulsada por la inflamación de tipo 2.3-5
Esta enfermedad requiere de un seguimiento a largo plazo para asegurar la adherencia al tratamiento, limitar las complicaciones futuras y reducir la necesidad de dilataciones.1-3
Esofagitis eosinofílica: una enfermedad crónica y progresiva1-3
Transcripción
Los pacientes con Esofagitis Eosinofílica experimentan síntomas discapacitantes, como la disfagia, que impactan negativamente en su calidad de vida2,4-6
Los pacientes con EEo experimentan:2,4-6
Transcripción
Es importante recordar que la Esofagitis Eosinofílica no suele presentarse de manera aislada.1,10
Aproximadamente el 75% de los pacientes con EEo tiene al menos una enfermedad inflamatoria de tipo 2 coexistente.10
Esta asociación refuerza la hipótesis de una inflamación sistémica común que debe tenerse en cuenta en el abordaje integral del paciente.
EoE: Retraso en el tratamiento
~75% de los pacientes con EEo tiene al menos una enfermedad inflamatoria de tipo 2 coexistente:10
- Rinitis alérgica
- Asma
- Dermatitis atópica
- Alergias alimentarias
Transcripción
Un aspecto preocupante es el retraso en el tratamiento.7
Se tardan 6 años de mediana desde el inicio de los síntomas hasta el diagnóstico.7
Además, el 46,5% de los pacientes con retraso en el diagnóstico de 2 años o menos experimenta cambios impulsados por la inflamación y/o aumento de fibrosis.7
Inflamación T2 subyacente
El 46,5% de los pacientes con retraso en el diagnóstico < 2 años experimenta cambios impulsados por la inflamación y/o aumento de fibrosis7
Transcripción
Actualmente, las opciones de tratamiento son insuficientes.8,9
El 50% de los pacientes con IBP no logra una remisión clínico-histológica10, y el 61% de los pacientes con corticoides tópicos muestra una recaída histológica a pesar del tratamiento continuo.9
Retraso en el tratamiento
 El 50% de los pacientes con IBP no logra una remisión clinico-histológica8
El 50% de los pacientes con IBP no logra una remisión clinico-histológica8
 El 61% de los pacientes con corticoides tópicos muestra una recaída histológica a pesar del tratamiento continuo9
El 61% de los pacientes con corticoides tópicos muestra una recaída histológica a pesar del tratamiento continuo9
Transcripción
Soy “EOmilio Fagitis” y voy a hablarte sobre Esofagitis Eosinofílica, una enfermedad crónica y progresiva del esófago impulsada por la inflamación de tipo 2.3-5
Esta enfermedad requiere de un seguimiento a largo plazo para asegurar la adherencia al tratamiento, limitar las complicaciones futuras y reducir la necesidad de dilataciones.1-3
Esofagitis eosinofílica: una enfermedad crónica y progresiva1-3
Transcripción
Los pacientes con Esofagitis Eosinofílica experimentan síntomas discapacitantes, como la disfagia, que impactan negativamente en su calidad de vida2,4-6
Los pacientes con EEo experimentan:2,4-6
Transcripción
Es importante recordar que la Esofagitis Eosinofílica no suele presentarse de manera aislada.1,10
Aproximadamente el 75% de los pacientes con EEo tiene al menos una enfermedad inflamatoria de tipo 2 coexistente.10
Esta asociación refuerza la hipótesis de una inflamación sistémica común que debe tenerse en cuenta en el abordaje integral del paciente.
EoE: Retraso en el tratamiento
~75% de los pacientes con EEo tiene al menos una enfermedad inflamatoria de tipo 2 coexistente:10
- Rinitis alérgica
- Asma
- Dermatitis atópica
- Alergias alimentarias
Transcripción
Un aspecto preocupante es el retraso en el tratamiento.7
Se tardan 6 años de mediana desde el inicio de los síntomas hasta el diagnóstico.7
Además, el 46,5% de los pacientes con retraso en el diagnóstico de 2 años o menos experimenta cambios impulsados por la inflamación y/o aumento de fibrosis.7
Inflamación T2 subyacente
6 AÑOS de mediana desde el inicio de los síntomas hasta el diagnóstico7
El 46,5% de los pacientes con retraso en el diagnóstico < 2 años experimenta cambios impulsados por la inflamación y/o aumento de fibrosis7
Transcripción
Actualmente, las opciones de tratamiento son insuficientes.8,9
El 50% de los pacientes con IBP no logra una remisión clínico-histológica10, y el 61% de los pacientes con corticoides tópicos muestra una recaída histológica a pesar del tratamiento continuo.9
Retraso en el tratamiento
 El 50% de los pacientes con IBP no logra una remisión clinico-histológica8
El 50% de los pacientes con IBP no logra una remisión clinico-histológica8
 El 61% de los pacientes con corticoides tópicos muestra una recaída histológica a pesar del tratamiento continuo9
El 61% de los pacientes con corticoides tópicos muestra una recaída histológica a pesar del tratamiento continuo9
Transcripción
Un aspecto menos visible pero igualmente relevante es el uso de conductas adaptativas por parte de los pacientes.
Estas son estrategias que desarrollan para facilitar la ingesta de alimentos y enmascarar los síntomas, lo que puede retrasar el diagnóstico y favorecer la progresión de la enfermedad.11
Es fundamental preguntar activamente a los pacientes sobre estos mecanismos para identificar posibles síntomas ocultos y realizar una evaluación más precisa.11
Conductas adaptativas
- Mojar los alimentos con líquidos o tomar demasiados líquidos11
- Procesar la comida (cortarla en trozos pequeños, hacerla puré)11
- Prolongar el tiempo de las comidas11
- Evitar comida texturizada como la carne y el pan11
- Masticar excesivamente11
- Evitar el uso de comprimidos/píldoras11
Transcripción
Un aspecto menos visible pero igualmente relevante es el uso de conductas adaptativas por parte de los pacientes.
Estas son estrategias que desarrollan para facilitar la ingesta de alimentos y enmascarar los síntomas, lo que puede retrasar el diagnóstico y favorecer la progresión de la enfermedad.11
Es fundamental preguntar activamente a los pacientes sobre estos mecanismos para identificar posibles síntomas ocultos y realizar una evaluación más precisa.11
Conductas adaptativas
- Mojar los alimentos con líquidos o tomar demasiados líquidos11
- Procesar la comida (cortarla en trozos pequeños, hacerla puré)11
- Prolongar el tiempo de las comidas11
- Evitar comida texturizada como la carne y el pan11
- Masticar excesivamente11
- Evitar el uso de comprimidos/píldoras11
Transcripción
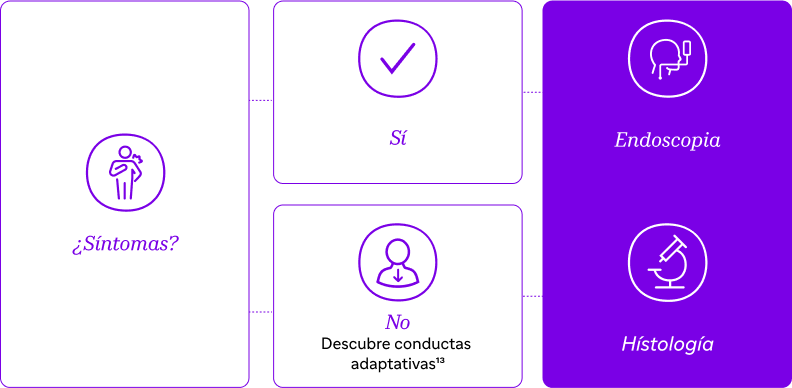
Para un adecuado manejo de la EEo, es fundamental ir más allá de los síntomas visibles e identificar conductas adaptativas. Un abordaje holístico permitirá un diagnóstico más preciso y un tratamiento más efectivo.11,12
- Sí tu paciente tiene síntomas la endoscopia con biopsia e histologia son necesarias para evaluar la inflamación y los marcadores de la enfermedad12
- Si tu paciente No presenta síntomas → Explora sus conductas adaptativas y realiza la endoscopia e histología para obtener un diagnóstico certero11,12
Transcripción
La inflamación de tipo 2 es la causa subyacente en la mayoría de los pacientes con EEo 1,10. Las citocinas IL-4 e IL-13 desempeñan papeles compartidos y específicos en las vías de señalización de la EEo.13,14,15
A nivel local, estas citocinas provocan alteraciones en la barrera epitelial, inflamación y cambios estructurales en el tejido.13,14,15
A nivel sistémico, favorecen la aparición de enfermedades coexistentes, la producción de IgE y la activación de células inmunitarias.13,14,15 Por su parte, IL-5 desempeña un papel esencial en la inflamación eosinofílica.13,15
El papel de la IL-4 y IL-13
Inflamación sistémica
- Enfermedades coexistentes relacionadas con la inflamación de tipo 210
- Cambio de clase de células B y producción de IgE13
- Activación de mastocitos13
Inflamación local
- Disfunción de la barrera epitelial13,14,15
- Elevación de EOS13,14,15
- Remodelado tisular13,14
- Fibrosis (anillos, estenosis)13,14,15
- Contracción del músculo liso13,14
Transcripción
Para un adecuado manejo de la EEo, es fundamental ir más allá de los síntomas visibles e identificar conductas adaptativas. Un abordaje holístico permitirá un diagnóstico más preciso y un tratamiento más efectivo.11,12
- Sí tu paciente tiene síntomas la endoscopia con biopsia e histologia son necesarias para evaluar la inflamación y los marcadores de la enfermedad12
- Si tu paciente No presenta síntomas → Explora sus conductas adaptativas y realiza la endoscopia e histología para obtener un diagnóstico certero11,12

Transcripción
La inflamación de tipo 2 es la causa subyacente en la mayoría de los pacientes con EEo 1,10. Las citocinas IL-4 e IL-13 desempeñan papeles compartidos y específicos en las vías de señalización de la EEo.13,14,15
A nivel local, estas citocinas provocan alteraciones en la barrera epitelial, inflamación y cambios estructurales en el tejido.13,14,15
A nivel sistémico, favorecen la aparición de enfermedades coexistentes, la producción de IgE y la activación de células inmunitarias.13,14,15 Por su parte, IL-5 desempeña un papel esencial en la inflamación eosinofílica.13,15
El papel de la IL-4 y IL-13

Inflamación sistémica
- Enfermedades coexistentes relacionadas con la inflamación de tipo 210
- Cambio de clase de células B y producción de IgE13
- Activación de mastocitos13
Inflamación local
- Disfunción de la barrera epitelial13,14,15
- Elevación de EOS13,14,15
- Remodelado tisular13,14
- Fibrosis (anillos, estenosis)13,14,15
- Contracción del músculo liso13,14
EEo: esofagitis eosinofílica; IBP: inhibidores de la bomba de protones; EOS: eosinófilos; Ig: inmunoglobulina; IL: interleucina
Referencias:
- Gandhi NA, et al. Targeting key proximal drivers of type 2 inflammation in disease. Nat Rev Drug Discov. 2016;15(1):35-50.
- Mukkada V, et al. Health-related quality of life and costs associated with eosinophilic esophagitis: a systematic review. Clin Gastroenterol Hepatol. 2018;16(4):495-503.e8.
- Chehade M, et al. Phenotypic characterization of eosinophilic esophagitis in a large multicenter patient population from the Consortium for Food Allergy Research. J Allergy Clin Immunol Pract. 2018;6(5):1534-1544.e5.
- D’Alessandro A, et al. Eosinophilic esophagitis: from pathophysiology to treatment. World J Gastrointest Pathophysiol. 2015;6(4):150-158.
- Li-Kim-Moy JP, et al. Esophageal subepithelial fibrosis and hyalinization are features of eosinophilic esophagitis. J Pediatr Gastroenterol Nutr. 2011;52(2):147-
- Straumann A, et al. Eosinophilic esophagitis: analysis of food impaction and perforation in 251 adolescent and adult patients. Clin Gastroenterol Hepatol. 2008;6(5):598-600.
- Schoepfer AM, et al. Delay in diagnosis of eosinophilic esophagitis increases risk for stricture formation in a time-dependent manner. Gastroenterology. 2013;145(6):1230-1236.
- Lucendo AJ, et al. Efficacy of proton pump inhibitor drugs for inducing clinical and histologic remission in patients with symptomatic esophageal eosinophilia: a systematic review and meta-analysis. Clin Gastroenterol Hepatol. 2016;14(1):13-22.
- Eluri S, et al. Diminishing effectiveness of long-term maintenance topical steroid therapy in PPI non-responsive eosinophilic esophagitis. Clin Transl Gastroenterol. 2017;8(6):e97.
- Van Rhijn BD, Bredenoord AJ. Management of eosinophilic esophagitis based on pathophysiological evidence. J Clin Gastroenterol. 2017;51(8):659-668.
- Hirano I, et al. Approaches and challenges to management of pediatric and adult patients with eosinophilic esophagitis. Gastroenterology. 2020;158(4):840-
- Aceves SS, et al. Endoscopic approach to eosinophilic esophagitis: American Society for Gastrointestinal Endoscopy Consensus Conference. Gastrointest Endosc. 2022;96(4):576-592.
- Bredenoord AJ, et al. Disease Burden and Unmet Need in Eosinophilic Esophagitis. Am J Gastroenterol. 2022;117(8):1231-1241.
- O’Shea KM, et al. Pathophysiology of eosinophilic esophagitis. Gastroenterology. 2018;154(2):333-345.
- Hill DA, Spergel JM. The immunologic mechanisms of eosinophilic esophagitis. Curr Allergy Asthma Rep. 2016;16(2):9.
MAT-ES-2502545-V1 – September 2025