注意を要する副作用とその対応
定期的なモニタリングが必要な副作用
以下に示す副作用では定期的なモニタリングが必要となります。発現した際の対処法と合わせて参照してください。
間質性肺炎
「発現状況」、「投与前・投与中の留意点」、「治療法」、「参考症例」について
詳細は、以下よりご覧ください。
その他重大な副作用
「発現状況」、「投与前・投与中の留意点」、「治療法」、「参考症例」について
詳細は、以下よりご覧ください。
間質性肺炎
【本剤による間質性肺炎について】
本剤における間質性肺炎については、国内での発売後約5ヵ月間(2003年9月12日〜2004年1月30日)に3,470例の患者に本剤の投与が行われ、2004年1月30日までに間質性肺炎の発現あるいは悪化が18例報告され、そのうち6例が死亡例であった。
18例中12例に合併症または既往歴として間質性肺炎、肺線維症等の肺障害、日和見感染による肺炎が含まれていたことから、2004年1月27日に緊急安全性情報をもって、これら間質性肺炎等の既往・合併のある患者に対する投与を避けていただく等の注意喚起を行い、また、添付文書の「警告」及び「使用上の注意」の改訂を行った。
間質性肺炎の発現状況
本剤の販売開始直後より死亡例を含む間質性肺炎の報告があったことから、間質性肺炎を全例調査の重点項目に追加し、「警告」及び「使用上の注意」改訂の安全対策による間質性肺炎の発現頻度低下の確認と背景因子の検討を目的として、2010年10月15日までに投与を開始した症例を対象とした全例調査を実施した。
全例調査の結果
間質性肺炎を発現した症例数
再審査期間及び再審査期間終了日以降(平成15年4月16日~平成26年6月30日)に報告された間質性肺疾患(非重篤症例を含む):101例。
自発症例を含むため発現頻度の算出は不能であることから、売上額に基づく推定使用患者数から報告率を算出した。
表:再審査期間及び再審査期間終了日以降(平成15年4月16日~平成26年6月30日)に報告された間質性肺疾患の暦年毎の症例数、報告率
|
暦年 |
間質性肺疾患の |
推定使用患者数* |
報告率 |
|
平成15年(4月16日~) |
14 |
1,588 |
0.88 |
|
平成16年 |
50 |
2,391 |
2.09 |
|
平成17年 |
15 |
1,941 |
0.77 |
|
平成18年 |
3 |
2,251 |
0.13 |
|
平成19年 |
4 |
2,227 |
0.18 |
|
平成20年 |
4 |
2,400 |
0.17 |
|
平成21年 |
3 |
2,336 |
0.13 |
|
平成22年 |
3 |
2,551 |
0.12 |
|
平成23年 |
2 |
2,620 |
0.08 |
|
平成24年 |
1 |
2,791 |
0.04 |
|
平成25年 |
2 |
3,057 |
0.07 |
|
平成26年(~6月30日) |
0 |
1,514 |
0 |
*推定使用患者数は、暦年毎の出荷数量、アラバ錠 使用成績調査における平均維持用量17.6 mgから次の計算式により算出した。
[推定使用患者数]=[出荷数量mg]/([平均維持用量17.6mg]×365日)
再審査報告書より抜粋
背景因子
全例調査における患者背景因子の層別解析の結果、間質性肺炎または肺線維症の既往歴・合併症が重要な背景因子であると考えられた。
|
投与開始日 |
解析対象症例数 |
間質性肺炎の発現症例数 |
発現率 |
検定結果 | |
|
症例数 |
6,878例 |
72例 |
1.05% |
- | |
|
間質性肺炎または肺線維症の既往/合併 |
無 |
6,006例 |
37例 |
0.62% |
Fisher |
|
有 |
669例 |
34例 |
5.08% | ||
| 不明・未記載 |
203例 |
1例 |
0.49% |
- | |
発現時期
全例調査の安全性解析対象症例6,878例において、間質性肺炎を発現した72例の発現(初発)までの日数は以下のとおりであった。
|
最小日数 |
7日 |
最大日数 |
163日 |
平均日数 |
77.92日 |
重篤性・転帰
全例調査の安全性解析対象症例6,878例で間質性肺炎を発現した72例における重篤性の内訳は、重篤62例非重篤10例であった。また、重篤性別の転帰は以下のとおりである。
|
回復 |
軽快 |
未回復 |
死亡 |
後遺症 |
不明 | |
|
重篤例 62例 |
20 (32.3%) |
15 (24.2%) |
4 (6.5%) |
20 (32.3%) |
1 (1.6%) |
2 (3.2%) |
|
非重篤例 10例 |
4 (40.0%) |
2 (20.0%) |
1 (10.0%) |
0 (0.0%) |
0 (0.0%) |
3 (30.0%) |
投与前・投与中の留意点
|
時期 | 検査 | 確認事項 | 対応 |
|
投与開始前 | 胸部X線、可能であれば高分解能CT(HR-CT)検 査 | 間質性肺炎・肺線維症、日和見感染による肺炎の合併または既往の有無 | 既存肺病変をもつ患者へのアラバの投与を避ける |
| 低アルブミン血症・高齢・喫煙歴有などの背景因子の有無 | これら背景因子がある場合、投与量の減量を考慮するなど慎重に投与する | ||
|
投与中 | 血液検査 【異常時】 胸部X線、動脈血酸素分圧(PaO2)等 | KL-6、CRP、LDH 発熱・咳嗽・呼吸困難等の自覚症状 |
|
治療法
- 患者が呼吸器症状を訴えて来院した場合、パルスオキシメーター等を使用して血中酸素飽和度を測定する。
酸素飽和度が低下していた場合はアラバの内服を中断しコレスチラミンの内服による薬物除去を開始する。
コレスチラミンによる薬物除去前後の血漿中の活性代謝物濃度測定をMRを通じ依頼する。
(薬物除去方法と代謝物の半減期 参照)
- 胸部X線写真(又はHR-CT)撮影を行い投与前の画像と比較する。呼吸器感染症専門医、放射線専門医との連携をとることが望ましい。
| 限局的肺病変が認められた場合 |
| 薬剤性肺障害は否定的である。 肺感染症を疑い、病原微生物の検出を行うと共に抗生物質等の投与を行う。 |
| びまん性肺病変が認められた場合 |
| β-D-グルカン、PCR、アンチゲネミア法、血液培養等により日和見肺感染症の鑑別診断を行う。 鑑別診断には数日を要するため、感染性肺炎が否定できない場合は抗生物質およびST合剤の治療を開始し、可能性に応じて抗MRSA治療剤、抗真菌剤、抗ウイルス剤などの追加を考慮する。 薬剤性肺障害が疑われる場合は患者の状況に応じ、ステロイド大量療法・パルス療法等適切な治療を実施する。ステロイドパルス療法施行後に易感染状態になることがあるので二次感染に気をつける。 |
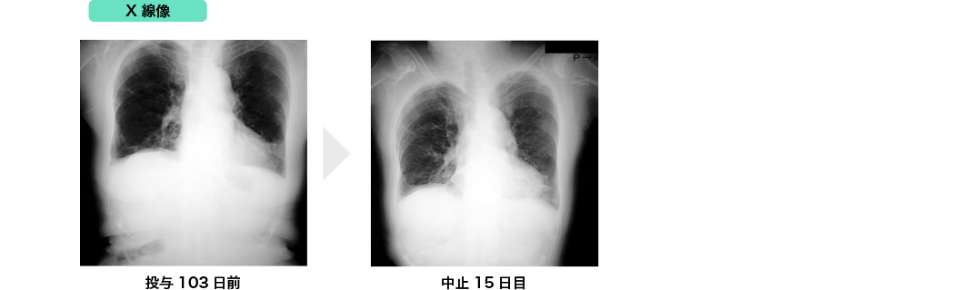
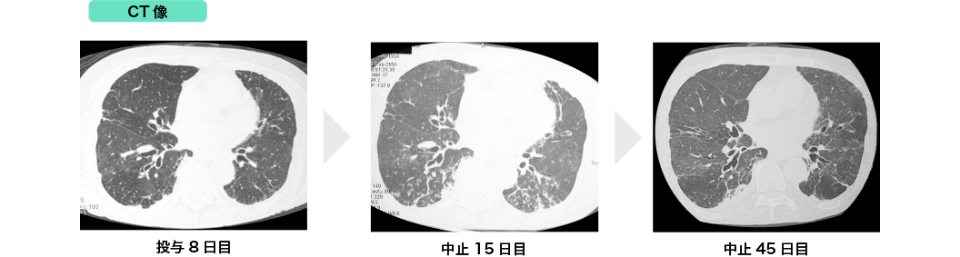
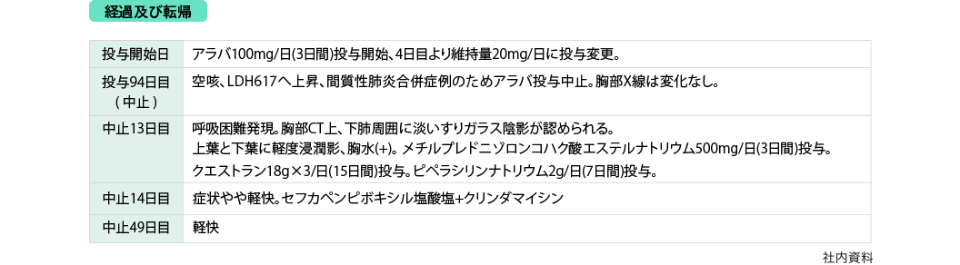
参考症例
(1) 間質性肺炎発現症例

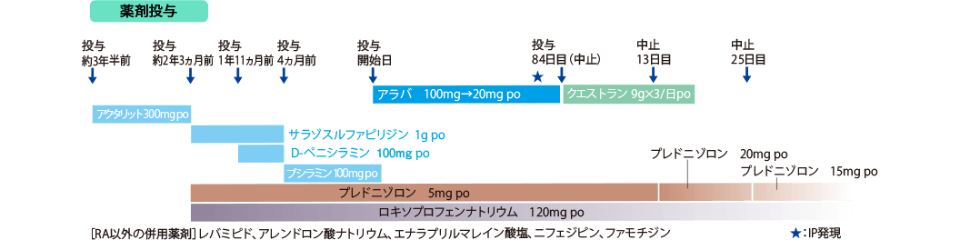
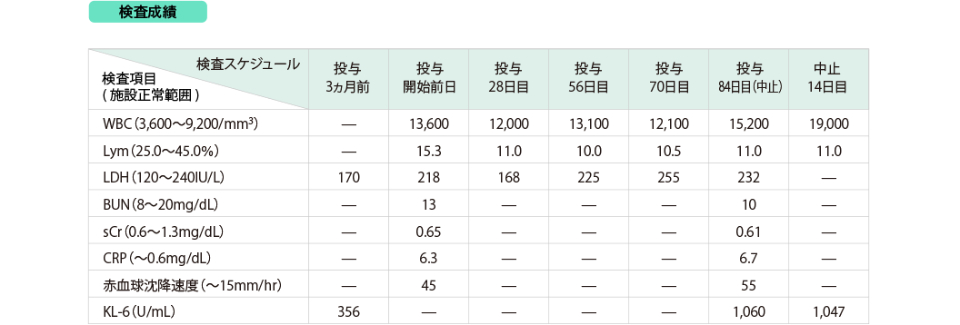
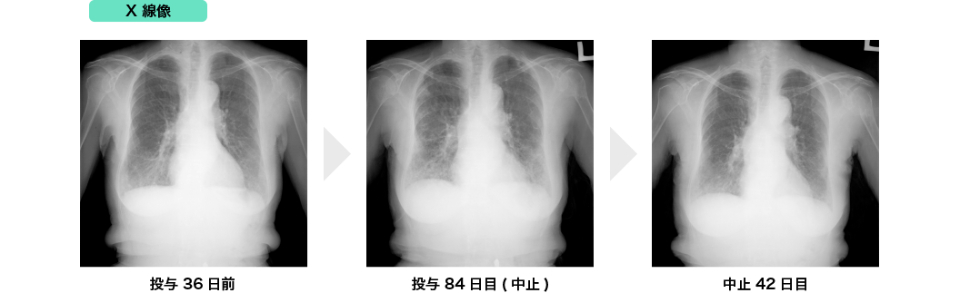


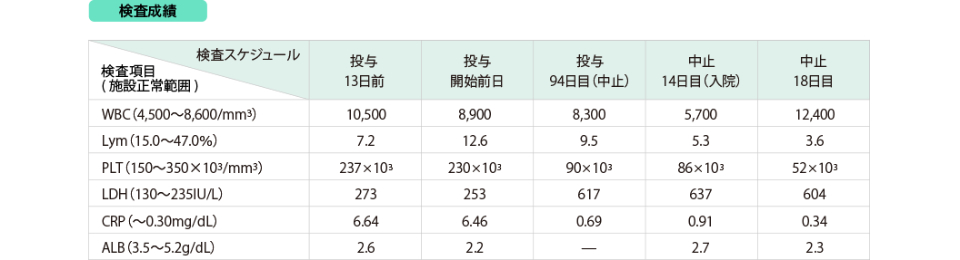
(2) 汎血球減少に伴う呼吸器感染症例


その他重大な副作用
肝機能検査値異常
AST(GOT)、ALT(GPT)、アルカリホスファターゼ等の肝機能検査値の上昇がみられる。中でもALT(GPT)は最も高い感度で反応するパラメータである。臨床試験では、肝機能検査値異常は投与開始後6ヵ月以内の初期に発現することが多かったが、その後も投与量や投与期間にかかわらず発現していたこと、また重篤な肝障害を起こす可能性もあることから、定期的なモニタリングを継続して行うことが必要となる。
〈投与前チェック〉
投与開始時に肝機能検査を行う。また、服用中はアルコールの摂取を控えるように指導する。
〈モニタリング〉
投与開始後6ヵ月間は少なくとも1ヵ月に1回、その後は1~2ヵ月に1回肝機能検査を行う。特に、ALT(GPT)の変動に注意する。
〈発現時期〉
投与開始後6ヵ月以内に起こることが多い。とくに、1〜8週での発現率が最も高く、その後発現率は低下する。
〈程度・経過〉
ほとんどは軽度~中等度で可逆的である。
海外第Ⅲ相臨床試験及びその継続長期投与試験において、基準値上限の2倍までのALT(GPT)の上昇では、その80%以上がアラバの減量もしくは減量することなしに投与継続中に正常値まで回復した。ALT(GPT)が基準値上限の2倍を超えたときの回復率は、減量した場合は92%であったが、減量しなかった場合は76%であった。
対処法
ALT(GPT)の上昇の程度により、下記のように対処する。
| 基準値上限の2~3倍 | 維持量を10mg/日に減量 頻回に肝機能検査を行う |
| 基準値上限の3倍以上 | 投与を中止 薬物除去法を施行する等、適切な処置を行う |
| 減量後も基準値上限の2~3倍値が持続 | 投与を中止 薬物除去法を施行する等、適切な処置を行う |
ウイルス性肝炎
B型肝炎ウイルスキャリアの患者又は既往感染者(HBs抗原陰性、かつHBc抗体又はHBs抗体陽性)において、B型肝炎ウイルスの再活性化による肝炎が現れることがある。また、C型肝炎ウイルスキャリアの患者において、C型肝炎の悪化がみられることがある。肝炎ウイルスキャリアの患者に本剤を投与する場合は、肝機能検査値や肝炎ウイルスマーカーのモニタリングを行うなど、B型肝炎ウイルスの再活性化やC型肝炎の悪化の徴候や症状の発現に注意する必要がある。
〈投与前チェック〉
投与開始時に肝機能検査を行う。
肝炎ウイルス感染の既往歴、家族歴、現在の感染の有無を確認する。
キャリアと診断された場合、あらかじめ肝臓専門医による治療を行ったのちに、関節リウマチの治療を開始することを検討する。
〈モニタリング〉
投与開始後6ヵ月間は少なくとも1ヵ月に1回、その後は1~2ヵ月に1回肝機能検査を行う。
肝炎ウイルスキャリアの患者又はB型肝炎の既往感染者に本剤を投与する場合は、肝炎ウイルスマーカーのモニタリングも行うなど、B型肝炎ウイルスの再活性化やC型肝炎の悪化の徴候や症状の発現に注意する。
〈発現時期〉
一定の傾向は不明である。
〈程度・経過〉
一定の傾向は不明である。
〈対処法〉
B型肝炎ウイルスの再活性化やC型肝炎の悪化の徴候や症状の発現が疑われたら、投与を中止し、肝臓専門医と協力して治療を行う。
血球減少/骨髄抑制
血液学的検査において臨床的に問題となる臨床検査値異常のうち、白血球数の減少(<2,000/mm3)、好中球数の減少(<1,000/mm3)、血小板数の減少(<50,000/mm3)を示す症例は、骨髄抑制が起きている可能性が高い。
臨床試験において、血液学的検査上、骨髄抑制が起きている可能性のある症例はアラバ群の0.1~0.2%にみられたが、いずれも一過性であった。しかし、国内臨床試験や海外の市販後において汎血球減少症等が報告されており、これらの副作用を早期に発見するため、血液学的検査を定期的に行う必要がある。
〈投与前チェック〉
投与開始時に白血球分画を含む血液学的検査を行う。
〈モニタリング〉
投与開始後6ヵ月間は2週間に1回、その後は1~2ヵ月に1回、白血球分画を含む血液学的検査を行うこと。特に以下の患者に対しては、より頻回に血液学的検査を行う必要がある。
- 免疫抑制剤や他のDMARDs等の血液毒性を有する薬剤を最近まで投与されていたか、投与中の患者。
- 貧血、白血球減少症、血小板減少症、骨髄機能低下、骨髄抑制のある患者、及びこれらの既往歴のある患者。
〈発現時期〉
投与開始後6ヵ月以内に起こることが多い。とくに、2~8週での発現率が高い。
〈程度・経過〉
多くは一過性であるが、汎血球減少症等、重篤なケースに至ることもある。以下に国内臨床試験例を示す。
血球減少症の発現時期と経過
<白血球減少症>
|
発現時 |
回復時 |
投与開始時 | ||||||
|
投与開始後期間 |
WBC |
重症度 |
経過 |
期間 |
WBC |
WBC |
転帰 | |
| 1 |
2週 |
3,800 |
軽度 |
継続 |
投与開始後4週 |
4,200 |
5,700 |
回復 |
| 2 |
2週 |
3,100 |
中等度 |
中止 |
投与終了後4週 |
7,700 |
7,000 |
回復 |
| 3 |
4週 |
3,100 |
軽度 |
継続 |
投与開始後8週 |
8,500 |
7,300 |
回復 |
| 4 |
4週 |
3,700 |
軽度 |
継続 |
投与開始後8週 |
7,000 |
7,600 |
回復 |
| 5 |
8週 |
4,100 |
中等度 |
中止*1 |
投与終了後4週 |
8,600 |
7,900 |
回復 |
| 6 |
16週 |
3,400 |
軽度 |
継続 |
投与開始後20週 |
4,700 |
4,680 |
回復 |
| 7 |
20週 |
3,250 |
軽度 |
中止 |
投与終了後4週 |
4,540 |
4,900 |
回復 |
*1
回復後、再投与を開始した
<血小板減少症>
|
発現時 |
回復時 |
投与開始時 | ||||||
|
投与開始後期間 |
PLT |
重症度 |
経過 |
期間 |
PLT |
PLT |
転帰 | |
| 1 |
18日 |
12.4 |
中等度 |
中止 |
投与終了後4週 |
27.8 |
45.6 |
回復 |
| 2 |
2週 |
9.4 |
中等度 |
中止 |
投与終了後4週 |
22.2 |
25.6 |
回復 |
| 3 |
8週 |
12.9 |
軽度 |
継続 |
投与開始後20週 |
15.4 |
33.4 |
回復 |
| 4 |
8週 |
11.2 |
重度 |
中止*2 |
投与終了後8週 |
7.3↓*3 |
25.4 |
回復 |
| 5 |
24週 |
11.9 |
軽度 |
継続 |
投与開始後28週 |
20.7 |
25.7 |
回復 |
*2 回復後、再投与を開始した
*3 投与終了後、8週では回復がみられなかった
〈対処法〉
検査値の経過に回復傾向がみられなければ、減量又は投与を中止して薬物除去法を考慮する。必要があれば輸血やG-CSF製剤を使用する。
高血圧/血圧上昇
原因は不明であるが、軽度~中等度の血圧上昇が現れることがある。海外第Ⅲ相臨床試験においては、重篤な血圧上昇が0.2%発現している。
また、海外の臨床試験においては、高血圧の既往歴や投与前から血圧の高い場合に発現する例が多かった。
〈投与前チェック〉
投与開始時に血圧を測定する。
〈モニタリング〉
定期的に血圧を測定する。
〈発現時期〉
投与開始後1~8週が最も多く、その後はバラツキがあるものの減少傾向を示す。
〈程度・経過〉
軽度〜中等度であり、投与期間中に回復することが多い。海外での市販後において、重度の高血圧
(収縮期血圧200mmHg以上、拡張期血圧115mmHg以上)が自発報告されている。
〈対処法〉
投与を継続しながら経過を観察する。回復傾向がみられなければ減量又は投与を中止し、必要があれば降圧剤を使用する。
結核
結核が現れることがあるので、観察を十分に行い、異常が認められた場合には、投与を中止するなどの適切な処置を行う。
結核の既感染者では症状の顕在化及び悪化のおそれがあるため、本剤の投与に先立って結核に関する十分な問診及び胸部X線検査に加え、インターフェロン-γ遊離試験又はツベルクリン反応検査を行い、適宜胸部CT検査等を行うことにより、結核感染の有無を確認する。結核の既往歴を有する場合及び結核を疑う症状(持続する咳、発熱等)が発現した場合には、結核の診療経験がある医師にコンサルトする。
〈投与前チェック〉
本剤投与に先立って結核に関する十分な問診及び胸部X線検査に加え、インターフェロン-γ遊離試験又はツベルクリン反応検査を行い、適宜胸部CT検査等を行うことにより、結核感染の有無を確認すること。
〈モニタリング〉
胸部X線検査等の適切な検査を定期的に行う。
患者に対し、結核を疑う症状が発現した場合(持続する咳、発熱等)には速やかに主治医に連絡するよう説明する。
結核の活動性が確認された場合は本剤を投与しない。
〈発現時期〉
一定の傾向は不明である。
〈程度・経過〉
一定の傾向は不明である。
〈対処法〉
結核の既往歴を有する場合及び結核を疑う症状(持続する咳、発熱等)が発現した場合には、結核の診療経験がある医師にコンサルトする。以下のいずれかの患者には、原則として抗結核薬を投与した上で本剤を投与する。
- 胸部画像検査で陳旧性結核に合致するか推定される陰影を有する患者
- 結核の治療歴(肺外結核を含む)を有する患者
- インターフェロン-γ遊離試験やツベルクリン反応検査等の検査により、既感染が強く疑われる患者
- 結核患者との濃厚接触歴を有する患者
結核の活動性が確認された場合には、本剤の投与を中止し、結核の診療経験がある医師と協力して治療を行う。
