- Wissen
- Quelle: Campus Sanofi
- 08.07.2025
Diagnose Typ-1-Diabetes: Augen auf bei diesen Patienten

Besonders hohes Risiko bei Verwandten von Menschen mit T1D
Typ-1-Diabetes (T1D) ist in fast allen Fällen autoimmunbedingt und zeichnet sich durch eine progressive Zerstörung der insulinproduzierenden Betazellen des Pankreas aus.1 Die genauen Auslöser sind bis dato nicht eindeutig bekannt, jedoch haben insbesondere nahe Verwandte von Menschen mit T1D ein erhöhtes Risiko selbst zu erkranken. So weisen Kinder von Müttern mit T1D bereits ein 10-fach erhöhtes Risiko auf. Sind gleich mehrere Verwandte an T1D erkrankt, steigt dies noch weiter (Abb. 1).2
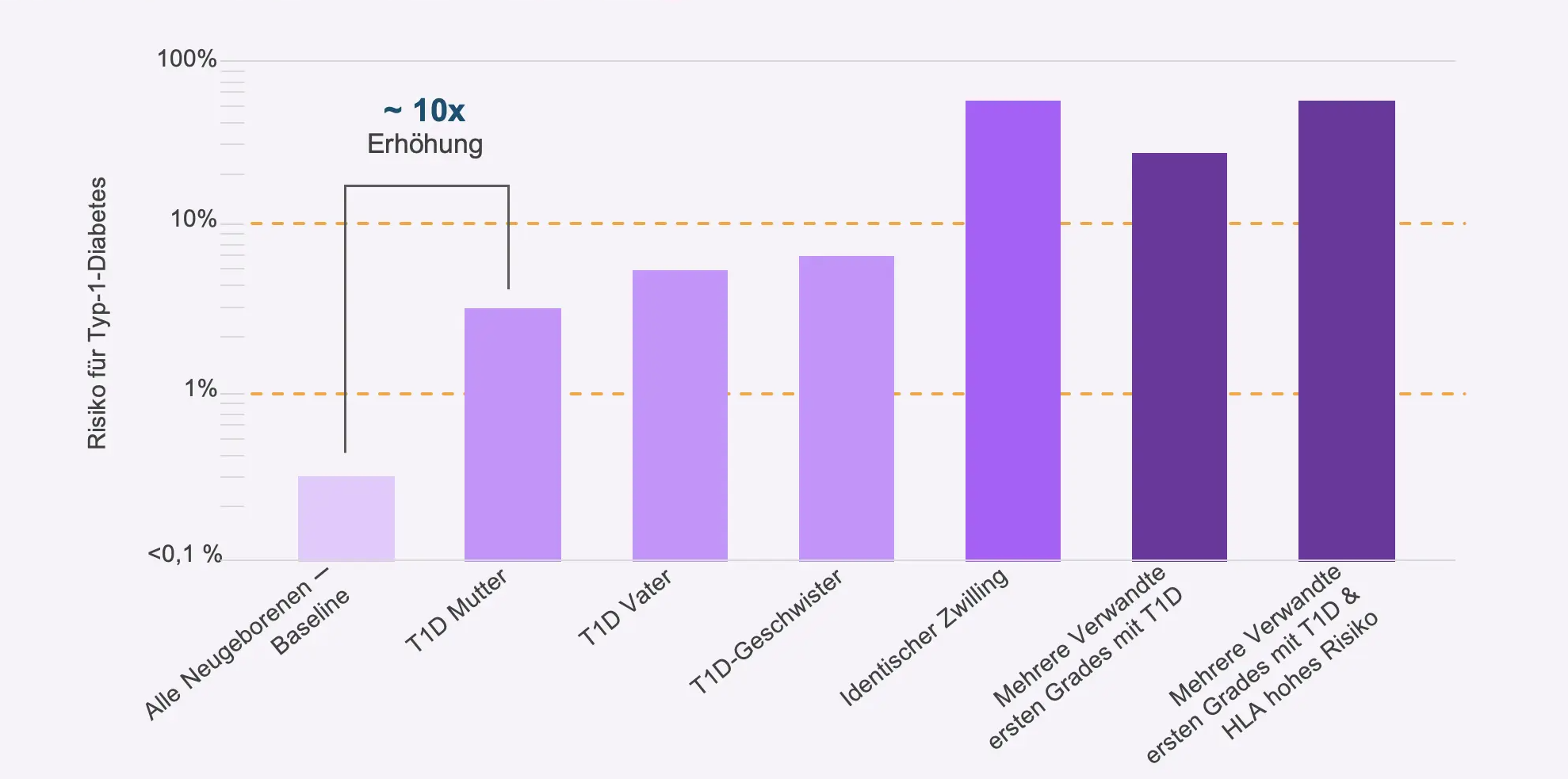
T1D in der Familie: Wissen schützt Kinder nicht automatisch
Gerade bei Kindern mit T1D von ebenfalls erkrankten Eltern sollte ein besonderes Augenmerk auf der Stoffwechselkontrolle liegen. Man würde allgemein davon ausgehen, dass aufgrund des höheren Wissensstands zum Therapiemanagement und der Erkrankung selbst, Kinder von Eltern mit T1D eine bessere glykämische Kontrolle aufweisen.
Eine aktuell publizierte schwedische Studie konnte dies widerlegen. Dabei wurde die Stoffwechselkontrolle und das Risiko für langfristige Komplikationen – insbesondere Nierenversagen und vorzeitiger Tod – bei Personen mit T1D mit Krankheitsbeginn im Kindesalter untersucht.3 Es wurden Betroffene mit einem an T1D erkrankten Elternteil zum Zeitpunkt der eigenen Diagnose (elterlicher Diabetes) mit solchen verglichen, deren Eltern keinen T1D hatten (sporadischer Diabetes).3 Im Einklang mit früheren Studien deuten die Ergebnisse darauf hin, dass die Stoffwechselkontrolle bei Personen mit elterlichem Diabetes tendenziell schlechter ist.3
Grund dafür sind vermutlich soziale Faktoren wie die Weitergabe veralteter Therapiestrategien durch die Eltern, sowie negative Erfahrungen mit akuten Komplikationen oder Spätfolgen bei den Eltern. Ebenfalls ist es möglich und wahrscheinlich, dass genetische Faktoren den Krankheitsverlauf beeinflussen – dies bedarf jedoch weiterer Nachforschungen.3
Ähnliche Ergebnisse lieferte eine retrospektive Datenanalyse, die auf dem Kongress der Deutschen Diabetes Gesellschaft im Mai 2025 vorgestellt wurde. Hierbei wurden 218 Kinder mit neu manifestiertem T1D untersucht. Es stellte sich heraus, dass das Vorhandensein eines erstgradigen Verwandten in der Familie (Elternteil oder Geschwisterkind) mit T1D nicht vor schwerwiegenden Komplikationen, wie der diabetischen Ketoazidose (DKA), schützt. So war die DKA-Prävalenz vergleichbar bei Kindern mit bzw. ohne erstgradigen Verwandten.4
Erhöhtes Risiko für T1D bei Zöliakie und Schilddrüsenerkrankungen
T1D ist häufig mit anderen endokrinen Autoimmunerkrankungen assoziiert, einschließlich Zöliakie und Schilddrüsenerkrankungen (z. B. Hashimoto-Thyreoiditis).5-7
Eine retrospektive Kohortenstudie Studie zeigte kürzlich, dass während einer medianen Nachbeobachtungszeit von etwa 2 Jahren das Risiko, an T1D zu erkranken, bei Personen mit Zöliakie (Hazard Ratio [HR] = 2,54), Hyperthyreose (adjustierte HR = 2,98) und Hypothyreose (HR = 2,41) 2-3-fach höher ist als bei den jeweiligen Kontrollpersonen ohne diese Erkrankungen.8
Angesichts des erhöhten Risikos, an T1D zu erkranken, könnte eine T1D-Früherekennung auf Inselautoantikörper bei Personen mit Zöliakie, Hypothyreose und Hyperthyreose somit hilfreich sein, um T1D bereits in präsymptomatischen Stadien zu diagnostizieren.8
Frühdiagnose von T1D
T1D äußert sich in 3 Stadien: Von den präsymptomatischen Stadien 1 und 2 zur klinischen Manifestation (Stadium 3).9,10 Der Langzeit-T1D wird auch als Stadium 4 bezeichnet.
Über einen Nachweis von ≥ 2 Autoantikörpern kann mit einer Sicherheit von nahezu 100 % eine T1D-Diagnose in präsymptomatischen Stadien erfolgen.11
T1D assoziierte Autoantikörper, die zur Früherkennung herangezogen werden können, sind:12
- Insulinautoantikörper (IAA)
- Autoantikörper gegen Glutamat-Decarboxylase (GADA)
- Autoantikörper gegen Insulinoma-assoziiertes Antigen-2 oder Tyrosinphosphatase IA2 (IA-2A)
- Autoantikörper gegen den Zink-Transporter 8 (ZnT8A)
- Inselzellantikörper (ICA)
Ziel der Früherkennung von T1D ist es, einer diabetischen Ketoazidose bei Manifestation vorzubeugen und gleichzeitig den optimalen Zeitpunkt für den Beginn einer Insulintherapie zu ermitteln.12 Patienten mit einer bestätigten Diagnose von T1D im Stadium 2 können auch zugelassene Therapien angeboten werden.18
Welche Personen sollten für eine Testung auf Typ-1-Diabetes in Betracht gezogen werden?
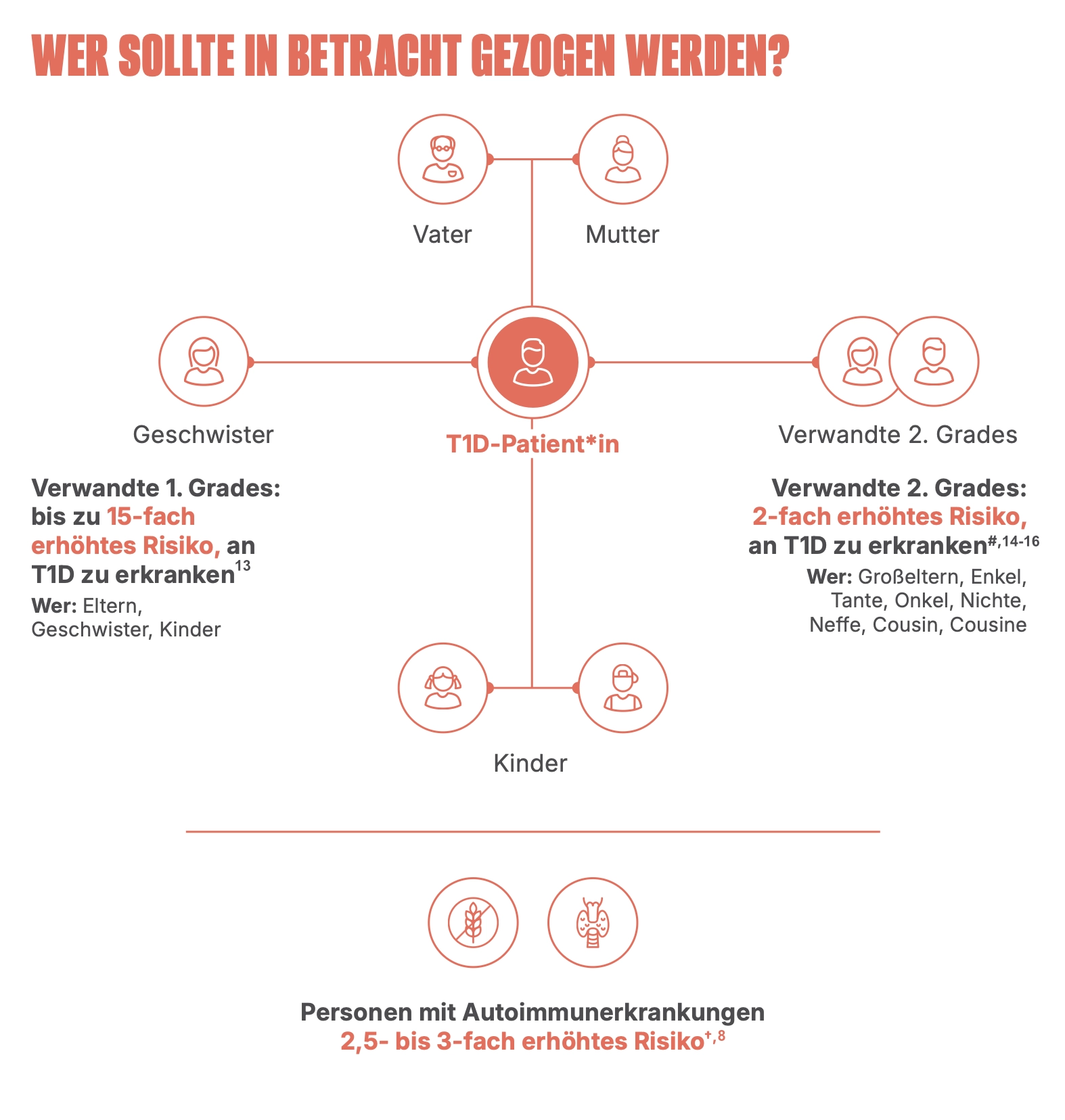
Alle Kinder (2-10 Jahre) in teilnehmenden Bundesländern können im Rahmen der Fr1da-Studie auf T1D-Autoantikörper getestet werden.
Für Verwandte von Menschen mit T1D (1-21 Jahre) mit Wohnsitz in Deutschland ist eine Testung auf T1D-Autoantikörper im Rahmen der Fr1da-Studie für Verwandte ebenfalls bundesweit möglich.
Erfahren Sie hier mehr zu den Früherkennungsstudien.
Darüber hinaus kann es sinnvoll sein, bei den Gesundheits-Check-Ups für Erwachsene (für alle gesetzlich Versicherten in Deutschland einmalig im Alter von 18-34 und ab 35 Jahren alle 3 Jahre) auch auf T1D zu achten, denn ca. 62 % der Betroffenen entwickeln einen klinisch manifesten T1D erst nach dem 20. Lebensjahr.17 So kann im Rahmen des Check-Ups ein erhöhter Nüchtern- oder Gelegenheitsblutzuckerwert auf eine beginnende Stoffwechselveränderung hinweisen und Anlass für eine zusätzliche Autoantikörper-Testung geben.
Empfehlungen nach erfolgter Autoantikörper-Testung
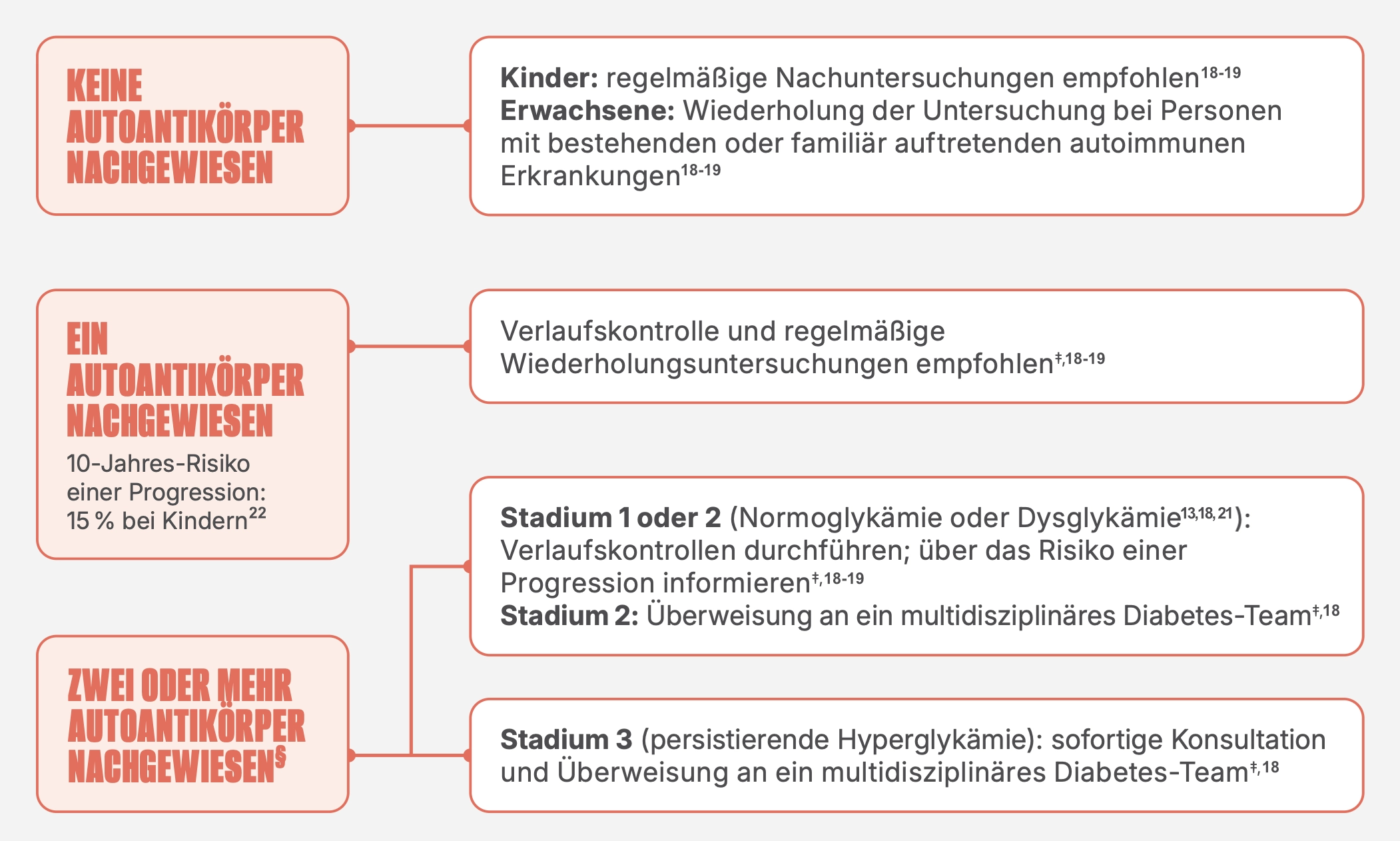
Ausführliche Information zum Monitoring von T1D in präsymptomatischen Phasen finden sie hier.
ICD-10 Codes - T1D präsymptomatische Stadien
R76.80
Diabetes mellitus Typ 1, präsymptomatisch, Stadium 1 23
Definition:
Nachweis von mindestens 2 Inselzellauto-antikörpern ohne metabolische Auffälligkeiten
Keine Kodierung zusammen mit Diabetes mellitus (E10–E14) oder Diabetes mellitus Typ 1, präsymptomatisch, Stadium 2 (R73.00)
R73.00
Diabetes mellitus Typ 1, präsymptomatisch, Stadium 2 24
Definition:
Nachweis von mind. 2 Inselzellautoantikörpern und zusätzlich mind. eines der folgenden Kriterien:
- Gestörte Glukosetoleranz (2-Stunden-Plasma-glukose 140-199 mg/dl bzw. 7,8-11,0 mmol/l)
- Gestörte Nüchtern-Plasmaglukose (FPG 100-125 mg/dl bzw. 5,6-6,9 mmol/l)
- HbA1c-Werte zwischen 5,7 und 6,4 % bzw. 39-47 mmol/mol oder Anstieg des HbA1c ≥ 10 %
Keine Kodierung zusammen mit Diabetes (E10–E14), Störungen beim Neugeborenen (P70.0-P70.2), Diabetes mellitus während der Schwangerschaft, der Geburt und des Wochenbettes (O24.-), postoperativer Hypoinsulinämie, außer pankreopriver Diabetes mellitus (E89.1).
# Verglichen mit der Allgemeinbevölkerung13 oder berechnetes relatives Risiko
† Basierend auf einer retrospektiven, beobachtenden, paarweise abgeglichenen Kohortenstudie mit Real-World-Daten aus der Optum-Clinformatics-Abrechnungsdatenbank, die Personen mit Zöliakie, Hyperthyreose (einschließlich Morbus Basedow) und Hypothyreose (einschließlich Hashimoto-Thyreoiditis) einschloss.8
‡ Diese Empfehlungen wurden von einer Reihe von Expertenarbeitsgruppen entwickelt, die im Rahmen einer Breakthrough-T1D-Initiative einberufen wurden.18,20
§ Bei einigen Personen mit zuvor bestätigten multiplen Autoantikörpern kann eine Rückkehr zu einem singulären oder negativen Autoantikörperstatus auftreten.18
- S3-Leitlinie Therapie des Typ-1-Diabetes. AWMF online 2023. Reg.-Nr.: 057-013; unter: https://register.awmf.org/assets/guidelines/057-013l_S3-Therapie-Typ-1-Diabetes_2023-09_1.pdf. Zuletzt abgerufen am 07.04.2026.
- Bonifacio E. Diabetes Care. 2015;38(6):989-996.
- Fredriksson M et al. BMJ Open Diabetes Res Care. 2025;13(1).
- Niemeyer M et al. Diabetologie und Stoffwechsel. 2025;20(S01):S78.
- Frommer L, Kahaly GJ. World J Diabetes. 2020;11(11):527-539.
- Popoviciu MS et al. J Pers Med. 2023;13(3).
- Naredi Scherman M et al. Front Pediatr. 2024;12:1386513.
- Edelman SV et al. Diabetes Obes Metab. 2025.
- Insel RA et al. Diabetes Care. 2015;38(10):1964-1974.
- American Diabetes Association Professional Practice Committee. 2. Classification and Diagnosis of Diabetes: Standards of Medical Care in Diabetes-2022. Diabetes Care. 2022;45(Suppl 1):S17-s38.
- Insel RA et al. Diabetes Care 2015; 38: 1964-74.
- Deutsche Diabetes Gesellschaft (DDG). S3-Leitlinie Diagnostik, Therapie und Verlaufskontrolle des Diabetes mellitus im Kindes- und Jugendalter. AWMF online 2023. Reg.-Nr.: 057-016; unter https://www.ddg.info/fileadmin/user_upload/05_Behandlung/01_Leitlinien/Evidenzbasierte_Leitlinien/2023/S3_DM_Kinder_Jugendliche_20231113_Langfassung.pdf. Zuletzt abgerufen am 07.04.2026.
- Haller MJ et al. Horm Res Paediatr 2024; 97: 529–45.
- Weires MB et al. Exp Clin Endocrinol Diabetes 2007; 115: 634–40.
- Parkkola A et al. Diabetes Care 2013; 36: 348–54.
- Allen C et al. Diabetes 1991; 40: 831–6.
- Gregory GA et al. Lancet Diabetes Endocrinol 2022; 10: 741–60.
- Phillip M et al. Diabetes Care 2024; 47: 1276–98.
- Moore DJ et al. Int J Gen Med 2024; 17: 3003–14.
- Juvenile Diabetes Research Foundation. New guidance sets out how to support people with early stage type 1 diabetes. Erhältlich unter https://breakthrought1d.org.uk/news/new-guidance-sets-out-how-to-support-people-with-early-stage-type-1-diabetes/. Zuletzt abgerufen am 07.04.2026.
- Breakthrough T1D. The stages of type 1 diabetes. Erhältlich unter https://breakthrought1d.org.au/what-is-t1d/stages/. Zuletzt abgerufen am 07.04.2026.
- Ziegler AG et al. JAMA 2013; 309.
- ICD-10-GM R76.80. Erhältlich unter: https://klassifikationen.bfarm. de/icd-10-gm/kode-suche/htmlgm2026/block-r70-r79.htm. Zuletzt abgerufen am 09.04.2026.
- ICD-10-GM R73.00. Erhältlich unter: https://klassifikationen. bfarm.de/icd-10-gm/kode-suche/htmlgm2026/block-r70-r79.htm#R73.00. Zuletzt abgerufen am 09.04.2026.
MAT-DE-2502770-1.0-04/2026