- Article
- Source : Campus Sanofi
- 19 mai 2022
Médecine de précision : de quoi parle-t-on ?

La médecine évolue, ce n’est pas un scoop. Avec cette progression, de nouveaux termes voient le jour. Médecine de précision, médecine personnalisée, médecine 5P, médecine 6P… il n’est pas toujours facile de s’y retrouver !
Voyons ce qu’impliquent ces notions et quels en sont les enjeux.
Une empreinte unique à chaque patient
Médecine de précision et médecine personnalisée, deux termes pour une même définition.
L’objectif étant d’améliorer la prévention ou l’évolution clinique, en proposant au patient un traitement adapté, plus ciblé. Pour cela la médecine de précision est multidimensionnelle. Et non plus basée uniquement sur la pathologie : 1,2
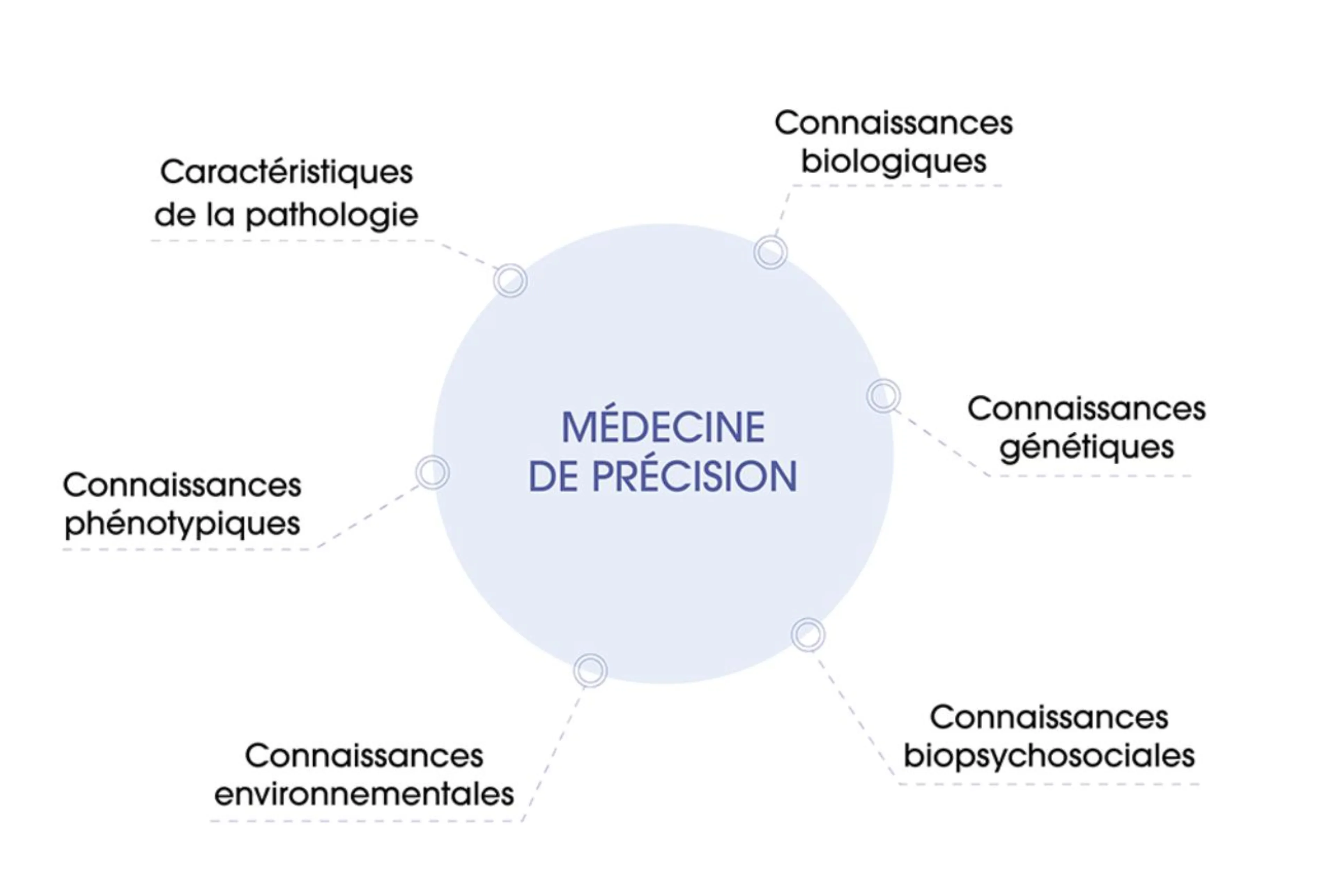
La médecine de précision s’appuie sur les connaissances environnementales, biopsychosociales, génétiques, biologiques, phénotypiques et sur les caractéristiques de la pathologie. L’ensemble de ces données constituent alors comme une empreinte unique à chacun, une signature individuelle complexe qui caractérise un organisme dans son ensemble.¹
Scientifiques et ingénieurs sur le front
Tout cela n’aurait pas été rendu possible sans un nombre considérable de progrès à la fois scientifiques ET technologiques !3
Cela va de pair. D’un côté les progrès scientifiques ont permis de mieux comprendre les mécanismes physiopathologiques donnant lieu au développement de diverses maladies, notamment les cancers. D’un autre, le séquençage de l’ADN utilise des technologies de plus en plus performantes.
On obtient alors de véritables profils moléculaires pour chaque patient et pour chaque tumeur. Car il n’existe pas UN, mais DES cancers pour un organe donné et chaque tumeur est spécifique.2,3
La combinaison de ces deux composantes permet alors l’entre-croisement d’un grand nombre d’informations et de données médicales pouvant donner lieu à un ciblage de grande précision en termes de choix thérapeutique.(2,3)
Médecine de précision et cancer
C’est dans le domaine de l’oncologie que la médecine de précision voit ses premières applications concrètes naître dans un premier temps.
En cancérologie, l’objectif actuel de la médecine de précision est clair : proposer au patient un traitement correspondant aux caractéristiques spécifiques de sa tumeur.2,4
En France, le développement de la médecine de précision a été favorisée par l’INCA, ayant mis en place, depuis 2006, 28 plateformes hospitalières de génétique moléculaire des cancers réparties sur l’ensemble du territoire.4 Grâce aux analyses « - omiques » (génomique, transcriptomique, métabolomique, protéomique, etc.), de nombreux essais cliniques indépendants étudiant des biomarqueurs permettant de guider la stratégie thérapeutique ont ainsi pu voir le jour.4
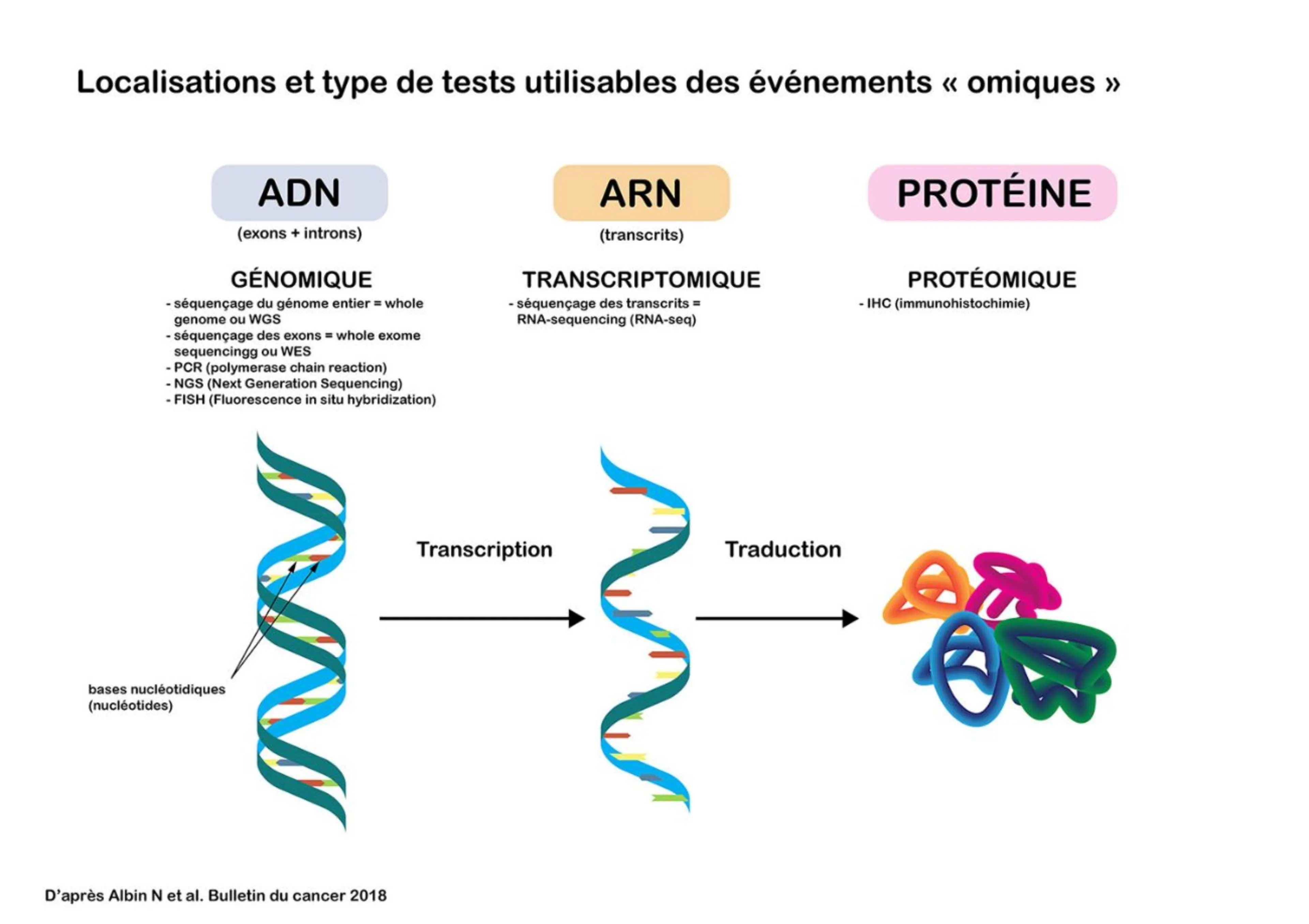
La génomique étudie l’ADN par séquençage du génome entier, séquençage des exons, par test PCR, NGS et FISH. La transcriptomique étudie l’ARN par séquençage des transcrits (RNA-seq). La protéomique étudie les protéines par test IHC.
Initialement, en oncologie, la médecine de précision donne lieu à des thérapies ciblées qui concernent des sous-groupes de patients auxquels on administre un traitement spécifique selon un biomarqueur particulier.4
Mais l’ambition est plus large et les perspectives nombreuses ! Les étapes suivantes consistent à proposer des traitements s’adressant à des groupes de patients de plus en plus spécifiques.5
L’hypothèse sous-jacente étant que cibler une seule altération moléculaire peut être insuffisant pour une action antitumorale durable.6 L’objectif est alors d’analyser la séquence complète de la tumeur pour chaque patient. Une empreinte moléculaire complète permettrait alors de prendre en compte non seulement les cellules tumorales, mais aussi leurs interactions avec leur environnement pour le choix d’un traitement réellement personnalisé.
Concrètement, quels sont les axes de progression ?6,7
Un réel changement de paradigme semble se dessiner en termes de décision thérapeutique : il serait question, pour le choix du traitement, de ne plus se baser sur la localisation de la tumeur en premier lieu, mais plutôt sur les critères moléculaires, avant de se fier aux informations histologiques, puis à la localisation de la tumeur.6,7
Cancer du foie, cancer du rein, cancer du sein ou encore de la prostate, qu’importe la localisation du moment que les analyses génomiques nous comblent d’informations précieuses pour le traitement du patient…
Par ailleurs, il ne s’agirait plus uniquement de tenir compte de l’ADN de la tumeur, mais également des données moléculaires provenant du microenvironnement de la tumeur et de l’ADN tumoral circulant. Pour le futur de la médecine de précision, ceci permettrait d’appréhender l’environnement complexe de la tumeur et son hétérogénéité, ainsi que les mécanismes de résistance à certains traitements.(6,7)
D’un point de vue technique, au-delà du séquençage de l’ADN, d’autres analyses permettraient de compléter le tableau moléculaire : les analyses épigénétiques, le séquençage de l’ARN, et la protéomique… l’objectif étant d’élargir le panel des altérations moléculaires potentiellement intéressantes en tant que cible thérapeutique.6,7
Le panel des pathologies candidates s’élargit
Aujourd’hui la médecine de précision ne se cantonne désormais plus uniquement à l’oncologie. Les maladies chroniques et certaines maladies rares notamment sont maintenant de la partie. Au fil de l’avancée de nos connaissances scientifiques, on s’aperçoit bel et bien que de nombreuses maladies sont, entre autres, impactées par la génétique et de multiples facteurs propres au patient et à son environnement.
Prenons l’exemple de pathologies inflammatoires, comme le psoriasis pour lequel le profil génétique et l’immunité jouent un rôle important. Le psoriasis résulte en effet de l’interaction de facteurs environnementaux et de prédispositions génétiques avec déjà plus de 40 gènes identifiés.8 De ces premières connaissances ont découlé de nombreuses thérapies ciblées. Avec la progression des découvertes et les analyses génétiques et transcriptomiques de plus en plus poussées, de multiples phénotypes de la maladie ont été mis à nu.
On cherche alors désormais à identifier les biomarqueurs responsables de l’efficacité des premières thérapies ciblées grâce à la médecine de précision. Les nouvelles générations de traitements permettront donc de traiter les patients de manière de plus en plus précise.8,9
Dans le diabète également, des projets d’avenir sont en cours. Et c’est justement le but du centre lillois PreciDIAB (Centre National de Médecine de Précision des Diabètes). Réel enjeu de santé publique avec près de 4 millions de personnes concernées en France (10), le diabète mobilise.
Avec pour objectif le développement de nouvelles approches médicales basées sur les données scientifiques et l’innovation, PreciDIAB a pour ambition la mise au point d’une médecine de précision d’avenir dans la prise en charge du diabète. Grâce à une méthode translationnelle et multidisciplinaire expérimentée dans un premier temps dans les métropoles lilloise et amiénoise, le projet s’étendra à l’ensemble du territoire français.
L’objectif étant d’identifier les patients à risque de complications pour ainsi les anticiper, de prévoir les mécanismes d’évolution du diabète, de prévenir les épisodes aigus, tout cela grâce à la médecine de précision.11
Avez-vous entendu parler du plan « France Médecine Génomique 2025 » ?
Tout commence en 2015, à la demande du Premier ministre Manuel Valls. Le projet, alors nommé « France Médecine Génomique 2025 », adressé à Aviesan (Alliance nationale pour les sciences de la vie et de la santé), durera 10 ans et permettra d’étudier la mise en place et les conditions d’accès au diagnostic génétique sur le territoire Français. Le but étant de faire évoluer la façon de diagnostiquer, prévenir et soigner les patients.12
La médecine génomique, c’est la médecine de précision ?
Pas vraiment, mais elles sont étroitement liées car c’est la médecine génomique, (via le séquençage du génome), qui permet notamment de développer une médecine de précision.13
La médecine génomique représente un enjeu au niveau international. En effet, des pays comme les Etats-Unis, le Royaume Uni ou encore des pays de l’Union Européenne comme l’Estonie et l’Allemagne ont déjà entrepris d’intégrer la médecine génomique dans le système de santé. Cependant, le développement d’une telle médecine dans des pays voisins de la France pourrait faire émerger un tourisme médical ! Il est alors indispensable pour la France de développer la médecine génomique sur son propre territoire. (12)
Dans ce contexte international fortement compétitif, le plan « France médecine génomique 2025 » comporte 4 types d’enjeux majeurs :12

Enjeu de santé publique :
-
Adaptation du parcours de soins nécessaire dans le but d’une prise en charge diagnostique et thérapeutique personnalisée pour un grand nombre de patients
-
Priorisation pour les patients atteints de maladies rares ou cancers
-
Puis extension progressive à l’ensemble des patients

Enjeu scientifique et clinique :
-
Renforcement de la chaine à partir de l’exploration moléculaire des pathologies jusqu’au bénéfice thérapeutique du patient
-
Regroupement et constitution de bases de données biologiques, cliniques et environnementales

Enjeu technologique :
-
Utilisation des sciences et technologies de l’information et de la communication (serveurs, logiciels, méthodes de calcul intensif) pour la fouille, l’analyse de données et la modélisation
-
Afin d’acquérir, stocker, distribuer, apparier et interpréter un nombre massif de données

Enjeu économique :
-
Optimisation des coûts grâce notamment à la diminution du nombre de bilans inadaptés et onéreux, la réduction des délais d’analyses, la suppression de certains traitements inutiles, etc.
Ainsi, dans un contexte constitué de défis et d’enjeux de taille, les objectifs du plan « France Médecine Génomique 2025 » sont les suivants :12

Placer la France dans le peloton de tête des pays engagés en médecine de précision, avec une exportation du savoir-faire de l’expertise médicale et industrielle en médecine génomique.

Intégrer la médecine génomique dans le parcours de soins et la prise en charge des pathologies communes, maladies rares et cancers.

Mettre en place une filière nationale de médecine génomique capable d’être un levier d’innovation scientifique et technologique, de valorisation industrielle et de croissance économique. La collaboration des industriels aux côtés de la recherche académique et des acteurs publiques est alors indispensable.
Concrètement, que s’est-il passé depuis 2015 ?
Dans le cadre du Plan France Médecine Génomique 2025, les deux premières plateformes de séquençage génomique à très haut débit ont vu le jour en 2017, avec une mise en service fin 2018.
Les deux projets soutenant ces plateformes, SeqOIA et AURAGEN, effectuent désormais des examens de séquençage de génome entier à partir de prélèvements sanguins et de tissus. Chaque plateforme est prévue pour séquencer et interpréter jusqu’à 18 000 génomes par an. A l’issue de 5 années tests, une évaluation approfondie de ces données de santé sera réalisée afin d’en mesurer l’apport dans le parcours de soins des patients.12,14
Le but étant, à l’horizon 2025, la mise en place de 12 plateformes de séquençage à très haut débit pour répondre aux objectifs et ainsi permettre l’accès à la médecine génomique pour tous les patients.12,14
La suite au prochain épisode… Rendez-vous au bilan en 2025 !
La médecine de précision, pièce à part entière du puzzle « Médecine 5P »
La médecine 5P, en voilà une notion qui ne cesse de ressurgir dans les médias.
Elle désigne une approche holistique de la médecine, regroupant médecine prédictive, médecine préventive, médecine participative et médecine basée sur les preuves, auxquelles s’ajoute donc la médecine de précision.
Mais avec tous ces termes, il est facile de s’y perdre ! Nous vous proposons d’éclaircir ces notions.
Pour commencer, la médecine prédictive s’adresse à des personnes non malades susceptibles de développer une pathologie. On cartographie alors les facteurs de risque responsables et les éléments protecteurs liés. Il reste cependant à encadrer cette pratique d’un point de vue éthique afin d’en évaluer les bénéfices. Dans d’autres pays, certains dépistages dès la naissance ont par exemple pu permettre de faire disparaitre des pathologies parfois très handicapantes.15
La médecine préventive, quant à elle, est plus concrète. Elle s’appuie sur l’éducation et la sensibilisation des patients à la santé. L’objectif étant de réduire les risques de développer une maladie, mais également de dépister précocement et d’améliorer la qualité de vie des patients. Le « bien-être » de l’Homme est donc le mot d’ordre de la médecine préventive.15
La médecine participative laisse une place importante au patient en tant qu’acteur de sa santé et de son parcours de soins aux côtés du professionnel de santé. En favorisant l’engagement du patient, de nombreux bénéfices se profilent : une amélioration de l’observance aux traitements, une réduction des erreurs médicales, engendrant notamment une baisse des coûts des soins.15
Enfin, la médecine des preuves, ou « evidence based medecine », repose sur un service médical rendu aux patients.16
Ajoutons à ces 4 types de médecine, la « médecine de précision » (ou médecine personnalisée), pour en ressortir ce qu’on appelle aujourd’hui la médecine « 5P ».16
On se dirige même déjà aujourd’hui vers une médecine « 6P », intégrant une progression des parcours de soins. Une étroite collaboration entre les différents acteurs en jeu est en effet nécessaire : depuis la recherche, à la prise en charge à l’hôpital et en ville, afin de favoriser une bonne transition ambulatoire et de maintenir les patients les plus âgés à domicile.
Les parcours de soins actuels évolueront vers des parcours « de santé », de manière globale, et adaptés à chacun.16 En bref, l’évolution de la médecine et de tout ce qui gravite autour a encore de belles années devant elle !
Références
- Waeber G et al. Médecine de précision : un rendez-vous à ne pas manquer pour l’interniste généraliste. Rev Med Suisse 2017 ; 13 : 133-7.
- INCA. Qu’est-ce que la médecine de précision ? Disponible sur https://www.e-cancer.fr/Comprendre-prevenir-depister/Comprendre-la-recherche/La-medecine-de-precision/Qu-est-ce-que-la-medecine-de-precision Consulté le 08.06.2022.
- Claeys A & Vialatte JS. Les progrès de la génétique : vers une médecine de précision ? Les enjeux scientifiques, technologiques, sociaux et éthiques de la médecine personnalisée. 22 janvier 2014.
- Albin N et al. Médecine de précision : une avancée majeure dans des situations spécifiques, un mythe dans les cancers réfractaires ? Bulletin du cancer 2018 ; 105(4) : 375-96.
- INCA. Médecine de précision : et demain ? Disponible sur https://www.e-cancer.fr/Comprendre-prevenir-depister/Comprendre-la-recherche/La-medecine-de-precision/Et-demain Consulté le 08.06.2022.
- Le Tourneau C et al. Molecular profiling in precision medicine oncology. Nature medicine 2019 ; 25 : 711-2.
- Institut Curie. Cancérologie et médecine de précision : vers une approche innovante et améliorée. Pr C Le Tourneau. Communiqué de presse. 29 avril 2019.
- Académie des sciences naturelles. Psoriasis : traitement personnalisé d’une maladie génétique complexe. Disponible sur https://sciencesnaturelles.ch/personalized-health-explained/personalisierte_gesundheit_und_medizin_heute_und_morgen/m_glichkeiten_heute/fallbeispiel_psoriaris Consulté le 15.06.2022.
- Gilliet M & Boehncke WH. Dermatologie : en route vers la médecine de précision. Rev Med Suisse 2016 ; 512 (2) : 627-8.
- Ministère de la Santé et de la Prévention. Diabète. Mis à jour le 07.03.2022. Disponible sur https://solidarites-sante.gouv.fr/soins-et-maladies/maladies/article/diabete Consulté le 15.06.2022.
- I-SITE ULNE. Les Hauts-de-France se dotent dans la métropole lilloise d’un Centre National de Médecine de Précision autour de la thématique du diabète. Communiqué de presse. 09.10.2019.
- AVIESAN. Plan France Médecine Génomique 2025.
- Genomic and Immunotherapy Medical Institute. Qu’est-ce que la médecine génomique ? Disponible sur http://www.gimi-institute.org/plus-dinfos/medecine-genomique.html Consulté le 08.06.2022.
- Ministère de la Santé et de la Prévention. Médecine France Génomique 2025. Mis à jour le 03.03.33. Disponible sur https://solidarites-sante.gouv.fr/systeme-de-sante-et-medico-social/recherche-et-innovation/france-genomique Consulté le 08.06.2022.
- Rajae G. La médecine du futur. Mis à jour le 04.01.2021. Disponible sur https://www.journaldunet.com/economie/sante/1496651-la-medecine-du-futur/ Consulté le 08.06.2022.
- LEEM. La médecine : vision d’aujourd’hui et de demain. Mis à jour le 19.04.2019. Disponible sur https://www.leem.org/la-medecine-vision-daujourdhui-et-de-demain#:~:text=La%20sant%C3%A9%20devient%20de%20plus,d%C3%A9velopper%20telle%20ou%20telle%20maladie. Consulté le 08.06.2022.
MAT-FR-2202672 - 04/2024