- Wissen
- Quelle: Campus Sanofi
- 20.08.2024
Früherkennung

Typ-1-Diabetes früh diagnostizieren: Die Chancen gründlicher Vorbereitung
Durch eine Frühidentifikation von Typ-1-Diabetes (T1D) kann das Risiko von Akut-Komplikationen bei der klinischen Manifestation verringert werden. Hier erfahren Sie mehr über Früherkennung und wie sie dazu beitragen kann, Leben zu verändern und Gesundheitsrisiken zu minimieren.
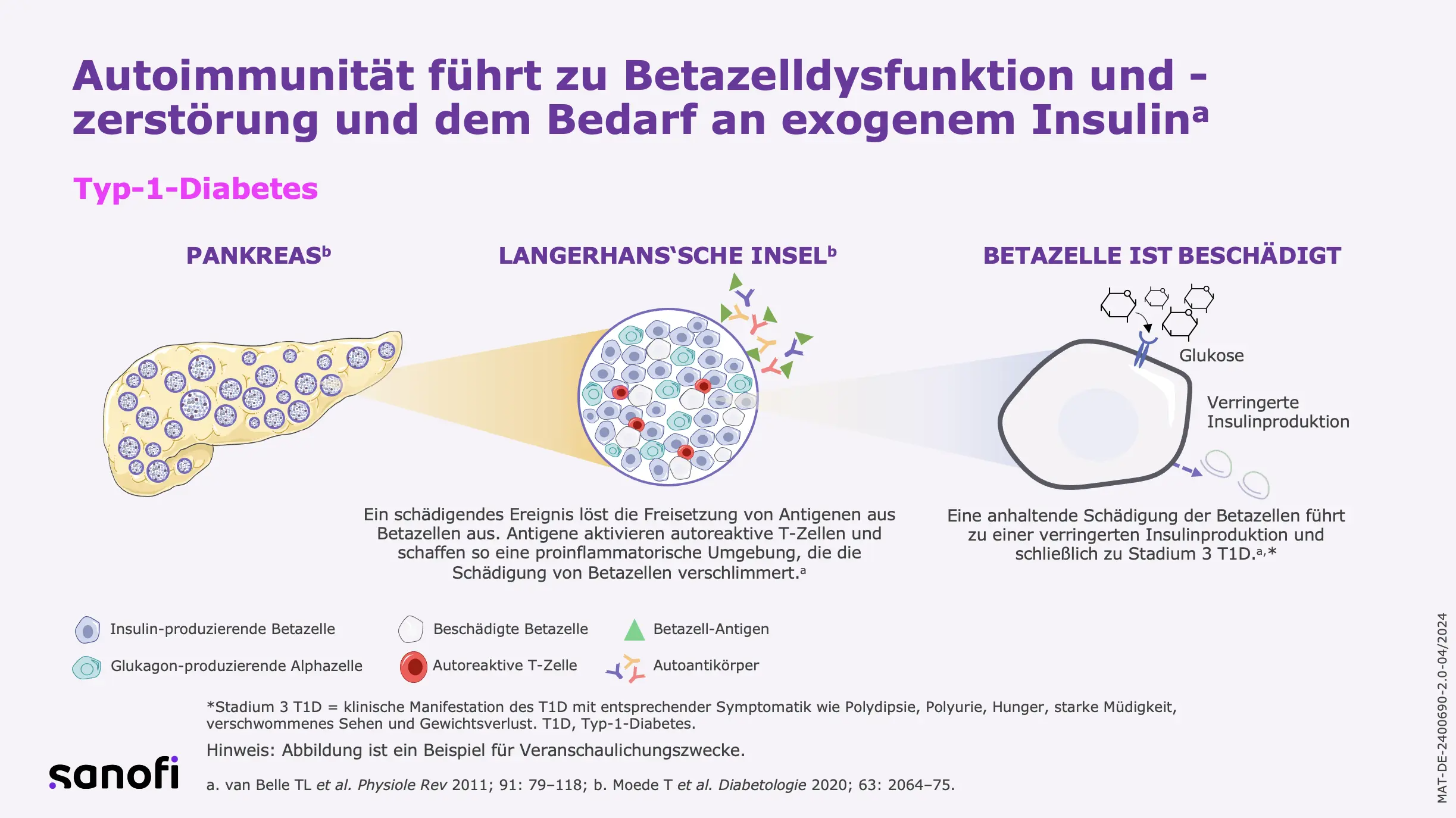
Typ-1-Diabetes (T1D) ist eine Autoimmunerkrankung, bei der autoreaktive T-Zellen nach und nach die insulinproduzierenden Zellen der Bauchspeicheldrüse zerstören. Das führt erst langsam, dann kurz vor der klinischen Manifestation zu einer immer weniger Insulin produzierenden Bauchspeicheldrüse.1
.png)
.png)
.png)
.png)
.png)
.png)
.png)
.png)

.png)

.png)
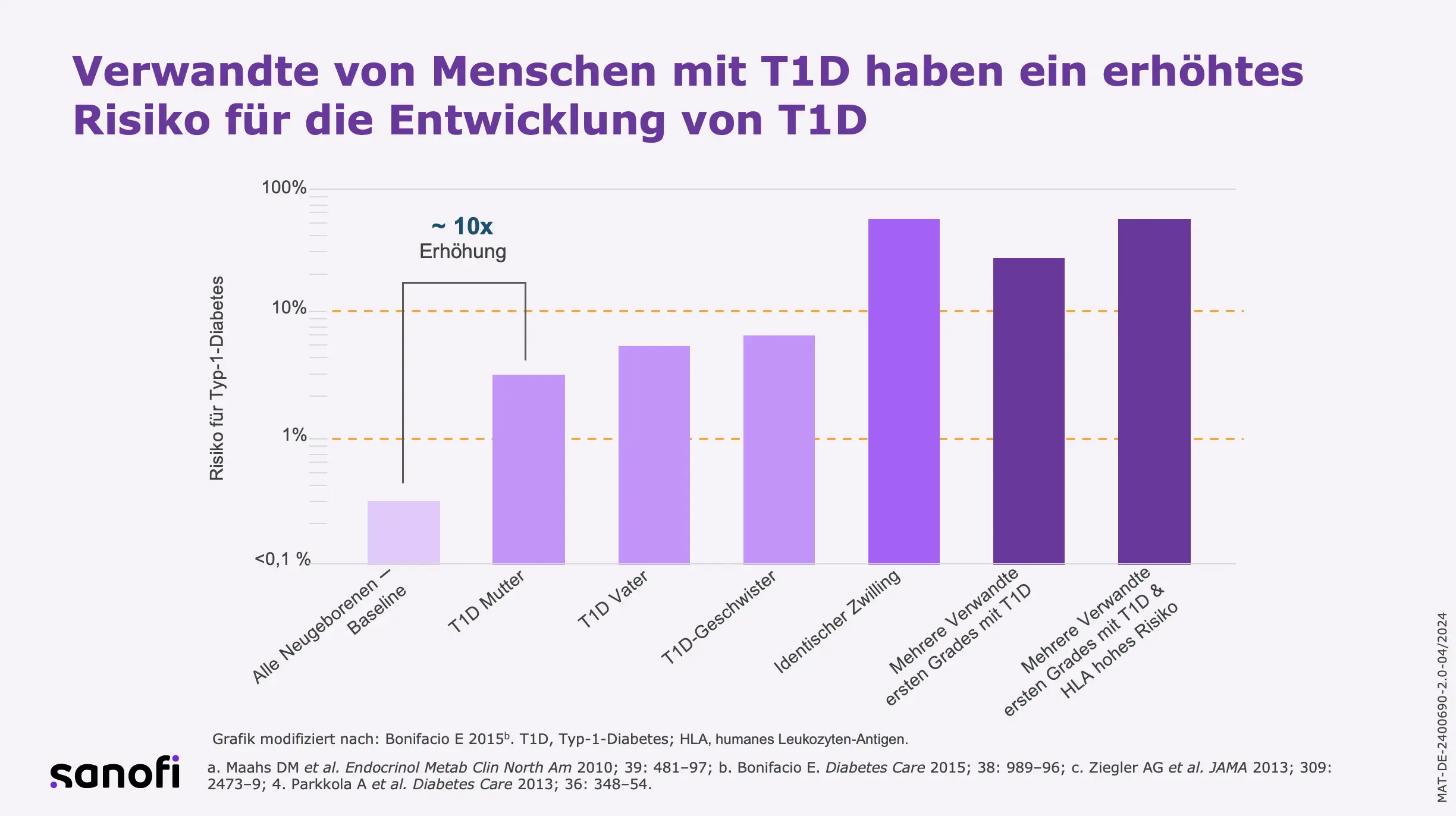
~ 85 % der T1D-Fälle treten bei Personen ohne Familienanamnese auf1
Die genetische Komponente des
Typ-1-Diabetes
- Gene des humanen Leukozyten-Antigens (HLA), die für die MHC-Klasse-II-Proteine kodieren, sind für ~ 50 % des genetischen T1D-Risikos verantwortlich; das größte Risiko tritt beim heterozygoten DR3/DR4-Genotyp auf1,2,3
- Betroffene mit familiärem vs. sporadischem T1D weisen vergleichbare Autoantikörperprofile auf, was auf ähnliche immunologische Krankheitsmechanismen hindeutet5; allerdings war bei langsamer Progression das Auftreten des Insulinom-assoziierten Antigen-2-Autoantikörper (IA-2A) verspätet6
- Groß angelegte Populationsstudien haben keinen signifikanten Unterschied in der zugrunde liegenden Pathophysiologie zwischen familiärem vs. sporadischem T1D gezeigt.3,4,5,6
- Mehrere T1D-Anfälligkeitsallele des Nicht-HLA-Typs, die alle in die Regulation der Immunantwort involviert sind, beeinflussen das rasche vs. langsame Fortschreiten der Krankheit: IL2, CD25, IL10, IFIH1, INSVNTR, IL18RAP und PTPN226
- Neben der Genetik werden Umweltfaktoren als zur Pathogenese von T1D beitragend angesehen, u. a. mütterliche und intrauterine Umgebung, Art der Entbindung, Viren, Mikrobiom, Antibiotika und Nahrungsmittel/Ernährung1
HLA, humanes Leukozyten-Antigen; MHC, Major Histocompatibility Complex, Haupt-Histokompatibilitäts-Komplex; T1D, Typ-1-Diabetes.
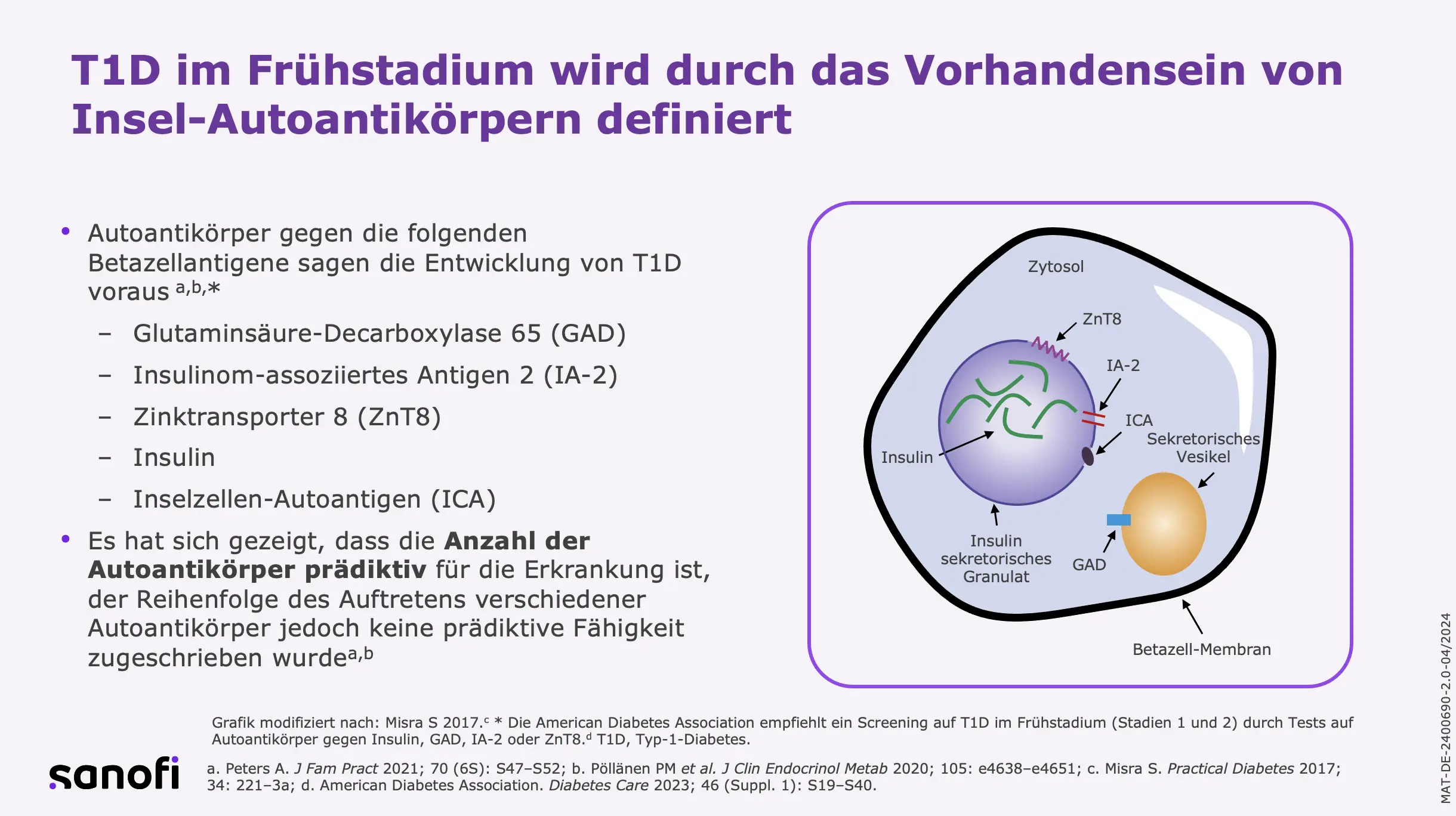


Inselautoantikörper – Diagnostische Marker zur Vorhersage des Typ-1-Diabetes
Bisher wird die T1D-Diagnose anhand der Symptome und dem Nachweis von Hyperglykämie bei der klinischen Manifestation gestellt. Allerdings treten erste Autoantikörper bereits im Säuglingsalter, mit einem Höhepunkt in den ersten beiden Lebensjahren, auf. Sie sind von prognostischer Bedeutung für die Entwicklung einer klinischen Manifestation des T1D.8 Durch die Bestimmung von Immunmarkern im Blut (Inselautoantikörper) kann T1D bereits in frühen, präklinischen Stadien sicher diagnostiziert werden, in denen noch keine klinischen Anzeichen der Erkrankung erkennbar sind.9 Inselautoantikörper treten bereits im Säuglingsalter auf, meist zwischen 6 Monaten und 3 Jahren, mit einem Höhepunkt um das 1. Lebensjahr.3 Der Nachweis von Autoantikörpern im Blut ist derzeit der wichtigste Marker für den Autoimmunprozess.
Progression des Typ-1-Diabetes – Frühzeitige Diagnose für eine bessere Behandlung
Zusammenfassende Studiendaten bestätigten, dass die Mehrheit der Kinder mit genetisch bedingtem Risiko und einem positiven Test auf Inselautoantikörper innerhalb von 15 Jahren T1D entwickelten.9 Die Progression zu Typ-1-Diabetes 10 Jahre nach Auftreten der Inselautoantikörper betrug bei Kindern
- mit mehreren Insel-Autoantikörpern 69,7 %
- mit einem einzelnen Insel-Autoantikörper 14,5 %
- mit keinen Inselautoantikörper im Alter von 15 Jahren 0,4 %.10
Durch einen Früherkennungstest auf Inselautoantikörper im Kindesalter könnten zukünftig Kinder mit einem präsymptomatischen Frühstadium des T1D unabhängig von ihrem genetischen Risiko diagnostiziert werden.11 Ob eine Antikörpertestung zur Vorhersage des T1D als allgemeine Routineuntersuchung bei allen Kindern der deutschen Bevölkerung eingeführt werden sollte, wird gegenwärtig diskutiert.12 Eine neue Definition des präklinischen Stadiums ist in jedem Fall dringend erforderlich. Tatsächlich haben 80 % der Kinder, die in der Kindheit T1D entwickeln, vor dem 5. Lebensjahr mehrere Inselautoantikörper.13
Durch eine frühzeitige Diagnose können alle Betroffenen im präsymptomatischen Frühstadium der Erkrankung geschult und präsymptomatisch behandelt werden, sofern notwendig. Gleichzeitig können die Auswirkungen der Früherkennung auf die klinische Manifestation (z. B. Häufigkeit von Komplikationen während der Manifestation) untersucht werden.1,11 Durch die Früherkennung des prädiabetischen Stadiums gewinnen Betroffene, Angehörige und auch der Behandelnde wertvolle Zeit, um sich auf die chronische Erkrankung vorzubereiten.12
Auch auf psychologischer Ebene sollten die Vor- und Nachteile der Früherkennung nicht unterschätzt werden. Einerseits ermöglicht die Früherkennung den Eltern eine intensive Auseinandersetzung mit der Erkrankung und den damit einhergehenden Veränderungen. Andererseits stellt die Ungewissheit über den Zeitpunkt der klinischen Manifestation eine zusätzliche, manchmal jahrelange Belastung dar und kann zu posttraumatischen Belastungsstörungen führen.15
Die Fr1da-Studie
Frühe Symptome des Typ-1-Diabetes können leicht übersehen werden. Umso wichtiger ist die Früherkennung bereits im Kindes- und Jugendalter, die sich die Fr1da-Studie auf die Fahne geschrieben hat. Welche Rolle Autoantikörper spielen und welche Erkenntnisse aus der Studie bereits gewonnen wurden, erfahren Sie hier.
Prof. Dr. med. Anette-Gabriele Ziegler; Direktorin des Instituts für Diabetesforschung am Helmholtz Munich mit Familie im Studienzentrum © Helmholtz Munich - Andreas Pfohl, NOZY Films GmbH
Unter dem Namen „Fr1da – Typ-1-Diabetes: Früh erkennen – Früh gut behandeln“ läuft in Bayern die weltweit erste bevölkerungsweite Studie zur Früherkennung von Typ-1-Diabetes (T1D) bei Kindern.8 Seit dem Start im Jahr 2015 wurden über ein Netzwerk von Kinder- und Jugendarztpraxen über 169.446 Kinder (Stand: Dezember 2022) im Alter von 2–10 Jahren auf das Vorliegen von Inselautoantikörpern untersucht.1
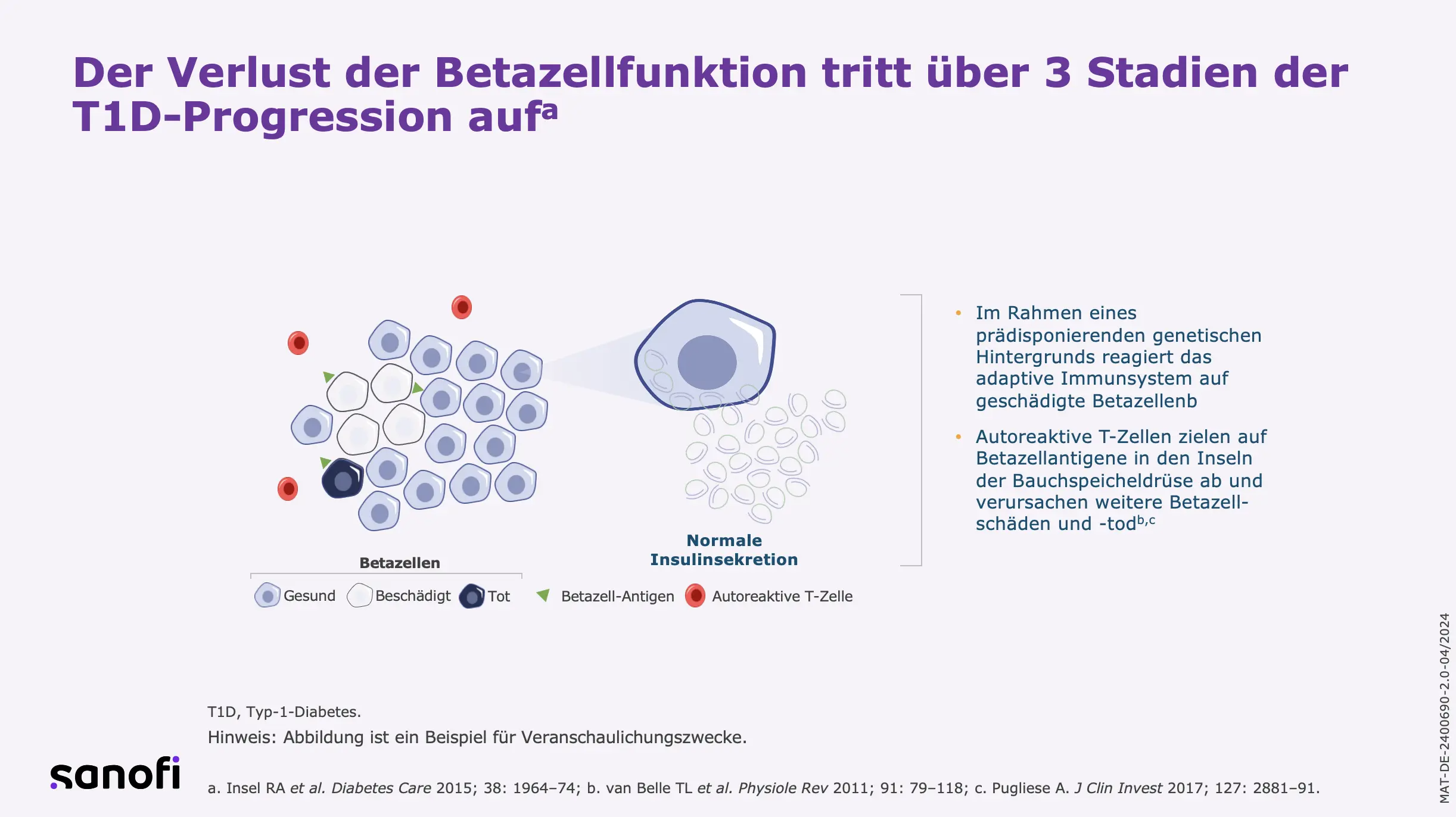
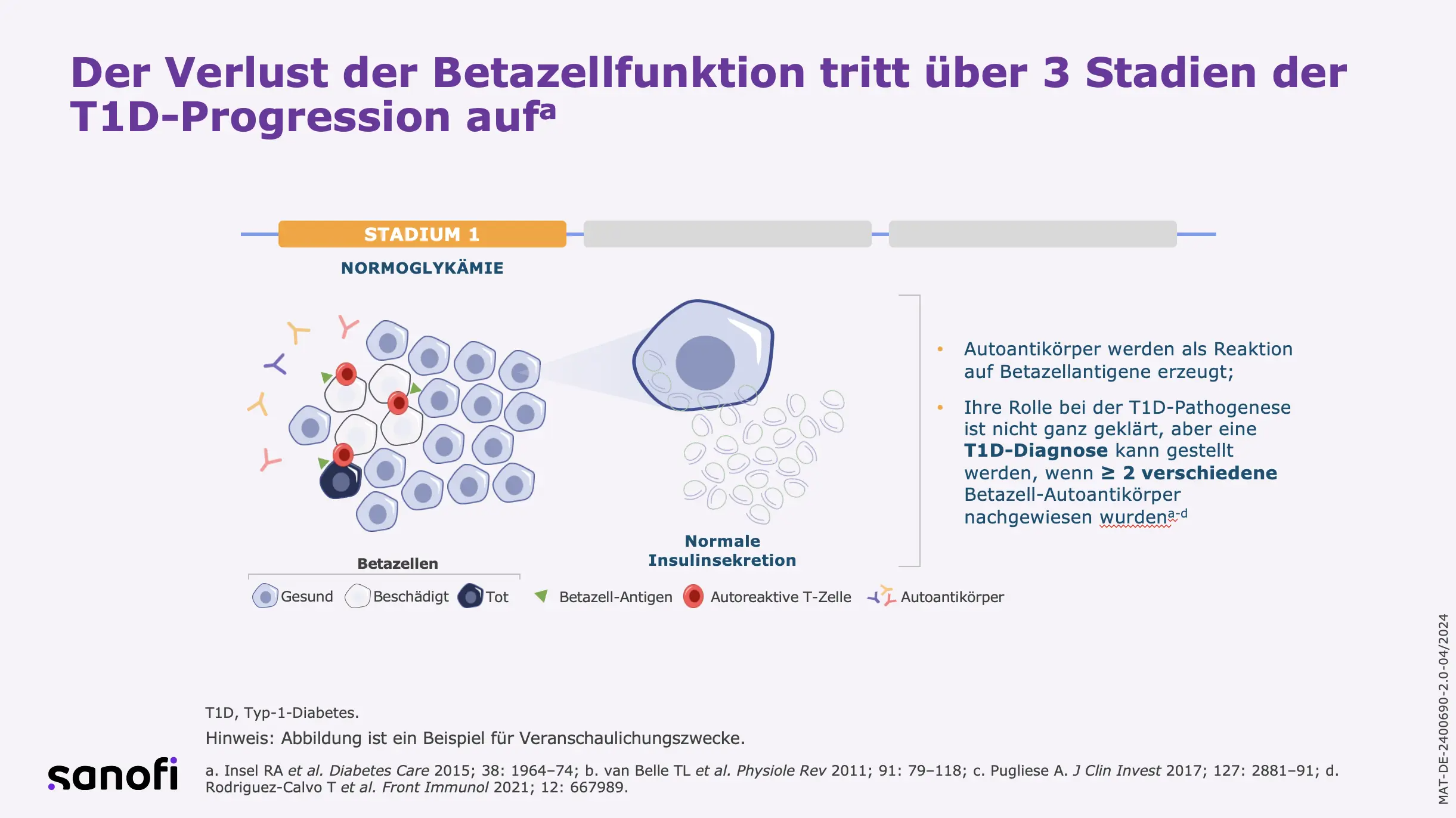
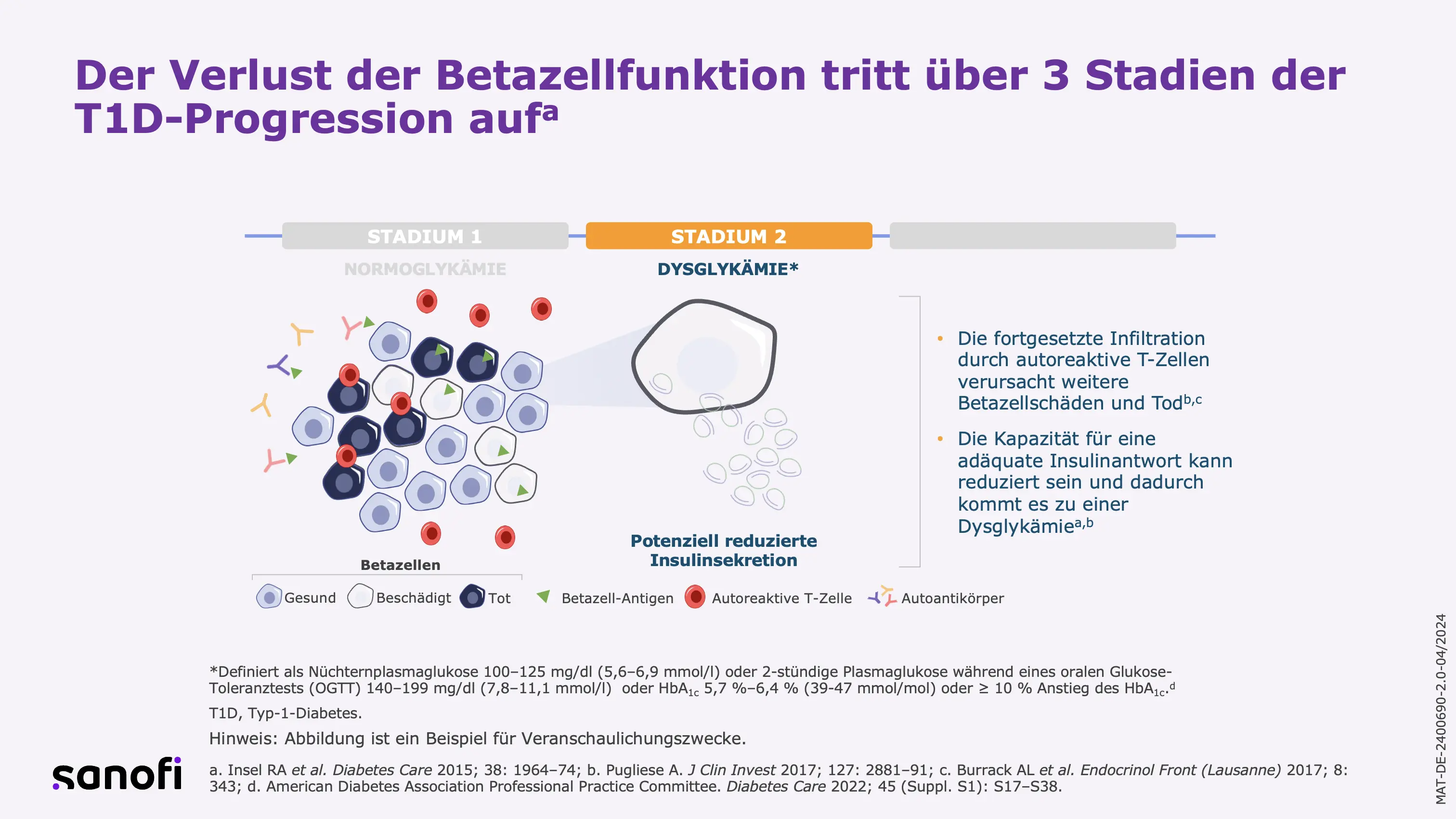
T1D äußert sich in 3 Stadien: Von den präsymptomatischen Stadien 1 und 2 zur klinischen Manifestation (Stadium 3).2,17 Nahezu 100 % der Kinder mit einer Diagnose des Stadium 1 oder 2 (Nachweis von ≥ 2 Autoantikörpern) entwickeln einen klinischen T1D.1 Anhand der ersten Ergebnisse der Autoantikörper-Untersuchungen in der Fr1da-Studie (Untersuchungsjahre 2015–2019) bei 90.632 Kindern (2–5 Jahre) und deren Beobachtung im weiteren Verlauf, konnten einige Erkenntnisse zur Progression des T1D gesammelt werden:18
- Bei 0,31 % der Kinder wurde ein präsymptomatischer T1D mit 2 oder mehr Autoantikörpern detektiert (95 %-Konfidenzintervall (KI): 0,27–0,35).18
- Das kumulierte Risiko einen manifestierten T1D (Stadium 3) zu entwickeln lag bei 24,9 % innerhalb von 3 Jahren (n = 54 von 280; 95 %-KI: 18,5–30,7).18
- Kinder mit 4 Autoantikörpern hatten ein signifikant höheres Risiko innerhalb von 3 Jahren einen manifesten T1D zu entwickelnd im Vergleich zu Kindern mit 2 Autoantikörpern (Hazard Ratio (HR) 1,85; 95 %-KI: 1,03–3,32; p = 0,04).18
- Faktoren, die mit der Progression der Erkrankung von Stadium 1 (≥ 2 Autoantikörper + Normoglykämie) zu Stadium 2 (≥ 2 Autoantikörper + Dysglykämie) signifikant assoziiert sind: Adipositas, das Vorliegen des Autoantikörpers IA-2A, HbA1c 5,7 % und schlechtere Glukosetoleranz (gemessen anhand der Fläche unter der Kurve (AUC) beim oralen Glukosetoleranztests (OGTT) sowie die einzelnen OGTT-Werte nach 1 h).18
- Nicht signifikant mit der Progression der Erkrankung von Stadium 1 zu Stadium 2 assoziiert waren Faktoren wie Geschlecht, Alter, Body-Mass-Index (BMI), T1D in der Verwandtschaft oder genetische Risikofaktoren.18
In einer späteren Analyse der Fr1da-Studie aus 2023 zeigte sich, dass bei klinischer Manifestation (Stadium 3) nur 2,5 % der Kinder aus der Fr1da-Studie von einer diabetischen Ketoazidose betroffen waren.16 Die Ketoazidoserate liegt bei nicht gescreenten Kindern in Deutschland deutlich höher, wie es u. a. den Daten des DPV-Registers entnommen werden kann.16
Abb.: Auftreten diabetischer Ketoazidosen (in %) bei Patientinnen und Patienten ohne T1D-Früherkennung (DPV-Daten)19 vs. Rate aus der Fr1da-Studie (T1D-Früherkennungsstudie)16
DKA: diabetische Ketoazidose; DPV: Diabetes-Patienten-Verlaufsdokumentation; T1D: Typ-1-Diabetes.
Kinder, die aufgrund der Teilnahme an der Fr1da-Studie eine T1D-Diagnose im Frühstadium erhielten, wiesen bei Manifestation der Erkrankung geringere HbA1c-Werte, niedrigere Nüchternblutzuckerwerte und höhere Nüchtern-C-Peptid-Werte auf, verglichen mit Kindern ohne Frühstadium-Diagnose.16
| Im Symposium „Wer früh hilft, hilft doppelt – Typ-1-Diabetes mal anders gedacht“ von Sanofi beim Diabetes Kongress 2024 der Deutschen Diabetes Gesellschaft (DDG), wurden u. a. die Ergebnisse der Fr1da-Studie tiefer von Prof. Dr. med. Peter Achenbach (Institut für Diabetesforschung, Helmholtz Munich) beleuchtet. Hier finden Sie die Aufzeichnung. |
In der Fr1da-Studie werden im ersten Schritt Autoantikörper gegen Glutamat-Decarboxylase 65 (GADA), Insulinoma-assoziiertes Antigen 2 (IA-2A) und Zinktransporter 8 (ZnT8A) kombiniert in einer Kapillarblutprobe mit einem Enzyme-Linked Immunosorbent Assay (ELISA)-Verfahren gemessen. Wenn dieser kombinierte Test positiv ist, wird das verbleibende Serum verwendet, um GADA, IA-2A, ZnT8A und Insulin-Autoantikörper (IAA) mittels Referenz-Radioimmunassays (RIA) zu messen. Wenn mindestens 2 positive Inselautoantikörper durch die Referenz-RIA-Methode nachgewiesen werden, wird eine Bestätigungsprobe aus venösem Blut entnommen. Die Diagnose eines Typ-1-Diabetes im Frühstadium (Stadium 1 oder 2) wird erst gestellt, wenn der Bestätigungstest ebenfalls positiv (d. h. Nachweis von ≥ 2 Autoantikörpern mit der RIA-Methode) ist.13
Hier finden Sie den Ablauf der T1D-Frühidentifikation in der Fr1da-Studie im Detail.
Die Fr1da-Studie für Verwandte deutschlandweit
- Weltweit erstes bevölkerungsweite Vorsorgeprogramm für das Frühstadium von T1D.8
- Für Kinder/Jugendliche/Erwachsene mit Verwandten 1. und 2. Grades mit T1D
1-21 Jahre: Fr1da-Studie für Verwandte deutschlandweit - Voraussetzungen:
- Die Person ist zwischen 1 und 21 Jahre alt und lebt in Deutschland.
- Ein Elternteil, Kind, (Halb-)Schwester, (Halb-)Bruder, Tante, Onkel, Cousin, Cousine, Nichte oder Neffe hat Typ-1-Diabetes.
- Bei der Person selbst wurde bislang kein Typ-1-Diabetes diagnostiziert.
- Bei 0,3 % der Kinder wurde ein asymptomatischer T1D identifiziert.8
- Innerhalb von ca. 2,5 Jahren entwickelte bereits ein Viertel der Kinder mit Stadium 1 oder 2 einen klinisch manifesten T1D (Stadium 3).8
- Bei klinischer Manifestation hatten nur 2 von 62 Kindern aus Fr1da (3,2 %) eine diabetische Ketoazidose; die Ketoazidoserate bei nicht gescreenten Kindern liegt bei 35,2%.8
- Bei Kindern mit 4 Autoantikörpern manifestiert sich die Erkrankung schneller.8
- Die Progressionsrate ist unabhängig von der genetischen Prädisposition.14
- Weitere Informationen erhältlich unter: https://www.typ1diabetes-frueherkennung.de/teilnahme-fr1da-studie/teilnahme-fr1da-studie-fuer-verwandte-deutschlandweit.html

Diabetische Ketoazidosen erkennen & vermeiden

Die Stadien von Typ-1-Diabetes

Monitoring bei präsymptomatischem Typ-1-Diabetes

Neue Erkenntnisse bei Typ-1-Diabetes

Typ-1-Diabetes neu denken

Diabetische Ketoazidosen erkennen & vermeiden

Die Stadien von Typ-1-Diabetes

Monitoring bei präsymptomatischem Typ-1-Diabetes

Neue Erkenntnisse bei Typ-1-Diabetes

Typ-1-Diabetes neu denken
Früherkennungsstudien Fr1da und Fr1da für Verwandte in Deutschland
Ihre Patient*innen leben in Bayern, Niedersachsen, Hamburg, Sachsen, Hessen oder Rheinland-Pfalz?
Alle Kinder im Alter von 2 bis 10 Jahren können hier an der Fr1da-Studie teilnehmen und sich auf Inselautoantikörper testen lassen.
Erfahren Sie mehr zum Früherkennungstest in der Fr1da-Studie!
Sie haben Patient*innen mit T1D mit Verwandten 1. oder 2. Grades, welche zwischen 1 und 21 Jahre alt sind und in Deutschland leben?
Deutschlandweit können diese sich auf Inselautoantikörper testen lassen.
Erfahren Sie mehr zum Früherkennungstest in der Fr1da-Studie für Verwandte!
-
DDG 2023. S3-Leitlinie: Diagnostik, Therapie und Verlaufskontrolle des Diabetes mellitus im Kindes- und Jugendalter, AWMF-Registernummer: 057-016. Erhältlich unter: https://register.awmf.org/assets/guidelines/057-016l_S3_Diagnostik-Therapie-Verlaufskontrolle-Diabetes-mellitus-Kinder-Jugendliche_2023-11.pdf (zuletzt abgerufen am 01.10.2024)
-
Marcus BA et al. Diabetologe 2020; 16: 654-61
-
Ziegler AG et al. JAMA 2013; 309: 2473-9
-
Ziegler AG et al. Diabetes Technol Ther 2016; 18: 687-93
-
Lipponen K et al. Diabetes 2010; 59: 3253–6
-
Parkkola A et al. Diabetes Care 2013; 36: 348–54
-
Achenbach P et al. Diabetologia 2013; 56: 1615–22
-
Marcus BA et al. Type 1 diabetes: Early diagnosis and preventive approaches: Update 2020.
-
Ziegler AG et al. Jama. 2013.
-
al. ZAe. 3 Screen ELISA for High-Throughput Detection of Beta Cell Autoantibodies in Capillary Blood. Diabetes Technology & Therapeutics. 2016.
-
Peter Achenbach, Typ-1-Diabetes im präsymptomatischen Frühstadium bei Kindern diagnostizieren: Erfahrungen aus der Fr1da-Studie, in: Spitzenforschung in der Diabetologie. Innovationen und Auszeichnungen 2021, hrsg. von der ALPHA Informations-GmbH, Lampertheim 2021, S. 12 – 20. Erhältlich unter: https://www.typ1diabetes-frueherkennung.de/fileadmin/FRIEDA/PDF/Presseseite/096-637_Beitrag_Achenbach.pdf (zuletzt abgerufen am 01.10.2024)
-
Becker N. FR1da-Studie: Testlauf für ein nationales Screening. Dtsch Arztebl 2014; 111: 12. Abrufbar unter: https://www.aerzteblatt.de/archiv/162946/FR1da-Studie-Testlauf-fuer-ein-nationales-Screening (zuletzt abgerufen am 01.10.2024)
-
Raab J et al. BMJ Open 2016; 6: e011144
-
Weiss A et al. Diabetologia 2022; 65: 2121-31
-
Houben J et al. Pediatr Diabetes 2022; 23: 1707-16
-
Hummel S et al. Diabetologia 2023; 66: 1633-42
-
American Diabetes Association Professional Practice Committee. Diabetes Care 2022; 45 (Suppl. 1): S17-S38
-
Ziegler AG et al. JAMA 2020; 323: 339-51
-
Baechle C et al. Diabetes Res Clin Pract 2023; 197: 110559Ziegler AG et al. Jama. 2020;323(4):339-351
MAT-DE-2401628-1.0-09/2024