- Articolo
- Fonte: Campus Sanofi
- 23 apr 2026
BPCO vs asma: scopri le differenze
I segni e i sintomi sovrapponibili di BPCO e asma possono rendere difficile distinguere tra queste due condizioni.2 Alcuni gruppi di pazienti rappresentano una sfida per una diagnosi accurata di BPCO a causa di caratteristiche cliniche confondenti.2
BPCO e asma sono patologie ostruttive polmonari con caratteristiche epidemiologiche e fisiopatologiche distinte.3 Inoltre, queste due condizioni presentano differenti strategie di gestione e diversi obiettivi terapeutici raccomandati dalle linee guida.4 Pertanto, è necessario distinguere chiaramente le due condizioni per una diagnosi accurata e una gestione ottimale.4
La BPCO è una malattia cronica respiratoria, tipicamente associata al fumo e diagnosticata in soggetti di mezza età e anziani (>40 anni) ed è caratterizzata da un’ostruzione progressiva e irreversibile delle vie aeree.3
Al contrario, l’asma è caratterizzata da iperresponsività bronchiale, che porta ad una ostruzione intermittente e solitamente reversibile delle vie respiratorie. Tipicamente, l’asma si manifesta durante l’infanzia, sebbene possa essere diagnosticata anche in età adulta.3
Distinzione tra BPCO e asma4
|
BPCO |
Asma | |
| Ostruzione delle vie aeree |
Non completamente reversibile / irreversibile |
Completamente o quasi completamente reversibile |
| Età di insorgenza |
Più avanzata |
Più giovane |
| Storia di atopia |
– |
Presente |
| Storia di fumo (pack-years) |
Maggiore |
Minore |
| Decorso della malattia |
Progressivo |
Episodi ricorrenti con frequenza e intensità variabili |
| Pattern dei sintomi |
Spesso costante e progressivo |
Spesso intermittente, talvolta costante. Aumenta con esposizione ad allergeni/ esercizio fisico o esposizione ad aria fredda |
| Variabilità dei sintomi |
Minore |
Variazioni quotidiane frequenti |
| Sintomi tipici |
Dispnea, tosse (con abbondante produzione di muco nella bronchite cronica) |
Sibili, tosse, senso di costrizione toracica/ dispnea |
| Tosse |
Produttiva |
Secca |
| Radiografia toracica |
Segni di iperinflazione, ispessimento bronchiale e aumento dei segni basali |
Di norma, nella norma |
| Liquido di lavaggio broncoalveolare/sputo | ||
| Livello di eosinofili |
Maggiore nell’asma rispetto alla BPCO | |
| Livello di neutrofili |
Minore nell’asma rispetto alla BPCO | |
Elaborazione grafica da testo, Ref. 4
Infiammazione di tipo 2 nella BPCO e nell’asma
Sia la BPCO che l’asma sono associate a infiammazione cronica delle vie respiratorie.5 Sebbene le cellule e i mediatori coinvolti nell’infiammazione differiscano tra le due patologie, alcuni pazienti con BPCO presentano un pattern infiammatorio (infiammazione di tipo 2) simile a quello dell’asma.5
Si ritiene che l'infiammazione di tipo 2 sia una caratteristica tipica dell'asma piuttosto che della BPCO.7 Tuttavia, gli studi hanno dimostrato che esiste un sottogruppo di pazienti con BPCO affetti da infiammazione di tipo 2 delle vie aeree, anche in assenza di asma concomitante.7
È importante sottolineare che l'infiammazione di tipo 2 è associata a un aumento del rischio di riacutizzazioni sia nell'asma che nella BPCO da moderata a grave.8

Clicca qui per leggere ulteriori informazioni sul ruolo dell'infiammazione di tipo 2 nelle riacutizzazioni della BPCO
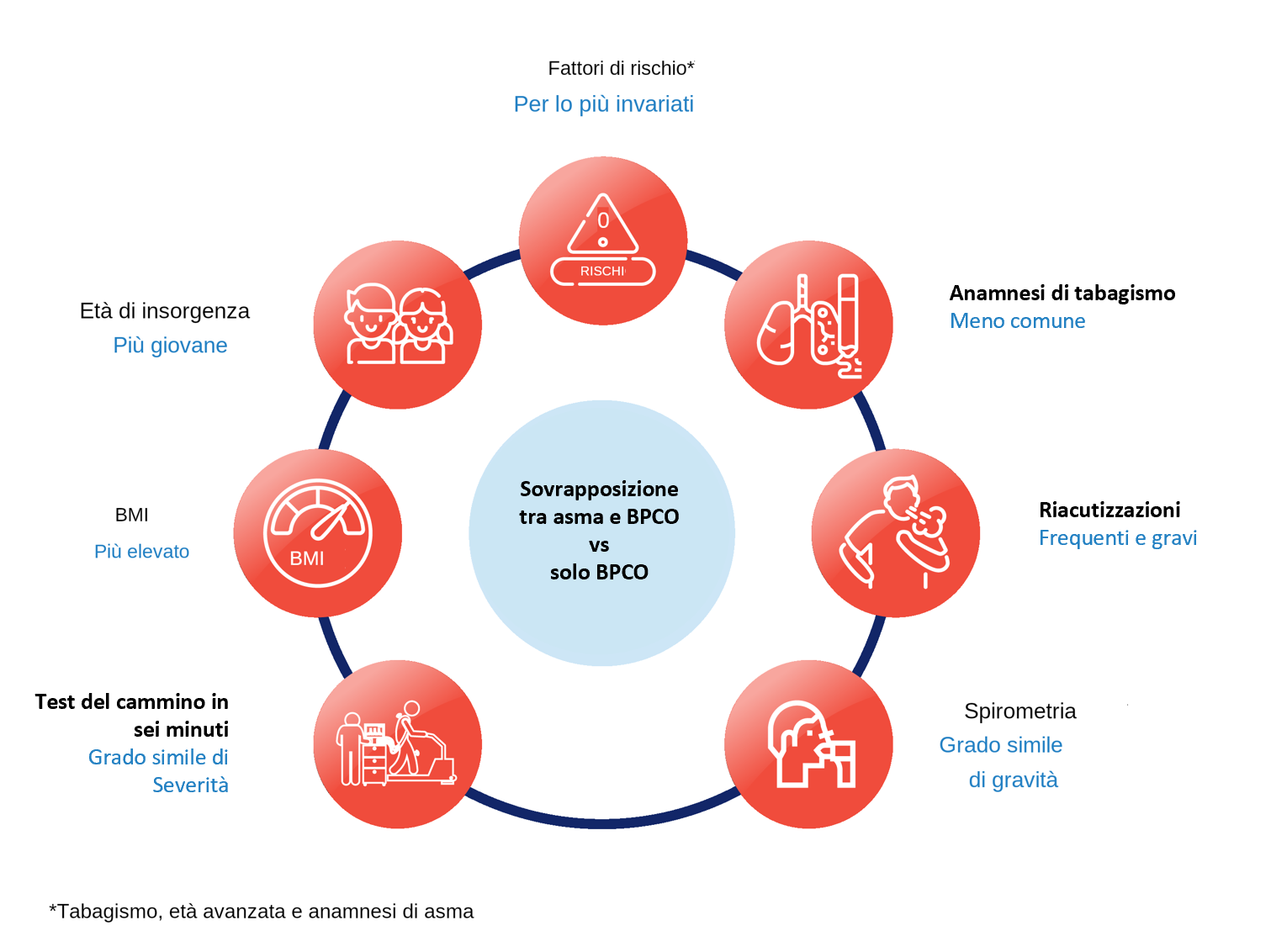
Sovrapposizione tra BPCO e asma
Il rapporto strategico 2025 della Global Initiative for Asthma (GINA) definisce I termini “overlap asma-BPCO” o “asma + BPCO” rappresentano semplici descrittori utilizzati per identificare i pazienti che presentano caratteristiche sia dell’asma sia della BPCO.1
Il rapporto 2026 della Global Initiative for Chronic Obstructive Lung Disease (GOLD) sottolinea che queste due condizioni sono distinte, pur riconoscendo che possono coesistere.5
Si stima che l’asma coesista in circa il 27% dei pazienti affetti da BPCO.3 In caso di diagnosi concomitante, il rapporto GOLD 2026 raccomanda di gestire la patologia seguendo le linee guida per l’asma.5
Risposta ai broncodilatatori: BPCO vs asma
Valori anomali del volume espiratorio forzato in un secondo (FEV1) e della capacità vitale forzata (FVC) sono indicativi di ostruzione al flusso aereo.4 La spirometria pre-broncodilatatore può essere utilizzata per una valutazione iniziale dell’ostruzione al flusso aereo nei pazienti sintomatici.5
La spirometria post-broncodilatatore è necessaria per la diagnosi e la valutazione della BPCO; un rapporto FEV1/FVC <0,7 è considerato diagnostico per la BPCO.5 La spirometria post-broncodilatatore può inoltre essere utile per distinguere tra la presentazione classica dell’asma e la BPCO. Nell’asma classica, l’ostruzione al flusso aereo è spesso completamente reversibile, mentre nella BPCO è irreversibile o solo parzialmente reversibile. Tuttavia, il grado di reversibilità può variare nel singolo paziente e la coesistenza di BPCO e asma può confondere la risposta al broncodilatatore. Pertanto, la spirometria post-broncodilatatore non dovrebbe essere considerata come unico criterio per differenziare la BPCO dall’asma.4
Linee guida per il trattamento della BPCO e dell'asma
Gestione della BPCO5
Gli obiettivi del trattamento delle riacutizzazioni di BPCO sono la riduzione dei sintomi e del rischio futuro di ulteriori riacutizzazioni.5 Il report GOLD 2026 propone un approccio personalizzato alla gestione della BPCO, basato sulla gravità dei sintomi e sul rischio di riacutizzazione.5
Il trattamento può essere intensificato o ridotto in base ai sintomi predominanti (caratteristiche trattabili) quali dispnea e limitazione dell’esercizio fisico, nonché al persistere delle riacutizzazioni durante la terapia di mantenimento.5
Trattamento farmacologico iniziale della BPCO5
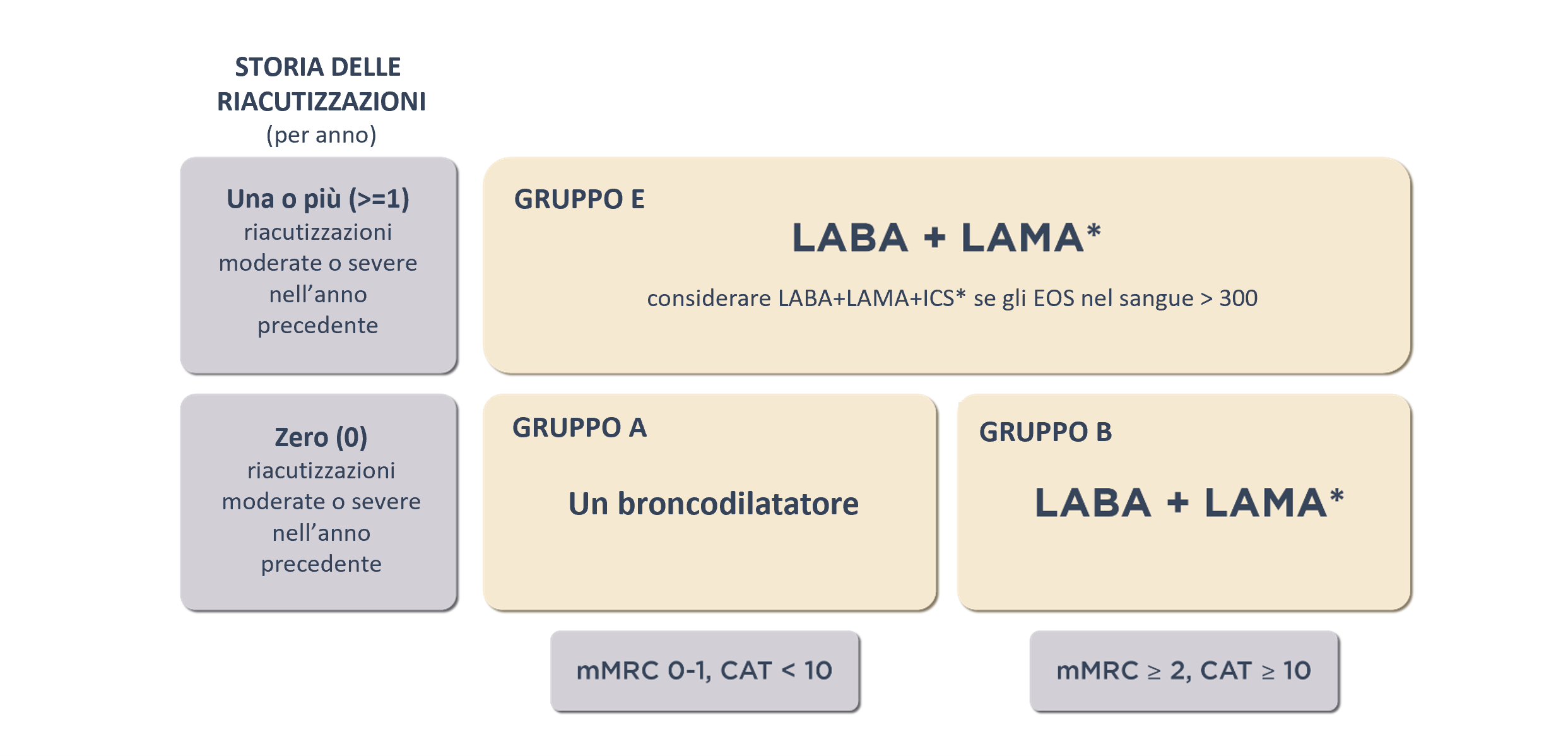
* La terapia con un unico inalatore può essere più conveniente ed efficace rispetto all’uso di più inalatori; l’impiego di un solo inalatore migliora l’aderenza al trattamento.
Le riacutizzazioni si riferiscono al numero di episodi all’anno; eos: conta degli eosinofili nel sangue in cellule per microlitro; mMRC: questionario sulla dispnea del Medical Research Council modificato; CAATTM: Chronic Airways Assessment TestTM.
Gestione dell’asma1
L’obiettivo della gestione dell’asma secondo GINA è ottenere i migliori risultati possibili a lungo termine per il singolo paziente, includendo il controllo dei sintomi e la riduzione al minimo del rischio di mortalità correlata all’asma, delle riacutizzazioni, della limitazione persistente del flusso aereo e degli effetti indesiderati del trattamento.
Gestione personalizzata per adulti e adolescenti finalizzata al controllo dei sintomi e alla minimizzazione del rischio futuro1
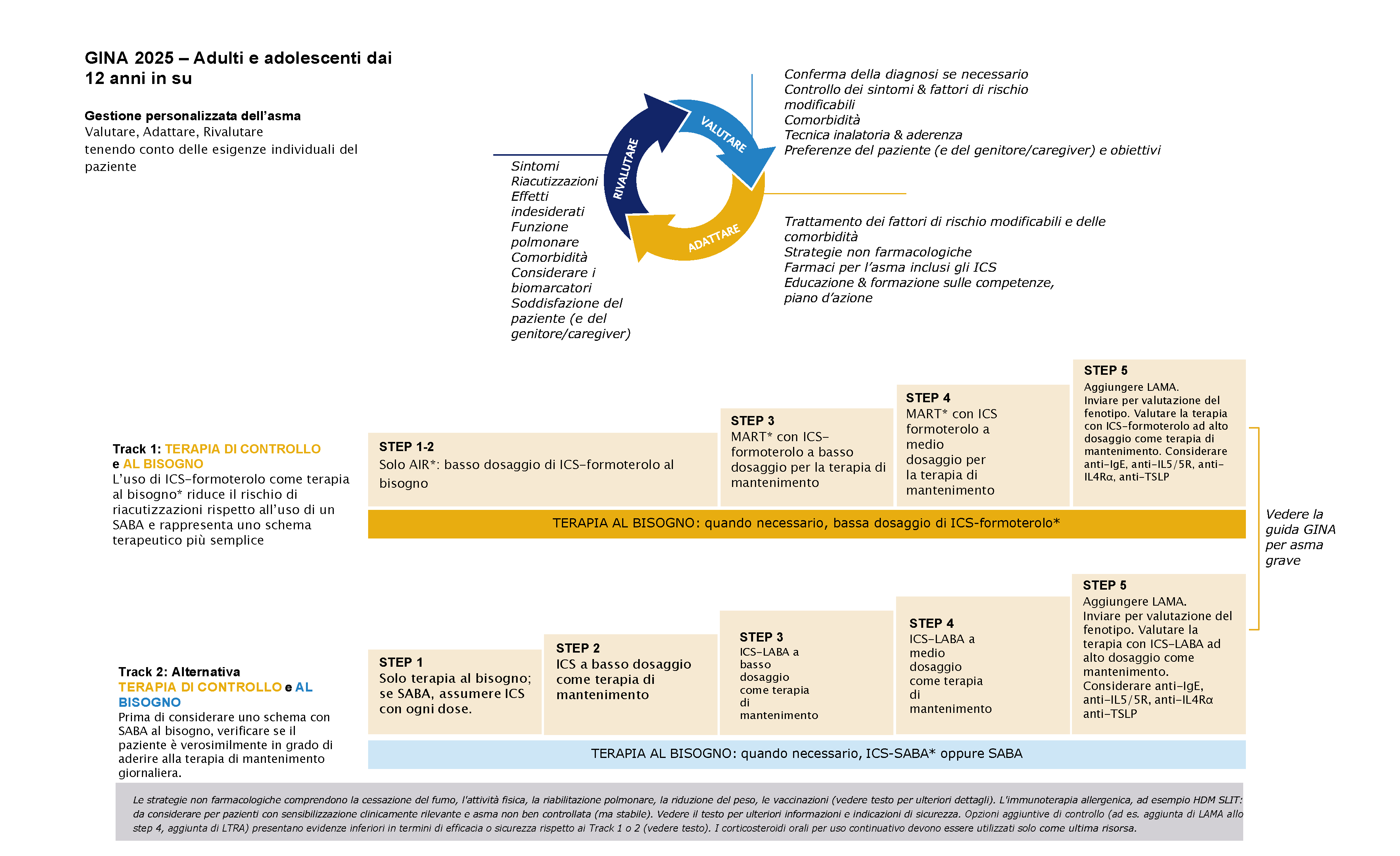
© Global Initiative for Asthma, www.ginasthma.org
AIR: antagonista infiammatorio; Ig: immunoglobulina; ICS: corticosteroidi inalatori; HDM: acari della polvere domestica; IL: interleuchina; LABA: beta agonista a lunga durata d'azione; LAMA: antagonista muscarinico a lunga durata d'azione; LTRA: antagonista dei recettori dei leucotrieni; MART: terapia di mantenimento e al bisogno con ICS-formoterolo; OCS: corticosteroide orale; SABA: beta agonista a breve durata d'azione; SLIT: immunoterapia sublinguale; agonist; TSLP: linfopoietina stromale timica. †Se si prescrive LTRA, informare il paziente/caregiver del rischio di eventi avversi neuropsichiatrici.
Bibliografia
- Global strategy for Asthma Management and Prevention (2025 update). (Accessed May 27, 2025, at https://ginasthma.org/2025-gina-strategy-report/.)
- Silva GE, Sherrill DL, Guerra S, Barbee RA. Asthma as a risk factor for COPD in a longitudinal study. Chest. 2004 Jul;126(1):59-65.
- Alshabanat A, Zafari Z, Albanyan O, Dairi M, FitzGerald JM. Asthma and COPD Overlap Syndrome (ACOS): A Systematic Review and Meta Analysis. PLoS One. 2015;10(9):e0136065.
- Yawn BP. Differential assessment and management of asthma vs chronic obstructive pulmonary disease. Medscape J Med 2009;11:20.
- ©[2025-2026] Global Strategy for Diagnosis, Management and Prevention of COPD. All rights reserved. Use is by express license from the owner. Ultimo accesso: gennaio 2026. 2026 GOLD Report and Pocket Guide - Global Initiative for Chronic Obstructive Lung Disease - GOLD
- Higham A, Beech A, Wolosianka S, Jackson N, Long G, Kolsum U, et al. Type 2 inflammation in eosinophilic chronic obstructive pulmonary disease. Allergy. 2021;76(6):1861-64.
- Singh D, Kolsum U, Brightling CE, Locantore N, Agusti A, Tal-Singer R; ECLIPSE investigators. Eosinophilic inflammation in COPD: prevalence and clinical characteristics. Eur Respir J. 2014;44(6):1697-700.
- Yun JH, Lamb A, Chase R, Singh D, Parker MM, Saferali A, et al; COPDGene and ECLIPSE Investigators. Blood eosinophil count thresholds and exacerbations in patients with chronic obstructive pulmonary disease. J Allergy Clin Immunol. 2018;141(6):2037-2047.e10.
Codice deposito aziendale MAT-IT-2600597