- Article
- Source : Campus Sanofi
- 17 avr. 2026
Polypose naso-sinusienne : quand adresser votre patient au pneumologue ?

La PNS est fréquemment associée à d'autres pathologies
Chez les patients avec une PNS*, il est fréquent de retrouver d'autres pathologies associées :1
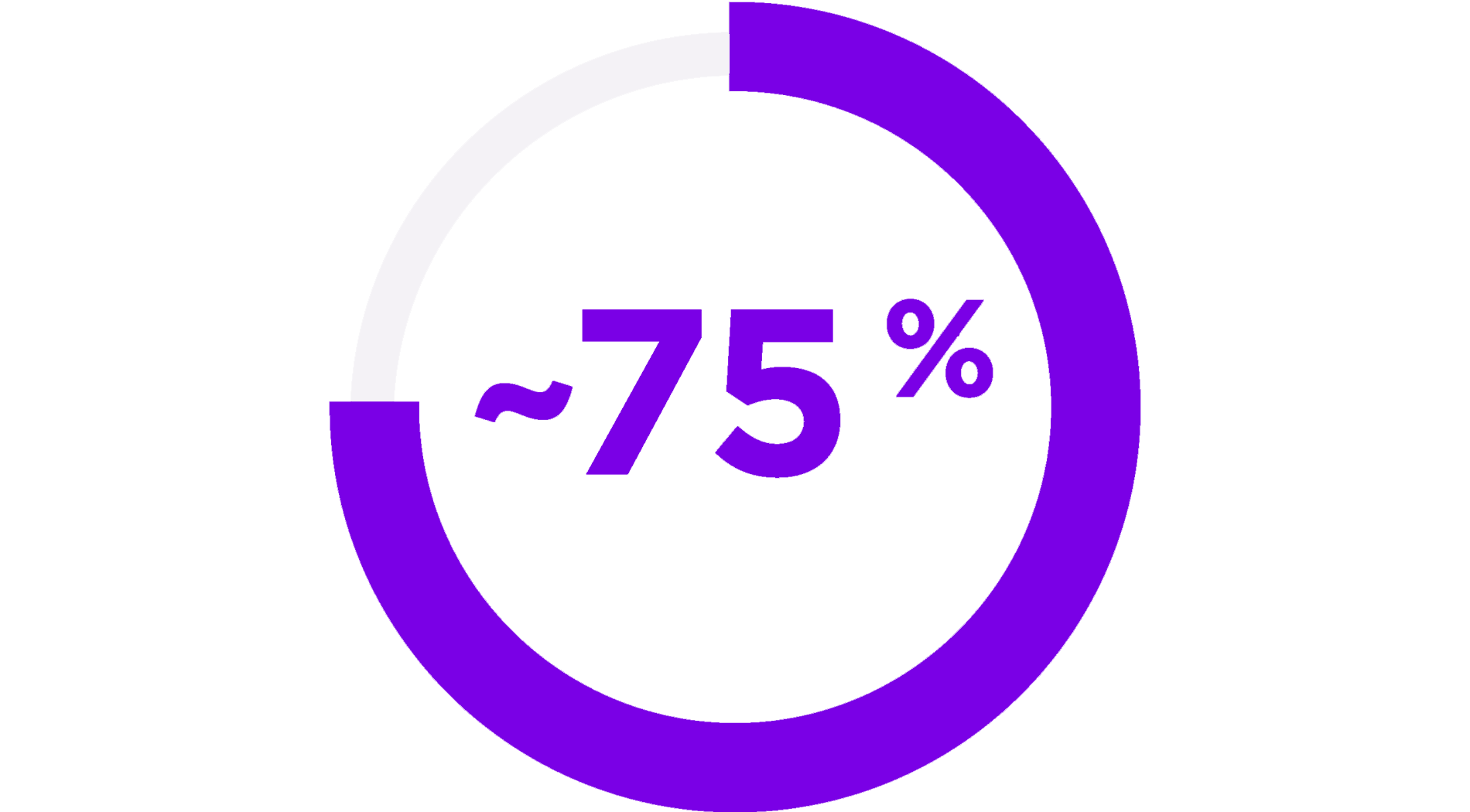
Rhinite allergique
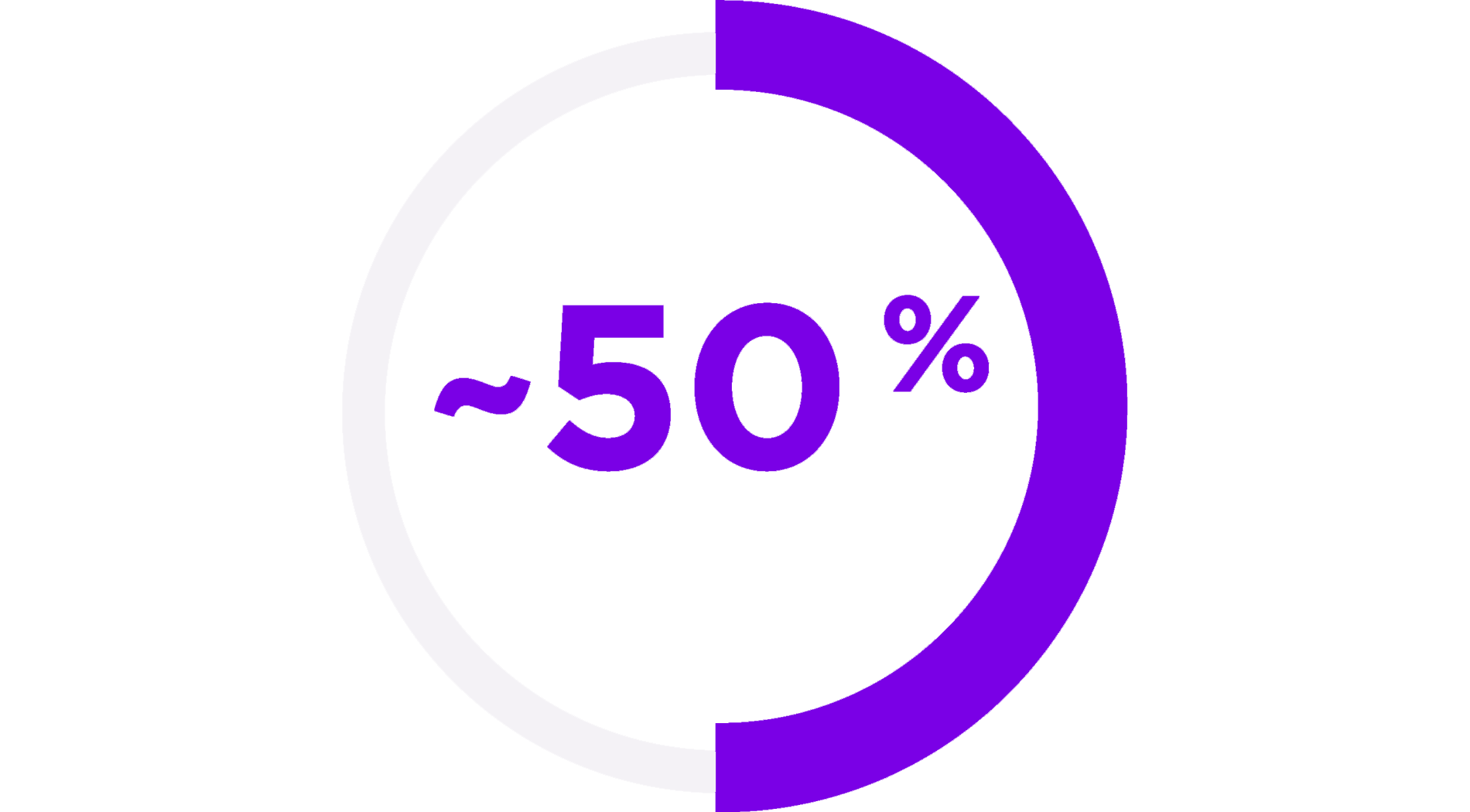
Asthme
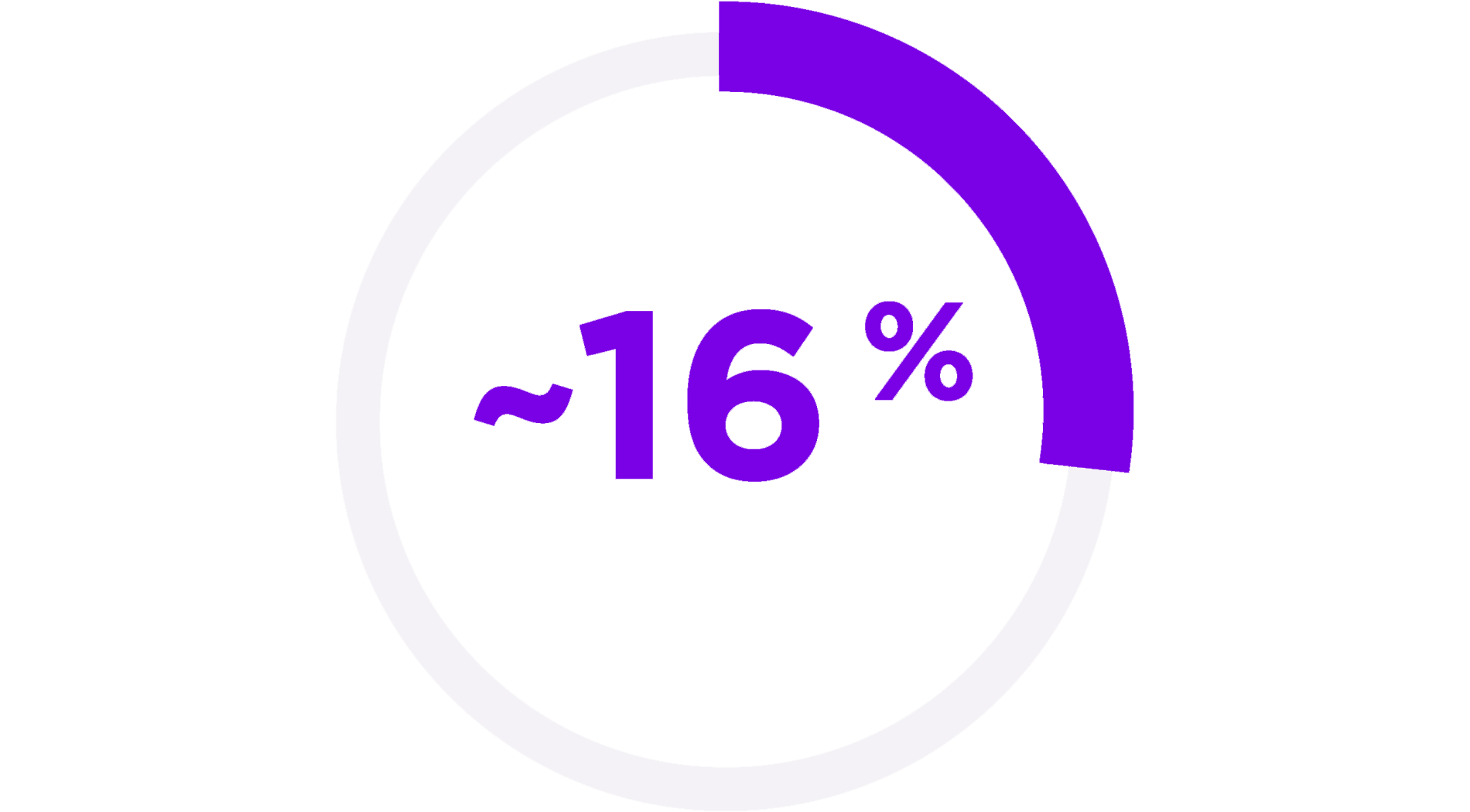
Dermatite atopique
Ces manifestations s'additionnent et aggravent le fardeau global : sommeil perturbé, fatigue chronique, limitations des activités quotidiennes et impact sur la vie sociale et professionnelle. La combinaison de ces troubles détériore la qualité de vie des patients.3-5
*Dans l’étude, les patients étaient atteints d’une forme modérée à sévère selon les critères de l’EPOS.
PNS et Asthme, deux pathologies intriquées

Les patients atteints à la fois d’asthme et de PNS présentent des symptômes plus sévères5,9,10*

- Non-contrôle des symptômes de l'asthme5
- Obstruction des voies respiratoires accrue5
- Inflammation des voies respiratoires inférieures plus marquées5

Recours plus fréquents aux corticostéroïdes5

Altération plus importante de l'odorat5

Taux de reprise chirurgical plus élevé :
JUSQU'À 3X PLUS de recidives dans les 12 années suivant la chirurgie9,10
*Chez les patients atteints de PNS avec un asthme associé comparé aux patients sans asthme associé.
Inflammation de type 2 : un mécanisme commun
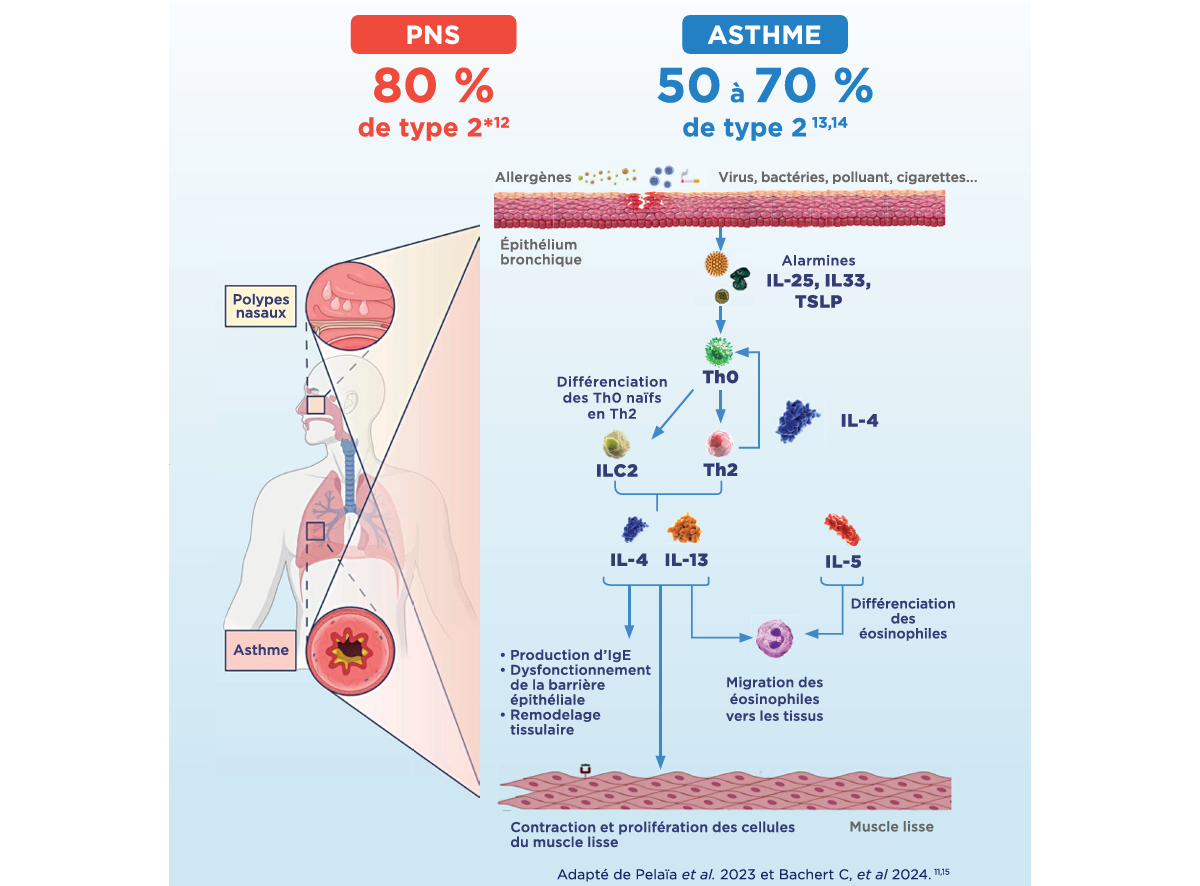
CSO: Corticosteroid-resistant oraux ; IgE: Immunoglobulins E ; E: Eosinophils ; IL: Interleukin ; ILC2: Innate lymphoid cells 2 ; Th0: Lymphocytes T auxiliaires naïfs ; Th2: Lymphocytes T auxiliaires de type 2
La PNS et l'asthme résultant majoritairement* d'une inflammation chronique de type 2 impliquant l'immunité innée et adaptative.11
Cette inflammation mobilise des cellules clés comme les alarmines (IL-25, IL-33, TSLP) qui jouent un rôle central dans l'amplification de cette réponse mais également les lymphocytes Th2 et les ILC2, qui participent à la production de cytokines telles que l'IL-4, l'IL-5 et l'IL-13. L'IL-4 et l'IL-13 favorisent la commutation isotypique des lymphocytes B vers la production d'IgE, un élément clé de la réponse allergique.11
L'ensemble de ces médiateurs entretient l'inflammation des voies aériennes supérieures et inférieures. Cette réponse altère l'intégrité épithéliale, facilitant l'entrée d'allergènes et de pathogènes à l'origine des symptômes.2,3,11
Des symptômes distincts :2,3,11
|
Une qualité de vie altérée, des symptômes respiratoires persistants, un recours aux CSO fréquent.3,11 |
*Dans les pays occidentaux.
Voyez-vous cette patiente ?

Cas patient Alexandra, 45 ans*
« Je sens de moins en moins, mon nez bouché m’empêche de bien dormir, je suis gênée au quotidien. »
Alexandra, 45 ans, présente une PNS SÉVÈRE AVEC ASTHME CONTRÔLÉ.
TABLEAU CLINIQUE

| HISTORIQUE THÉRAPEUTIQUE : • Ethmoïdectomie il y a 3 ans suite à une aggravation des symptômes • Observante aux corticostéroïdes intra-nasaux • CSI à faible dose • 2 cures de corticostéroïdes oraux dans l'année Dose cumulée annuelle de CSO : 760 mg. |
À surveiller : la dose cumulée annuelle de corticothérapie systémique, seuil recommandé ≤ 1 g/an pour tous les patients, ≤ 500 mg/an pour les patients à risque.
*Cas patient fictif
**Score de 0 à 3
0 : pas de symptômes, 1 : symptômes légers, 2 : symptômes modérés, 3 : symptômes sévères.
ACT : test de contrôle de l'asthme (asthma control test) ; CSI : corticostéroïdes inhalés ; LABA : B2-agoniste de longue durée d’action
Évaluer dose cumulée annuelle de CSO pour prendre en compte le risqué d'effets indésirables à long terme :16

Dose cumulée annuelle
≥ 500 MG / AN
pour les patients à risque
(obesité, diabète, ostéoporose, population pédiatrique par exemple)

Dose cumulée annuelle
≥ 1 G / AN
pour tous les patients
Voyez-vous ce patient ?

Cas patient Claude, 68 ans*
« Je suis très gêné par ma PNS et ma perte d'odorat et depuis quelques semaines je me sens plus essoufflé. »
Claude, 68 ans présente une PNS SÉVÈRE AVEC ASTHME PARTIELLEMENT CONTRÔLÉ.
TABLEAU CLINIQUE

| HISTORIQUE THÉRAPEUTIQUE : • Aggravation des symptômes 1 an après une ethmoïdectomie • Observant aux corticostéroïdes intra-nasaux • 2 cures de corticostéroïdes oraux dans l'année • Dose cumulée annuelle de CSO : 1 g, seuil maximal atteint |
À surveiller : la dose cumulée annuelle de corticothérapie systémique, seuil recommandé ≤ 1 g/an pour tous les patients, ≤ 500 mg/an pour les patients à risque.
*Cas patient fictif
**Score de 0 à 3
0 : pas de symptômes, 1 : symptômes légers, 2 : symptômes modérés, 3 : symptômes sévères.
ACT : test de contrôle de l'asthme (asthma control test) ; CSI : corticostéroïdes inhalés ; LABA : B2-agoniste de longue durée d’action
Évaluer dose cumulée annuelle de CSO pour prendre en compte le risqué d'effets indésirables à long terme :16

Dose cumulée annuelle
≥ 500 MG / AN
pour les patients à risque
(obesité, diabète, ostéoporose, population pédiatrique par exemple)

Dose cumulée annuelle
≥ 1 G / AN
pour tous les patients
Une approche multidisciplinaire indispensable : la collaboration ORL-Pneumologue
La forte association de la polypose naso-sinusienne et de l'asthme, majoritairement liée à des mécanismes inflammatoires de type 2*, rend indispensable une approche diagnostique et thérapeutique multidisciplinaire.1,11
Que recommande la SFORL ?17
La prise en charge a évolué pour intégrer des réunions multidisciplinaires (ORL-Pneumologues-Allergologues) dans les décisions diagnostiques et thérapeutiques de certaines polyposes naso-sinusiennes sélectionnées.
La SFORL recommande :
- Le dépistage de l'asthme sur la base de l'anamnèse chez les patients atteints de polypose naso-sinusienne.
- L'évaluation du contrôle de l'asthme associé dans l'évaluation de la sévérité de la polypose naso-sinusienne.
*Dans les pays occidentaux, 80% de type 2 retrouvé chez les patients atteints de PNS : 50 à 70% chez les patients atteints d’asthme.12-14
Dépister systématiquement l’asthme de votre patient
Selon la SPLF, quels symptômes évocateurs d'asthme sont à rechercher chez vos patients atteints de polypose naso-sinusienne ?18 Les récentes recommandations françaises reprenant le GINA précisent que la présence de plus d'un symptôme (sifflement, dyspnée, toux, oppression thoracique) est évocatrice d'asthme.18
Ces symptômes sont typiquement :18
- aggravés la nuit ou au réveil,
- variant dans le temps et en intensité,
- possèdent souvent des facteurs déclenchants bien identifiés (virus, exercice, allergènes...).
EN CAS DE SUSPICION D'ASTHME CHEZ VOTRE PATIENT, ADRESSEZ-LE À UN PNEUMOLOGUE QUI POURRA CONFIRMER LE DIAGNOSTIC.
PNS et asthme comorbide : impact sur la qualité de vie et le contrôle3,11

1 PATIENT SUR 2 avec une polypose naso-sinusienne modérée à sévère ont aussi un asthme1
Une prise en charge optimale repose non seulement sur le traitement des symptômes, mais aussi sur l'évaluation régulière du contrôle de la maladie et de la qualité de vie.
Des outils validés permettent d'objectiver ces dimensions :
- SNOT-22 : mesure de l'impact des symptômes de la polypose naso-sinusienne sur la qualité de vie
- ACT : évalue le contrôle de l'asthme et son influence sur les activités quotidiennes
Selon si la prise en charge des symptômes de la polypose naso-sinusienne est optimale ou non, et face à :
- Une aggravation des difficultés respiratoires
- Une plainte d'être très essoufflé
- Une difficulté à respirer correctement
UN BILAN D'ASTHME EST À ENVISAGER AVEC SON PNEUMOLOGUE.
Références
- Khan A, et al. The Global Allergy and Asthma European Network (GALEN rhinosinusitis cohort): a large European cross-sectional study of chronic rhinosinusitis patients with and without nasal polyps. Rhinology. 2019;57(1):32-42.
- Abdalla S, et al. Prevalence of sinonasal outcome test (SNOT-22) symptoms in patients undergoing surgery for chronic rhinosinusitis in the England and Wales National prospective audit. Clin Otolaryngol. 2012;37(4):276-282.
- GINA. Global strategy for asthma management and prevention. Updated 2025.
- Hello M, et al. Dermatite atopique de l'adulte. La Revue de médecine interne. 2016;37:91-99.
- Langdon C, Mullol J. Nasal Polyps in patients with asthma: prevalence, impact, and management challenges. J Asthma Allergy. 2016;9:45-53.
- Shaw DE, et al. Clinical and inflammatory characteristics of the European U-BIOPRED adult severe asthma cohort. Eur Respir J. 2015;44:1308-1321.
- Maio S, et al. RITA: The Italian severe uncontrolled asthma registry. Eur J of Allergy and clinical immunology. 2018;73(3):683-695.
- Matsusoka M, et al. Phenotype of asthma related with high serum periostin levels. Allergology international. 2015;64(2):175-180.
- Sella GC, et al. Asthma Is the Dominant Factor for Recurrence in Chronic Rhinosinusitis. American Academy of Allergy, Asthma & Immunology. 2020;8(1):302-309.
- Lotus CA, et al. Revision surgery rates in chronic rhinosinusitis with nasal polyps: meta-analysis of risk factors. Int Forum Allergy Rhinol. 2020;10(2):199-207.
- Pelajo C, et al. Pathology of Type 2 Inflammation in Asthma and Nasal Polyposis. J Clin Med. 2021;12(10):3371.
- Chaaban MR, et al. Epidemiology and differential diagnosis of nasal polyps. Am J Rhinol Allergy. 2013;27(6):473-478.
- Seys SF, et al. Cluster analysis of sputum cytokine-high profiles reveals diversity in T(h)2 high asthma patients. Respir Res. 2017;18:39.
- Peters MC, et al. Measures of gene expression in sputum cells can identify TH2-high and TH2-low subtypes of asthma. J Allergy Clin Immunol. 2014;133(2):388-394.
- Bachet C, et al. Burden of Disease in Chronic Rhinosinusitis with Nasal Polyps. J Asthma Allergy. 2021;14:127-134.
- Bourdin A, et al. How can we minimise the use of regular oral corticosteroids in asthma? Eur Respir J. 2020;29:1900085.
- SFORL. Recommandation de pratique clinique. Prise en charge ORL de la Polypose Naso-sinusienne de l'adulte (argumentaire bibliographique). 2023.
- Raherison-Semjen C, et al. Mise à jour des recommandations (2021) pour la prise en charge et le suivi des patients asthmatiques adultes sous l'égide de la Société de pneumologie de langue française (SPLF) et de la Société pédiatrique de pneumologie et allergologie (SP²A). Version longue. Rev Mal Respir. 2021;38:1048-1083.
MAT-FR-2601578-04/26