- Article
- Source : Campus Sanofi
- 24 avr. 2026
Les acteurs clés de l’inflammation de type 2 dans la polypose naso-sinusienne (PNS)
📌 Les points clés
• L'inflammation de type 2 est présente chez 80% des patients atteints de PNS, médiée par les cytokines de type 2 : IL-4, IL-5 et IL-13 responsables de la production d'IgE, de l'activation des éosinophiles et du remodelage tissulaire
• Les acteurs clés de cette inflammation sont les alarmines (TSLP, IL-33 et IL-25), les cellules innées de type 2 (ILC2), lymphocytes Th2 (LTh2), les cytokines de type 2, éosinophiles et les Immunoglobulines de type E (IgE)
• Les biomarqueurs de référence pour identifier un endotype T2 sont les éosinophiles sanguins ou tissulaires et les IgE totales, complétés par l'Eosinophil Cationic Protein (ECP) et la périostine reflétant l'activation éosinophilique et le remodelage tissulaire
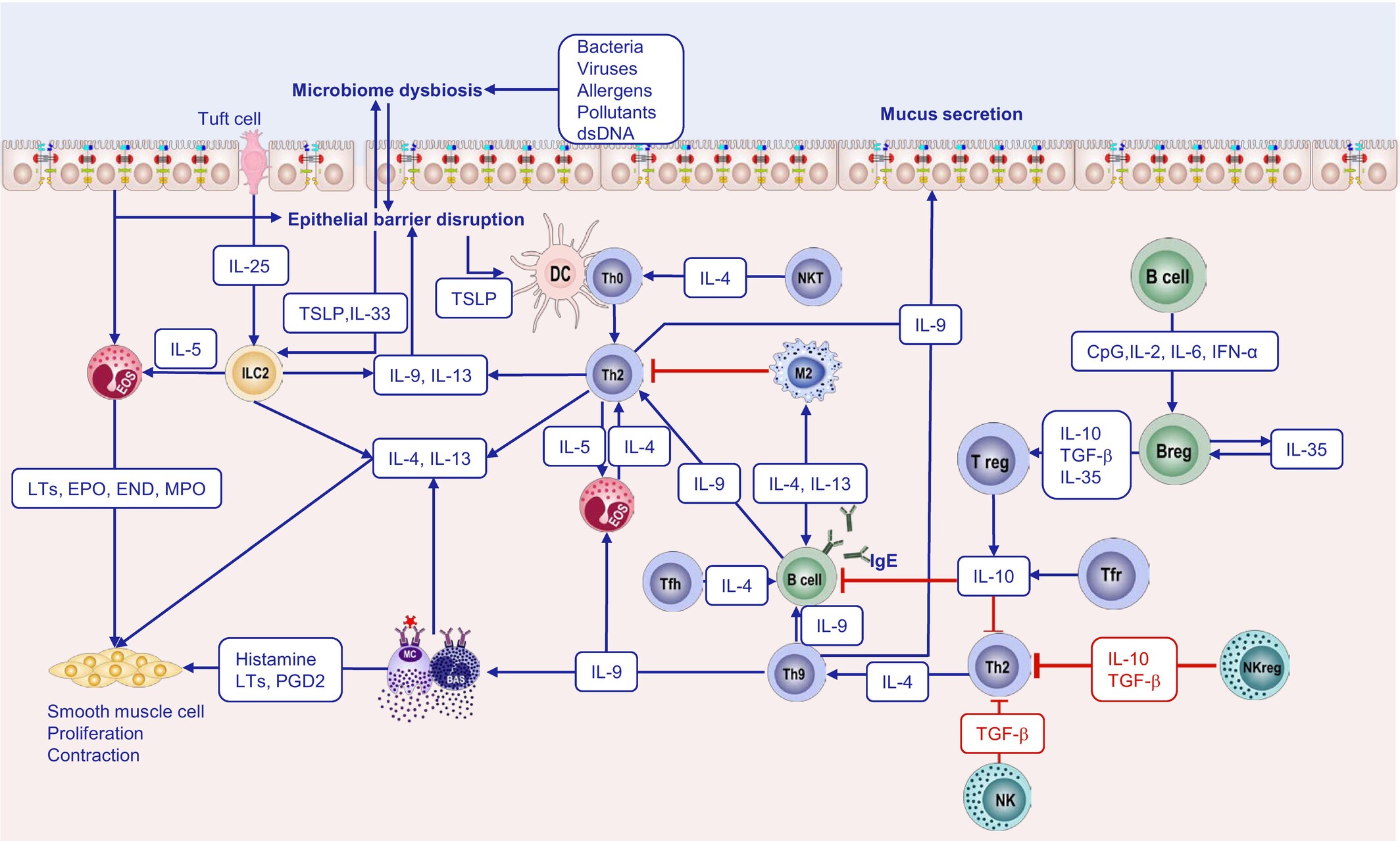
Gao et al., Allergy 2025
DC, dendritic cell (cellule dendritique) ; ILC2, type 2 innate lymphoid cells (cellules lymphoïdes innées de type 2) ; NKT, natural killer T (lymphocyte T natural killer) ; Tfh, T follicular helper cell (lymphocyte T auxiliaire folliculaire) ; Tfr, follicular regulatory T cell (lymphocyte T régulateur folliculaire) ; TGF-β, transforming growth factor-β (facteur de croissance transformant bêta) ; TSLP, thymic stromal lymphopoietin (lymphopoïétine stromale thymique).
Les alarmines sont des signaux d'alarme libérés par l'épithélium nasal en réponse à des agressions extérieures ou à un stress tissulaire. Elles constituent le point de départ de la cascade inflammatoire de type 2 en activant les cellules de l'immunité innée et adaptative, notamment les ILC2 et les cellules dendritiques, pour orienter la réponse immune vers un profil Th2. Trois alarmines jouent un rôle central dans la PNS.
- TSLP
Elle active les cellules dendritiques pour polariser les lymphocytes T naïfs vers un phénotype Th2.
- IL-33
Elle active directement les ILC2 et polarise les lymphocytes naïfs vers un phénotype Th2, induisant la production rapide d'IL-5 et d'IL-13. Elle favorise ainsi le recrutement des éosinophiles et entretient l'inflammation chronique.
- IL-25
Elle agit en synergie avec l'IL-33 pour stimuler les ILC2 et amplifie la production d'IL-5 et d'IL-13, contribuant au remodelage tissulaire et à la persistance de l'inflammation de type 2.
Les ILC2 sont les cellules effectrices de l'immunité innée, déclenchées par les alarmines. Elles produisent des cytokines de type 2, principalement IL-5 et IL-13, et dans une moindre mesure IL-4.
Leur activation est amplifiée par l'IL-2 dérivée des lymphocytes Th2, créant une boucle d'amplification positive de l'inflammation chronique. Les ILC2 coopèrent ainsi avec les lymphocytes Th2 pour maintenir l’éosinophilie, la production de mucus et le remodelage tissulaire.
Les lymphocytes Th2 sont une sous-population de lymphocytes T CD4+ spécialisée dans la régulation des réponses immunitaires de type 2.
Leur différenciation est induite par l'IL-4, qui active la voie de signalisation STAT6 et le facteur de transcription GATA-3. Une fois différenciés, les lymphocytes Th2 produisent principalement l'IL-4, l'IL-5 et l'IL-13, orchestrant ainsi l'ensemble de la réponse inflammatoire de type 2.
- IL-4 : Polarisation Th2 et commutation IgE
C’est la cytokine pivot de la différenciation des lymphocytes T naïfs vers le phénotype Th2 et de la commutation isotypique des lymphocytes B vers la production d'IgE.
- IL-13 : Remodelage tissulaire et dysfonction épithéliale
Elle induit l'hyperproduction de mucus, la fibrose sous-épithéliale et l'altération de la barrière muqueuse. C’est le principal médiateur du remodelage tissulaire dans la PNS.
- IL-5 : Eosinophilie et activation cellulaire
L'IL-5 est le facteur de croissance, de différenciation et de survie spécifique des éosinophiles. Elle est produite par les lymphocytes Th2 et les ILC2, et son taux corrèle avec le degré d'éosinophilie sanguine et tissulaire.
Les éosinophiles sont des leucocytes impliqués dans l’immunité et l’inflammation de type 2. Leurs valeurs usuelles sont généralement comprises entre 30 et 500/mm³. Ils participent à l’inflammation et au remodelage tissulaire dans des pathologies comme la polypose naso-sinusienne, sous le contrôle de cytokines telles que l’IL-5, l’IL-4 et l’IL-13.
LES DIFFÉRENTS SEUILS
- Éosinopénie
Diminution des éosinophiles circulants à une valeur très basse (pas de seuil universel unique et défini) le plus souvent transitoire et sans signification clinique isolée, pouvant être observée notamment en cas de : stress aigu, infection sévère, corticothérapie. Ces situations traduisent généralement une redistribution des éosinophiles plutôt qu’une anomalie pathologique durable.
- Éosinophilie
Augmentation des éosinophiles circulants, fréquente dans les maladies inflammatoires de type 2 :
- Éosinophilie : > 500/mm³
- Hyperéosinophilie (HE) : ≥ 1 500/mm³. Elle peut être liée à différentes étiologies telles que réactionnelles (allergiques, médicamenteuses, infectieuses), hématologiques et systémiques.
- Syndrome hyperéosinophilique (SHE) : HE et atteinte d’organe associée.
Les IgE sont des anticorps impliqués dans les réponses immunitaires de type allergique et de type 2.
- IgE totales
Il existe des valeurs de référence variables selon l'âge, mais aucun seuil diagnostique universel de l'atopie. Dans la PNS, les IgE totales sériques sont fréquemment élevées, même chez les patients non atopiques, reflétant une production locale polyclonale plutôt qu'une sensibilisation systémique.Des taux élevés sont fréquemment associés à un asthme comorbide.
- IgE spécifiques :
Positives au-delà de 0,35 kUA/L, elles témoignent d'une sensibilisation sans préjuger de la pertinence clinique.
PARTICULARITÉS DANS LA PNS
- IgE anti-entérotoxines staphylococciques : S. aureus (présent chez ~64 % des patients) induit une réponse IgE polyclonale locale, marqueur de sévérité et de risque d'asthme associé
- Production locale prédominante : les IgE tissulaires activent les mastocytes indépendamment des IgE sériques (les tests conventionnels sous-estiment leur rôle)
- Polyclonalité : contrairement à l'allergie classique, les IgE de la PNS sont polyclonales, pouvant saturer les récepteurs mastocytaires
MÉCANISME DE SYNTHÈSE
- Voie allergique classique :
- L’exposition à un allergène entraîne sa présentation par les cellules dendritiques, puis la différenciation des lymphocytes T naïfs en cellules Th2.
- Les cytokines Th2, notamment IL-4 et IL-13, induisent la commutation isotypique des lymphocytes B vers la production d’IgE spécifiques.
- Voie innée épithéliale :
- Une dysfonction de la barrière épithéliale favorise la libération d’alarmines telles que TSLP, IL-25 et IL-33.
- Ces cytokines activent les ILC2, qui produisent principalement IL-5 et IL-13, amplifiant l’inflammation de type 2, l’éosinophilie et un environnement favorable à la production locale d’IgE.
- Voie des superantigènes :
- Dans la PNS particulièrement, les entérotoxines de S. aureus peuvent agir comme superantigènes en liant directement le CMH-II et le TCR, sans présentation antigénique classique.
- Cette activation polyclonale favorise une réponse inflammatoire de type 2 et une production locale importante d’IgE polyclonales, notamment d’IgE anti-entérotoxines staphylococciques, indépendamment d’une sensibilisation allergénique classique.
L’ECP et la périostine apparaissent comme des biomarqueurs pertinents de l’inflammation de type 2 dans la PNS, en particulier de l’activation éosinophilique et du remodelage tissulaire. Toutefois, leur place en pratique clinique reste complémentaire, les biomarqueurs les plus établis pour l’identification d’un endotype T2 demeurant les éosinophiles sanguins ou tissulaires, avec parfois les IgE totales.
- ECP : marqueur de la dégradation éosinophilique
L'ECP (Eosinophil Cationic Protein) est une protéine cationique stockée dans la matrice des éosinophiles et libérée lors de leur dégranulation. Elle exerce une cytotoxicité par formation de pores membranaires et possède une activité ribonucléase, reflétant l'activation fonctionnelle des éosinophiles.
- Périostine : témoin du remodelage IL-13 dépendant
La périostine est une protéine de la matrice extracellulaire induite par l'IL-13 et l'IL-4 dans les fibroblastes et les cellules épithéliales, impliquée dans la fibrose sous-épithéliale et le remodelage tissulaire chronique. Dosable dans le sérum et les sécrétions nasales, elle constitue un biomarqueur non invasif de l'activité IL-13 et du remodelage en cours.
Conclusion
L’inflammation de type 2 constitue un mécanisme central dans la physiopathologie de la polypose naso-sinusienne, impliquant l’activation coordonnée des alarmines épithéliales, des cellules ILC2, des lymphocytes Th2 et des cytokines associées (IL-4, IL-5, IL-13). Cette cascade conduit notamment à une éosinophilie, à une production d’IgE et à des phénomènes de remodelage tissulaire.
Certains biomarqueurs, tels que les éosinophiles sanguins ou tissulaires, et dans une moindre mesure les IgE, l’ECP ou la périostine, peuvent contribuer à la caractérisation de ce profil inflammatoire en pratique clinique, sans toutefois constituer à eux seuls des critères diagnostiques.
La prise en charge de la PNS repose sur une évaluation globale du patient, intégrant les symptômes, la qualité de vie et les données biologiques, conformément aux recommandations en vigueur.
Références
- Chaaban MR, Walsh EM, Woodworth BA. Epidemiology and differential diagnosis of nasal polyps. Am J Rhinol Allergy. 2013;27(6):473–478.
- Gandhi NA, Bennett BL, Graham NMH, Pirozzi G, Stahl N, Yancopoulos GD. Targeting key proximal drivers of type 2 inflammation in disease. Nat Rev Drug Discov. 2016;15(1):35-50.
- Schleimer RP (2017). Immunopathogenesis of Chronic Rhinosinusitis and Nasal Polyposis. Annual Review of Pathology: Mechanisms of Disease, 12 : 331–357
- Tatsumi N & Kumamoto Y. (2025). The role of IL-2 in type 2 immunity. Frontiers in Immunology, 16 : 1622187.
- Zhu J, Yamane H & Paul WE. (2010). Differentiation of Effector CD4 T Cell Populations. Annual Review of Immunology, 28 : 445–489.
- Groh M, Lefèvre G, Kahn JE, et le groupe de travail. PNDS Hyperéosinophilies et Syndromes Hyperéosinophiliques. Juin 2022.
- Silva JM, Costa AM, Tuna C, et al. Eosinopenia as predictor of infection in patients admitted to an internal medicine ward: a cross-sectional study. Porto Biomed J. 2020;5:6(e084).
- Wechsler ME, Munitz A et al. Eosinophils in Health and Disease: A State-of-the-Art Review. Mayo Clin Proc. 2021;96(10):2694-2707. doi:10.1016/j.mayocp.2021.04.025.
- Gevaert, P., Wong, K., Millette, L. A., & Carr, T. F. (2022). The Role of IgE in Upper and Lower Airway Disease: More Than Just Allergy! Clinical Reviews in Allergy & Immunology, 62(2), 200–215.
- Ansotegui, et Al. (2020). IgE allergy diagnostics and other relevant tests in allergy, a World Allergy Organization position paper. World Allergy Organization Journal, 13(2), 100080
- Acharya, K. R., & Ackerman, S. J. (2014). Eosinophil Granule Proteins: Form and Function. The Journal of Biological Chemistry, 289(25), 17406–17415.
- Abdullah B, Mohamad S et Al. Defining the Role and Clinical Relevance of Periostin in Chronic Rhinosinusitis with or without Nasal Polyps: a Systematic Review and Meta-analysis. Curr Allergy Asthma Rep. 2026;26:5.
- Guo CL, Liu FF, Wang DY, Liu Z. Type 2 Biomarkers for the Indication and Response to Biologics in CRSwNP. Curr Allergy Asthma Rep. 2023;23:703–713.
- Fokkens WJ et al. EPOS/EUFOREA update on indication and evaluation of Biologics in Chronic Rhinosinusitis with Nasal Polyps 2023. Rhinology. 2023;61(3):194-202.
MAT-FR-2601694-04/26