- Article
- Source : Campus Sanofi
- 7 oct. 2025
La Gazette de l’Asthme Sévère : Contrôle des exacerbations

Comment peut-on contrôler les exacerbations de l’asthme ?
Propos recueillis auprès du Dr Naji Khayath (Strasbourg)
L’asthme est une maladie chronique mais également instable évoluant par crises et exacerbations. Actuellement, il existe peu de données qui permettent de prédire les exacerbations et le clinicien se base surtout sur les antécédents personnels d’exacerbation et le contrôle de la maladie . De nouveaux scores ou index sont actuellement évalués pour aider au contrôle des exacerbations.
Actuellement, la littérature ne propose pas d’outil quantifiable. À partir de 2 cohortes longitudinales richement phénotypées et très différentes, l’objectif de cette étude était d’identifier le risque d’exacerbations et de prédire la probabilité de la rémission clinique , au-delà des définitions pharmacologiques standard de l’ERS-ATS/GINA.
La première cohorte, SARP III, américaine, était composée de 528 patients adultes qui ont été suivis pendant environ 5 ans et dont 59 % souffraient d’asthme sévère. La deuxième, U‑BIOPRED, est européenne et comportait 509 patients adultes qui ont été suivis pendant 1 an et dont 83 % étaient atteints d’asthme sévère. Un score composite, burden score, a été élaboré. Centré sur l’instabilité de la maladie, ce score composite agrège des données d’exacerbations, des consultations non programmées, des passages aux urgences, les durées d’hospitalisation et la fréquence d’usage de traitements de secours d’action rapide, rapportés en patients-années.
Les résultats démontrent que le score n’est pas toujours bien relié à la sévérité de l’asthme tel qu’on le classe aujourd’hui. Comme en vie réelle, certains patients ayant une pression thérapeutique faible ont finalement une maladie instable qui nécessite des soins d’urgence. La sévérité fondée sur des critères pharmacologiques a beaucoup de mal à prédire les potentielles exacerbations et le recours aux soins d’urgence. Ce score est également corrélé négativement à la fonction pulmonaire , au contrôle de la maladie et à la qualité de vie . Cela renforce l’idée qu’il est fiable. De plus, un score inférieur à 0,15 identifie la rémission avec une aire sous la courbe (ASC) de 0,96 dans les 2 cohortes (sensibilité > 91 %, spécificité 99 %).
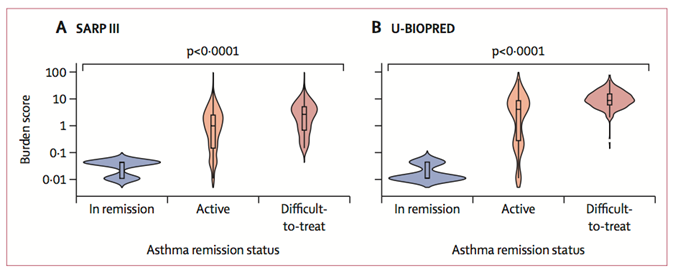
Figure 1 : Burden score en fonction du statut de la maladie (en rémission, active et difficile à traiter)
Se fonder sur le fardeau vécu de la maladie plutôt que sur la sévérité de la prescription permettrait de mieux anticiper les exacerbations. Ce score, dynamique et centré sur le patient, transforme le contrôle des exacerbations en cible opérationnelle. Il propose une lecture prédictive et pragmatique de l’asthme quel que soit le système de santé en vigueur dans le pays. Pour résumer, il permettrait d’identifier aujourd’hui ceux qui auront des exacerbations demain et de guider la prévention individualisée pour tendre vers la rémission clinique. Bien entendu, une validation prospective est souhaitable avant une utilisation en pratique clinique.
Malgré un traitement optimal, les exacerbations peuvent entraîner des conséquences dramatiques pour les patients, surtout quand les comorbidités s’en mêlent. L’asthme est encore une maladie qui engendre trop de décès chaque année : par exemple, au niveau mondial, près de 420000 sont attribuables aux exacerbations de l’asthme chaque année. Cette morbimortalité pourrait être limitée grâce à de nouveaux outils comme l’AECI (Asthma Exacerbation Comorbidity Index) présenté dans cette étude en vie réelle. Le but de cet indice est d’identifier les comorbidités les plus couramment associées à une évolution défavorable de l’asthme, c’est-à-dire à une admission en soins intensifs, une ventilation invasive ou le décès.
Deux cohortes de patients adultes hospitalisés pour exacerbation ont été utilisées dans cette étude rétrospective chinoise. La première, dite cohorte d’entraînement, a inclus 1331 patients entre 2017 et 2021. Une deuxième cohorte, de validation, comportant 453 patients suivis de 2021 à 2023, a permis de confirmer les résultats identifiés lors de l’analyse d’entraînement. 43 comorbidités ont été sélectionnées et évaluées pour chaque patient sous 24 h après le début de l’hospitalisation.
Au total 9 comorbidités sont associées à une évolution défavorable (tableau). Il est important de noter que chaque comorbidité supplémentaire augmente de 25 % le risque du critère composite AECI.
| Tableau. Identification des 9 comorbidités associées à une évolution défavorable de la maladie. | |||
| Comorbidités | RR (IC95) | p | Points |
| Cancer du poumon | 5,63 (1,44-19,16) | 0,008 | 4 |
| Dénutrition | 5,50 (3,28-9,21) | < 0,001 | 4 |
| Maladie rénale chronique | 3,01 (1,26-7,08) | 0,012 | 3 |
| Maladie cérébrovasculaire | 2,90 (1,54-5,38) | 0,001 | 3 |
| Cancers non respiratoires | 2,78 (0,84-8,14) | 0,074 | 3 |
| Hémorragie digestive | 2,71 (1,19-6,14) | 0,017 | 2 |
| Insuffisance cardiaque aiguë | 2,29 (1,01-4,92) | 0,039 | 2 |
| Hypertension | 1,52 (0,98-2,35) | 0,061 | 1 |
| Troubles hydroélectrolytiques | 1,25 (0,83-1,86) | 0,274 | 1 |
Tableau : identification des 9 comorbidités associées à une évolution défavorable de la maladie.
Les résultats montrent que l’AECI dépasse le CCI (Charlson Comorbidity Index) : en effet, toutes les comorbidités ne se valent pas. L’accumulation des dysfonctionnements des systèmes endocrinien, cardiovasculaire et respiratoire marque un terrain vulnérable chez nos patients asthmatiques hospitalisés.
Cet indice AECI pourrait être un nouvel outil de prévention immédiate en ciblant des critères concrets : corriger les désordres hydroélectrolytiques, dépister la dénutrition, optimiser la prise en charge cardiorénale et favoriser la coordination avec le service d’oncologie en cas de cancer.
Dès l’admission, l’AECI pourrait offrir une prédiction rapide des événements graves et aider à maîtriser les exacerbations par une prise en charge précoce des comorbidités à haut risque. Des validations ultérieures multicentriques et prospectives restent cependant nécessaires avant la généralisation de son utilisation.
Au-delà de la prévention des exacerbations, la rémission clinique (RC) de l’asthme est un objectif à rechercher. Aujourd’hui, à peine 10 % des patients atteignent une RC. Pour améliorer ce taux, plusieurs travaux désignent désormais la RC comme un objectif thérapeutique prioritaire, tout en recherchant les discriminants positifs (facteurs prédictifs et modifiables) afin d’optimiser la prise en charge. Cependant, il y a actuellement très peu de données sur la RC en dehors de l’asthme sévère.
Cette étude japonaise, rétrospective, monocentrique, a analysé 263 patients asthmatiques sur 12 mois selon 2 définitions : RC à 3 composantes (aucune exacerbation, aucune corticothérapie orale quotidienne, ACT ≥ 23) et RC à 4 composantes ajoutant un VEMS ≥ 80 %.
Chez les patients atteints d’asthme léger à modéré, la RC est fréquemment atteinte : 81,0 % (3 composantes) et 73,2 % (4 composantes), contre 30,6 % et 33,9 % dans l’asthme sévère. Le tabagisme cumulé (paquets-années) et un IMC élevé diminuent la probabilité de RC. À l’inverse, un début plus tardif et une durée de maladie plus courte favorisent la RC à 4 composantes. Les biomarqueurs de type 2 ne discriminent pas la RC dans cette population.
Cibler la RC chez les patients souffrant d’asthme léger à modéré apparaît comme un levier concret de prévention : l’absence d’exacerbation et le contrôle clinique soutenu s’accompagnent d’une stabilité remarquable à 10 ans (maintien d’un très haut taux de RC : 89,1 % pour celle à 3 composantes et 80,3 % pour celle qui en a 4). Les auteurs en déduisent que viser la RC aide à détecter et corriger précocement les facteurs de risque d’exacerbations, notamment le tabagisme et l’excès pondéral, véritables critères modifiables chez nos patients.
Dans l’asthme léger à modéré, la RC , incluant la normalisation du VEMS, est un objectif atteignable. En pratique, intégrer la RC comme objectif de suivi pourrait permettre de prévenir les exacerbations, d’anticiper le déclin fonctionnel respiratoire , de limiter le remodelage bronchique et de réduire le risque d’évolution défavorable de la maladie.
Références :
- Zein JG et al. Development of an asthma health-care burden score as a measure of severity and predictor of remission in SARP III and U-BIOPRED: results from two major longitudinal asthma cohorts. Lancet Respir Med 2025;13:35-46
- Zhao C et al. Asthma exacerbation comorbidity index (AECI): Predicting in-hospital adverse outcomes. Respir Med 2025;240:108024
- Ishizuka M et al. Clinical remission of mild-to-moderate asthma: rates, contributing factors, and stability. J Allergy Clin Immunol Global 2025;4:100431.
N. Khayath declare avoir des liens d’interets avec ALK, AstraZeneca, GSK, Novartis, Sanofi, Stallergenes, France Oxygene, SOS oxygene et Adiral Assistance.

Lire aussi :
MAT-FR-2503953 - 10/25


