- Artículo
- Fuente: Campus Sanofi
- 27 feb 2026
Qué es la Polimialgia Reumática (PMR)
La PMR es una enfermedad reumática muy común en población mayor
Segunda enfermedad reumática más frecuente después de la AR en población mayor (≥50 años)1,2
- En España, se estima una prevalencia general de 12.7/100.000 habitantes3
Más común en mujeres y en las personas de ascendencia del norte de Europa2
- Más de dos tercios son mujeres2
- Edad media de diagnóstico: 64,5 años4
- Norte vs. sur de Europa: 63,9 vs. 12,7 – 18.7 casos/100,0002
Los signos y síntomas comunes de la PMR incluyen dolor y rigidez matutina
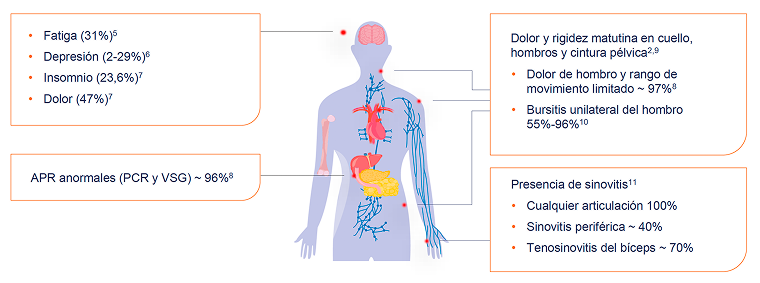
La PMR tiene un gran impacto en la calidad de vida de los pacientes
La enfermedad puede cursar de diferentes formas:12
Sin recaídas
Respuesta rápida sin recaídas significativas
Tratamiento prolongado
Respuesta rápida que requiere un tratamiento prolongado
Sin resolución de síntomas
Resolución incompleta de los síntomas, que requiere tratamiento prolongado con corticoides
Calidad de Vida relacionada con la salud:12
Fatiga diurna
El dolor interfiere con el sueño por la noche, lo que resulta en una fatiga diurna significativa
Rigidez
La rigidez matutina causa dificultad para levantarse de la cama y realizar las actividades diarias
Calidad de vida física y mental
Los niveles más altos de marcadores de actividad de la enfermedad se correlacionan con una menor calidad de vida física y mental
El diagnóstico de la PMR es un reto
- No se dispone de pruebas diagnósticas específicas, lo que a menudo conduce al diagnóstico por exclusión13
- Los médicos a menudo recurren a la respuesta de GC como una "prueba de tratamiento" para establecer el diagnóstico8
- Muchas enfermedades inflamatorias y no inflamatorias pueden confundirse con los síntomas de la PMR14
Enfermedades inflamatorias14
- Artritis reumatoide
- Espondilartritis
- RS3PE
- Artropatía cristalina
- Miositis autoimmune
- Otras enfermedades del tejido conectivo
Enfermedad no inflamatoria14
- Osteoartritis
- Fibromialgia
- Espondilosis y estenosis espinal
- Enfermedad de Parkinson
- Infección
- Neoplasias malignas y síndromes paraneoplásicos
- Miopatía inducida por fármacos
- Enfermedad tiroidea y paratiroidea
EVALUACIÓN PATOLÓGICA: la endoscopia y las biopsias revelan…

- Solo el 60% de los diagnósticos de PMR desde AP, estuvieron de acuerdo con los reumatólogos15
- Los médicos de cabecera informaron de dificultades diagnósticas, especialmente con presentaciones atípicas**16
- Baja precisión del diagnóstico de PMR en un estudio de cohortes (24%, n=123)17
- Reactantes de fase aguda no elevados en 11 de cada 100 recaídas18
- Las directrices de BSR establecen que la PMR puede diagnosticarse con marcadores inflamatorios normales, si existe un cuadro clínico clásico y respuesta a esteroides19
- El estudio de cohortes de PMR excluyó a un tercio de los pacientes basándose en una definición más estricta/estricta* de PMR acordada por los reumatólogos20
Criterios de clasificación ACR/EULAR 2012 de PMR8
- Edad ≥ 50 años en el momento del diagnóstico
- Reactantes de fase aguda elevados (PCR >10 mg/L y/o VSG >30 mm/hora)
- Dolor bilateral en el hombro
- Puntuación en el momento del diagnóstico de ≥4 (sin ecografía) o ≥5 (con ecografía)
| Puntuación | Sin ecografía | Con ecografía |
|---|---|---|
| Duración de la rigidez matutina >45 minutos | 2 | 2 |
| Dolor de cadera o rango de movimiento limitado | 1 | 1 |
| Seronegativo para RF y anti-CCP | 2 | 2 |
| Ausencia de otra afectación articular | 1 | 1 |
| ≥1 hombro con bursitis subdeltoidea y/o tenosinovitis del bíceps y/o sinovitis glenohumeral (posterior o axilar); y ≥1 cadera con sinovitis y/o bursitis trocantérea | N/A | 1 |
| Ambos hombros con bursitis subdeltoidea, tenosinovitis del bíceps o sinovitis glenohumeral | 2 | 2 |
Fisiopatología de la polimialgia reumática
Las artritis inflamatorias como la PMR son impulsadas por una red de citocinas proinflamatorias, incluida la IL-6
Más allá de su presentación clínica, la PMR se caracteriza por una respuesta inflamatoria sistémica mantenida. Diferentes citocinas participan en este proceso, pero la interleucina-6 (IL-6) parece ocupar un lugar central, contribuyendo a la respuesta de fase aguda, al dolor inflamatorio y al riesgo de recaída.1,2,21
Tratamiento estándar de la PMR con glucocorticoides. ¿Existe una dosis “segura”?
Las opciones de tratamiento para la PMR son limitadas
- Los GC siguen siendo el estándar de tratamiento actual22
- Altas tasas de recaídas y efectos adversos asociados al uso acumulado de los mismos
- No existe un estándar de tratamiento establecido en pacientes con respuesta inadecuada a GC
- Resultados contradictorios para algunos agentes ahorradores de GC habituales23
- Bajo nivel de evidencia y no reducción de los efectos adversos asociados a GC
- Bajo nivel de evidencia y no reducción de los efectos adversos asociados a GC
- Los estudios publicados han sugerido un papel de la vía de la IL-6 en la patogénesis de la enfermedad, lo que ha llevado a la aprobación de terapias inhibidoras de IL-6R, como Sarilumab para el tratamiento de la PMR24
Las opciones de tratamiento para la PMR son limitadas
EULAR/ACR Recomendaciones (2015)
Duración mínima efectiva de la terapia con GC23
Recomendaciones de la Sociedad Francesa (2024)
La dosis acumulada de corticosteroides debe ser lo más
baja posible y reducirse gradualmente en un plazo de 12 meses25
Existe una alta tasa de tratamiento prolongado con GC en el manejo de PMR, con altas tasas de recaída
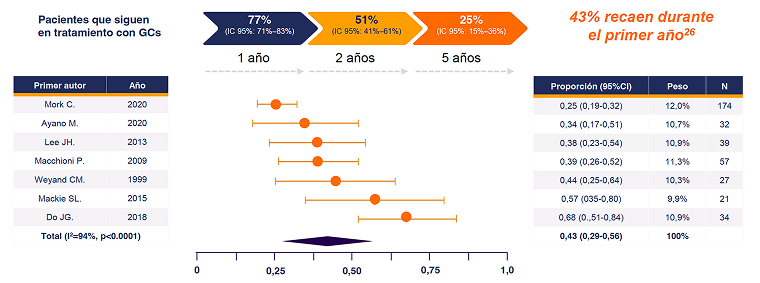
Dosis acumuladas de glucocorticoides administradas a diferentes perfiles de pacientes con PMR
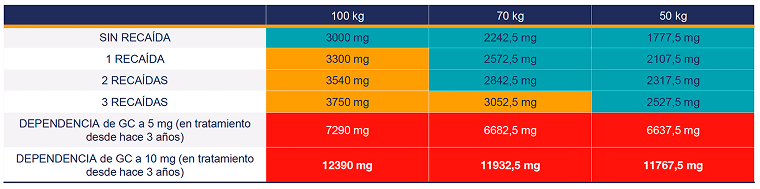
La mayoría de los expertos consideran que un tratamiento dirigido rentable que cure la PMR en 6 meses podría ser utilizado en pacientes desde el inicio y que estaría justificado en caso de corticodependencia por una dosis de GC>3 gramos. Se necesitan estudios futuros para definir mejor las indicaciones específicas de estos tratamientos en PMR.
Los pacientes con PMR tienen un mayor riesgo de comorbilidades asociadas a la GC en comparación con los pacientes sin PMR, incluso a dosis bajas de GC
Osteoporosis27
OR 1,11; IC 95%: 1,06–1,17
Problemas psiquiátricos27
OR 1,15; IC 95%: 1,12–1,19
Enfermedad respiratoria27
OR 1,24; IC 95%: 1,21–1,28
Infarto de miocardio27
OR 1,12; IC 95%: 1,08–1,16
Problemas endocrinos27
OR 1,14; IC 95%: 1,11–1,18
Infecciones27
OR 1,39; IC 95%: 1,35–1,43
Úlcera péptica27
OR 1,05; IC 95%: 0,99–1,11
Cataratas27
OR 1,13; IC 95%: 1,08–1,18
Un estudio en EEUU mostró: 72.5% tienen >2 comorbilidades y 33.8% eran pacientes frágiles al inicio del estudio28
¿Existe una dosis “segura” de corticoides?
Las dosis bajas de GC pueden aumentar rápidamente el riesgo de toxicidad29,30
Incluso <5 mg/día de GC aumentaron el riesgo de enfermedad cardiovascular en la PMR (HR [IC 95%]: 1,52 [1,64–1,84])29
En pacientes con AR, el riesgo de muerte por enfermedad CV nunca volvió a los niveles previos al uso de GC durante > 2 años31
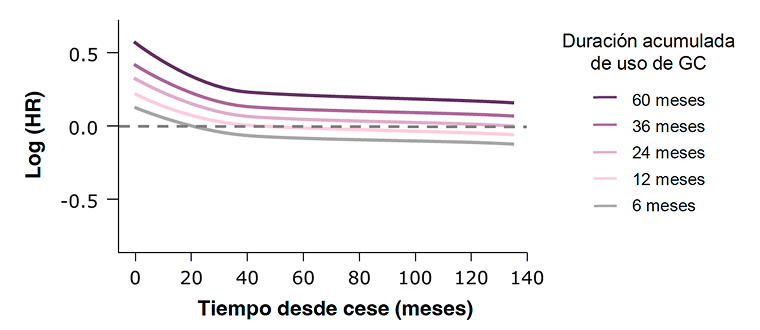
- Riesgo de fractura reportado con dosis GC ≤2,5 mg/día30
- En el plazo de 1 mes32
- Aumenta a los 3 meses (HR [IC 95%] 1,47 [1,22–1,77])33
- El riesgo de fractura aumenta con el uso acumulativo de GC y permanece elevado durante al menos 2 años después de la interrupción34
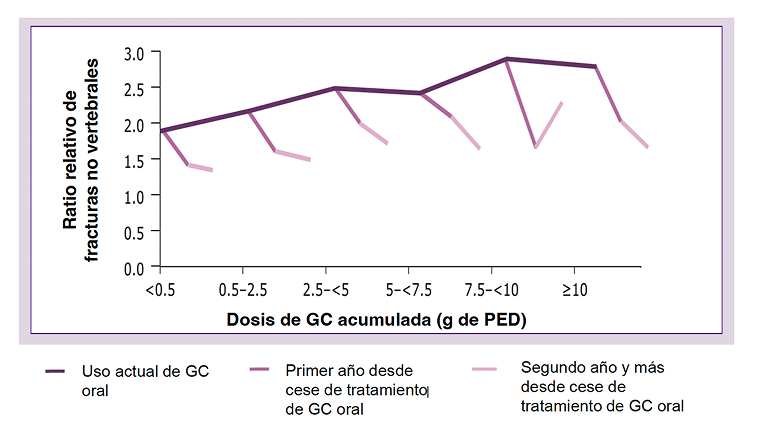
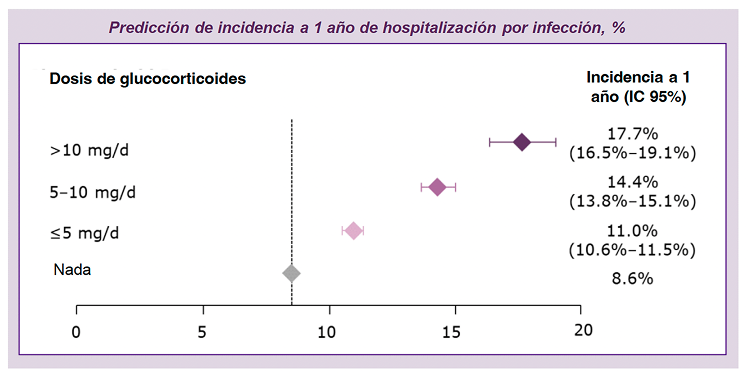
Incluso a dosis bajas de GC se aumentó significativamente el riesgo de hospitalización por infección en el plazo de 1 año en pacientes con AR35
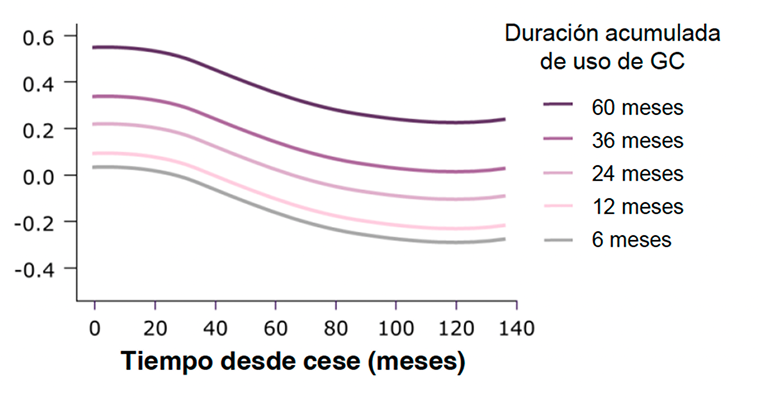
En los pacientes con AR, el riesgo de muerte por infección nunca volvió a los niveles previos al GC después del uso del GC durante >3 años36
El manejo de las comorbilidades de PMR implica evaluar los riesgos, minimizar la toxicidad del GC, mejorar el acceso a la atención y usar agentes ahorradores de GC

Screening de comorbilidades y fragilidad en el momento del diagnóstico y durante el tratamiento37,38

Adaptar los planes de tratamiento (reducción gradual de los GC) para mejorar los resultados37,38
Uso de agentes ahorradores de GC para reducir los riesgos de GC a largo plazo37

Mejorar el acceso a la atención reumatológica y a las pruebas de detección39
Monitorizar comorbilidades que derivan del uso de GC37
Resumen
Se observa una alta tasa de recaída de PMR con el tratamiento con GC
Una parte significativa de los pacientes con PMR permanecen en tratamiento con GC durante ≥1 año
Aproximadamente la mitad de los pacientes tratados con GC experimentarán EA, incluso cuando se usan en dosis bajas a moderadas con el tiempo

Contenido mínimo de Kevzara®
PRESENTACIÓN, PRECIO Y CONDICIONES DE PRESCRIPCIÓN Y DISPENSACIÓN:
KEVZARA® 200 mg solución inyectable en jeringa precargada, envase de 2 jeringas precargadas (CN 716173).
KEVZARA® 200 mg solución inyectable en pluma precargada, envase de 2 plumas precargadas (CN 716176).
PVP notificado: 1.033,06 € PVP IVA notificado: 1.074,38 €
Medicamento sujeto a prescripción médica. Diagnóstico hospitalario. Dispensación hospitalaria sin cupón precinto.
CONSULTE LA FICHA TÉCNICA COMPLETA ANTES DE PRESCRIBIR ESTE MEDICAMENTO.
Kevzara 200mg Jeringa
Kevzara 200mg Pluma
Kevzara está financiado en España de acuerdo con los criterios establecidos por el SNS.
Notas
ACG: arteritis de células gigantes; ACR/EULAR: Colegio Americano de Reumatología/Alianza Europea de Asociaciones de Reumatología; APR: reactantes de fase aguda; AR: artritis reumatoide; CCP: péptido citrulinado cíclico; CV: cardiovascular; EA: evento adverso; FLS: sinoviocito similar a un fibroblasto; GC: glucocorticoide; HR: harzard ratio; HPA: eje hipotálamo-hipófisis-suprarrenal; IC: intervalo de confianza; IL: interleucina; IL-6: interleucina-6; IL-6R: receptor de interleucina-6; PCR: proteína C reactiva; PMR: polimialgia reumática; RF: factor reumatoide; ROM: rango de movimiento; RS3PE: sinovitis simétrica seronegativa remitente con edema con fóvea; VSG: velocidad de sedimentación globular.
*Edad ≥50 años en el momento del diagnóstico; duración de la rigidez matutina ≥45 minutos al inicio; dolor bilateral y/o rigidez en los hombros al inicio del estudio en maniquíes corporales; glucocorticoides orales prescritos en el momento del diagnóstico
**Antecedentes clásicos pero marcadores inflamatorios normales o mala respuesta al tratamiento inicial con glucocorticoides
Referencias
- Camellino D, et al. Nat Rev Rheumatol. 2020; 16(9):481-495
- González-Gay MA, et al. Lancet. 2017; 390(10103):1700-1712
- Cortés Durán PM. Polimialgia y arteritis de células gigantes en un matrimonio. Revista Clínica de Medicina de Familia. octubre de 2017;10(3):197-201
- Raheel S, et al. Arthritis Care Res (Hoboken). 2017; 69(8):1282-1285.
- Green DJ, et al. Scand J Rheumatol. 2015; 44(3):219-223
- Vivekanantham A, et al. Clin Rheumatol. 2018; 37(6):1633-1638
- Prior JA, et al. Prim Health Care Res Dev. 2019; 20:E46
- Dasgupta B, et al. Arthritis Rheum (Reuma de la artritis). 2012; 64(4):943-954
- Mackie SL, et al. Clin Med (Londres). 2013; 13(4):398-400
- Ruta S, et al. Clin. Rheumatol. 2012; 31(9):1383-1387
- Frediani B, et al. J Rheumatol. 2002; 29(1):123-130
- Hutchings A, et al. Arthritis Rheum (Artritis reumatoide). 2007; 57(5):803-809.
- Kermani TA, et al. Ther Adv Musculoskelet Dis. 2014; 6(1):8-19.
- Mahmood. Clev Clin J Med. 2020:549-556.
- Fors C, et al. Rheumatol Adv Pract. 2019; 3(2):rkz033
- Helliwell T, et al. Br J Gen Pract. 2018; 68(676):E783-E793
- Bahlas S, et al. Clin Rheumatol. 2000; 19(4):278-280
- Cantini F, et al. Semin Arthritis Rheum. 2000; 30(1):17-24
- Dasgupta B, et al. Rheumatology (Oxford). 2010; 49(1):186-190
- Müller S, et al. Rheumatology (Oxford). 2020; 59(8):1906-1915.
- 27 Dayer J-M, et al. Rheumatology (Oxford). 2010; 49:15-24
- Buttgereit F, et al. JAMA. 2016; 315(22):2442-2458
- Dejaco C, et al. Ann Rheum Dis. 2015; 74:1799–1807
- Spiera RF, et al. N Engl J Med. 2023 Oct 5;389(14):1263-1272.
- Wendling D et al. Joint Bone Spine. 2024;91(4):105730
- Floris A, et al. Clin Rheumatol. 2022; 41(1):19-31.
- Hoes JN, et al. Ann Rheum Dis. 2009;68(12):1833-1838
- Curtis JR, et al. Arthritis Rheum. 2006;55(3):420-426
- Pujades-Rodriguez M, et al. PLoS Med. 2020;17(12):e1003432
- Van Staa TP, et al. J Bone Miner Res. 2000;15(6):993–1000
- Lacaille D, et al. Arthritis Rheumatol. 2024;76(suppl 9).
- Laan RF, et al. Ann Intern Med. 1993;119(10):963–968
- Iki M, et al. Osteoporos Int. 2024;35(5):805–818
- Van Staa TP, et al. Rheumatology (Oxford). 2000;39(12):1383–1389.
- George MD, et al. Ann Intern Med. 2020;173(11):870–878
- Lacaille D, et al. Arthritis Rheumatol. 2024;76(suppl 9).
- Wending D, et al. Joint Bone Spine 2024; 91:105730
- Dejaco C, et al. Arthrit Rheumatol 2015; 67(10): 2569–2580
- Sattui S, et al. EULAR 2024 Poster #POS1460-HPR
MAT-ES-2503753 - V1 Febrero 2026