- Artículo
- Fuente: Campus Sanofi
- 25 jun 2025
Fase IIIb HARMONIE: estudio de ▼Beyfortus® en lactantes prematuros y nacidos a término sanos, en condiciones similares a las de vida real
Beyfortus® ha demostrado mantener una eficacia del 82,7% en la hospitalización por ITRI-VRS a los 180 días de la administración o aleatorización2
Diseño del estudio
Ensayo pragmático abierto, multicéntrico, paralelo de 2 grupos, realizado en condiciones similares a las de vida real, en el que se compara Beyfortus® frente a ausencia de intervención (tratamiento estándar) durante toda la temporada de VRS.
Uno de los objetivos de este análisis es evaluar la eficacia de nirsevimab durante los 180 días posteriores a la administración de la dosis, un periodo que supera los 5 meses de la temporada típica del VRS.
Se aleatorizó en un ratio 1:1 a una población de 8.057 lactantes menores de 12 meses que habían nacido con ≥29 semanas de edad gestacional antes o durante su primera temporada de VRS. 4.038 recibieron una única inyección intramuscular de nirsevimab (50 mg si < 5kg; 100 mg si ≥5kg) y 4.019 no recibieron ninguna intervención (tratamiento estándar).
Criterio de valoración principal:
Eficacia frente a hospitalización por ITRI-VRS durante la temporada VRS a 150 y 180 días tras la administración de Beyfortus® o aleatorización.
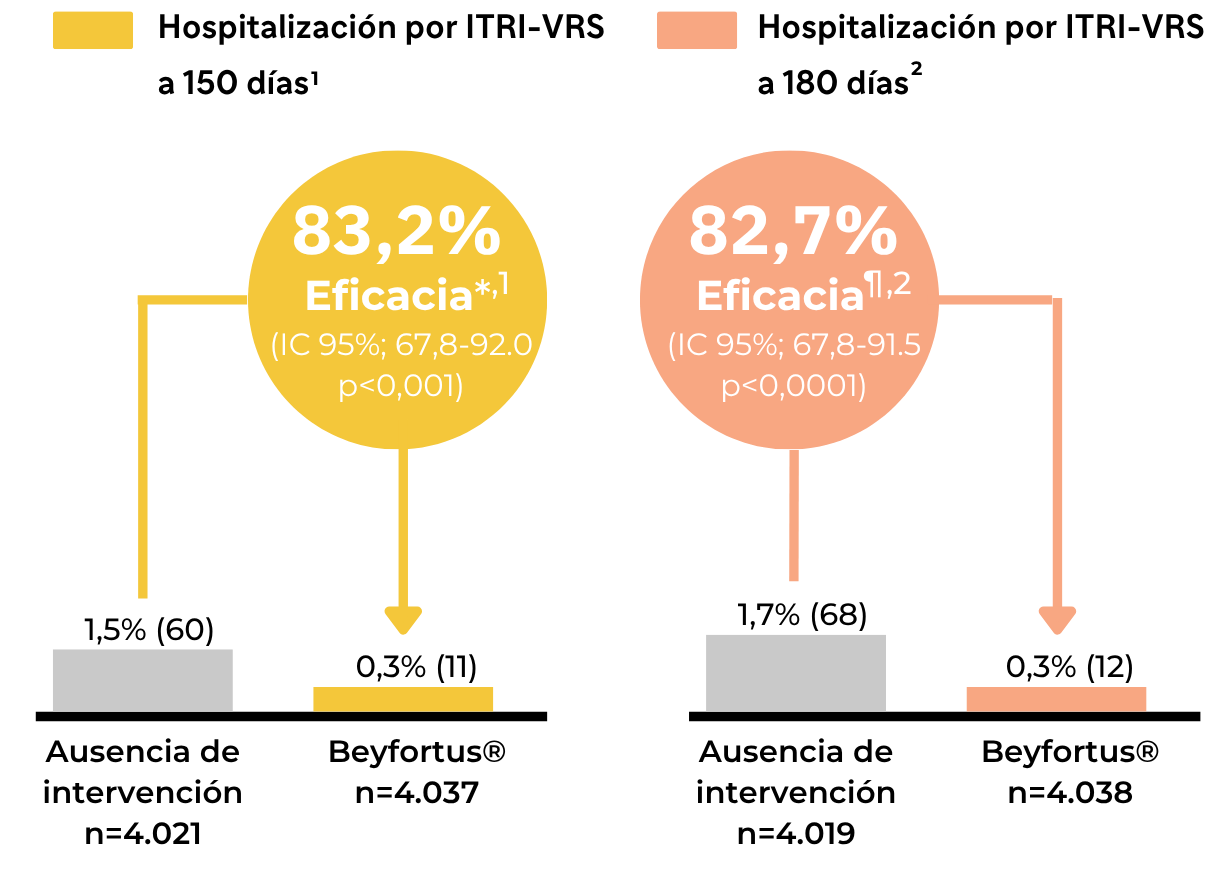
Extraído de (1) Drysdale SB et al. 2023 y (2) Munro APS et al. 2025
Criterios de valoración secundarios:
Eficacia frente a ITRI-VRS muy grave** a 150 y 180 días tras la administración de Beyfortus® o aleatorización.
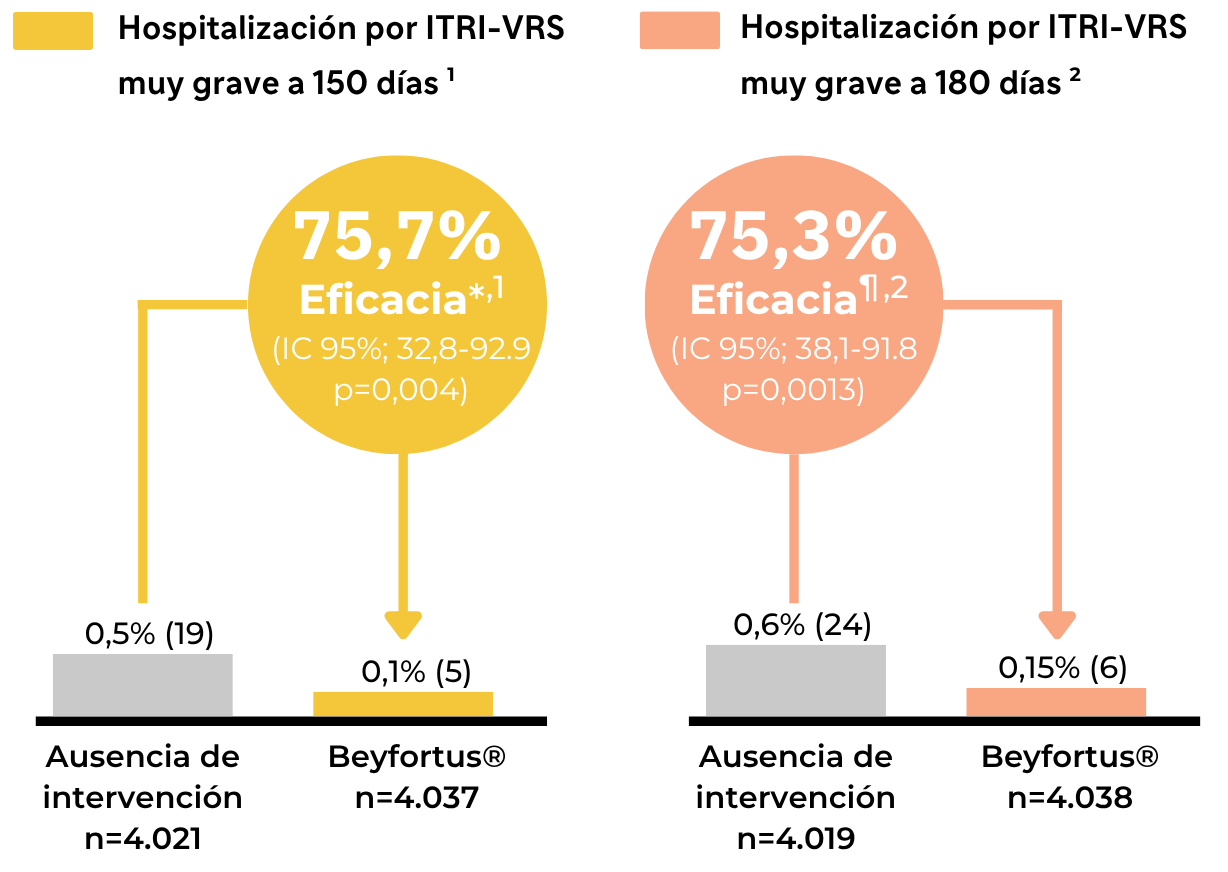
Extraído de (I) Drysdale SB et al. 2023 y (2) Munro APS et al. 2025
Eficacia frente a las hospitalizaciones por ITRI por cualquier causa en el grupo Beyfortus® tanto a 150, como a 180 días tras la administración de Beyfortus® o aleatorización.
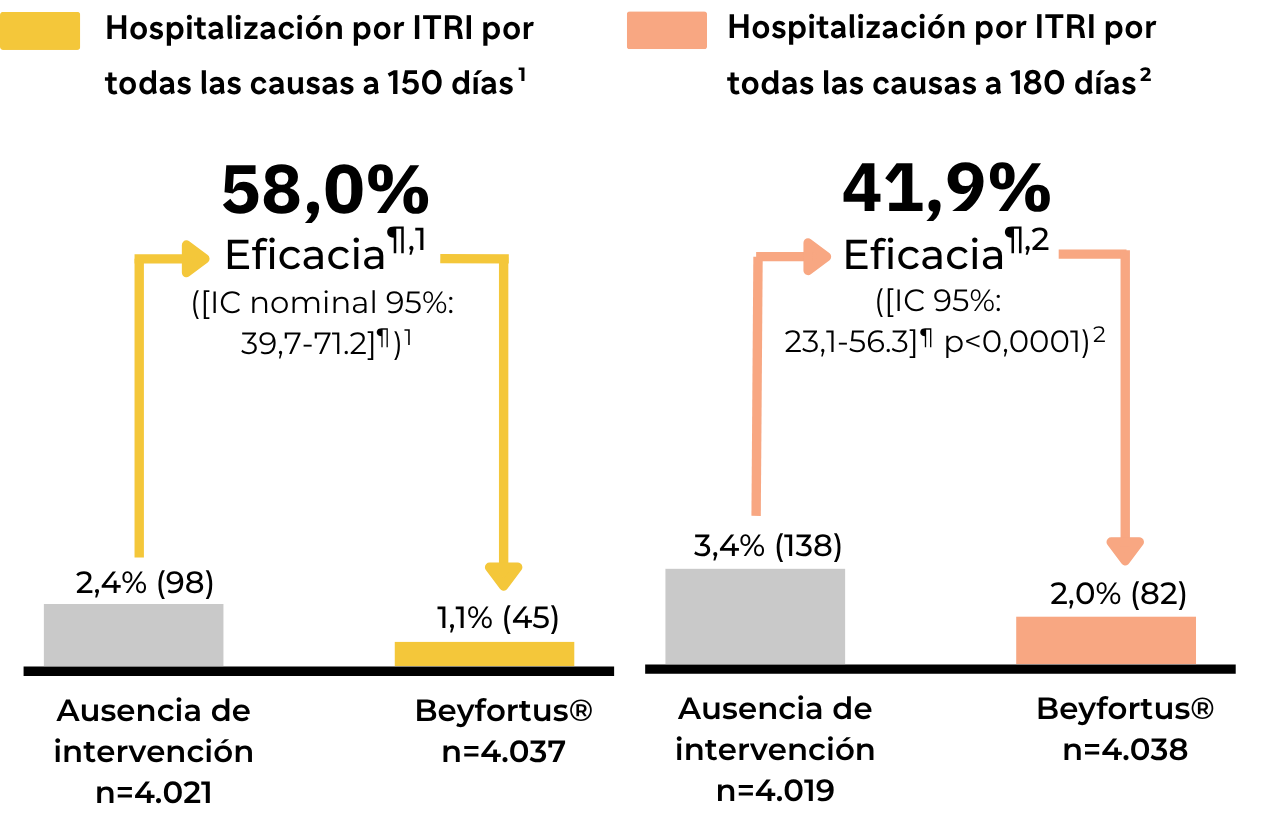
* El IC del 95% para la eficacia se calcula utilizando un método exacto, asumiendo una distribución binomial del número de hospitalizaciones por ITRI en el grupo de nirsevimab, condicionada al número total en ambos grupos (descrito por Breslow y Day), teniendo en cuenta el tiempo de seguimiento tras la administración/aleatorización.
¶No corregido por multiplicidad
** Definido como hospitalización por ITRI-VRS con una saturación de oxígeno «90% [de acuerdo con la definición de caso de la OMS] en cualquier momento de la hospitalización y la necesidad de soporte de oxígeno.
Extraído de (I) Drysdale SB et al. 2023 y (2) Munro APS et al. 2025
Eficacia en la incidencia de hospitalización por VRS por país1
La eficacia de Beyfortus® fue consistente en los tres países participantes. Este estudio proporciona nuevos datos sobre la duración de la protección de Beyfortus® más allá de la temporada típica del VRS, sin pruebas de una disminución significativa durante el periodo de seguimiento ampliado a 180 días.2
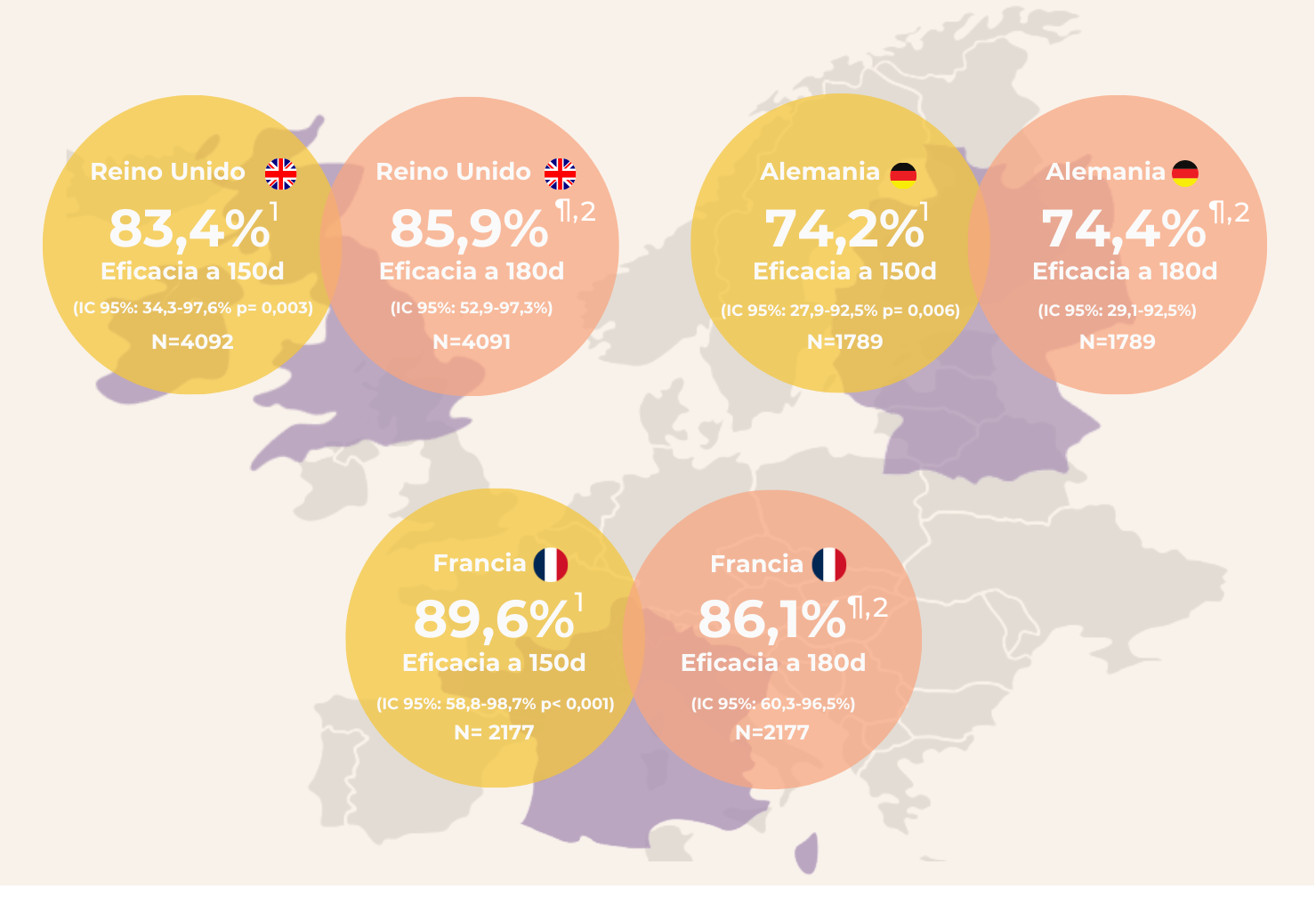
Datos de eficacia frente a la hospitalización por ITRI-VRS en los países participantes del estudio a 150 y 180 días de la administración de Beyfortus® o aleatorización de la población incluida; ¶No corregido por multiplicidad.
Extraído de (1) Drysdale SB et al. 2023 y (2) Munro APS et al. 2025
Los tipos y frecuencias de los AAs fueron similares en los grupos de Beyfortus® y en el grupo con ausencia de intervención. Nirsevimab fue bien tolerado y no se generaron problemas de seguridad aparentes durante los 12 meses siguientes a la aleatorización. 2
De acuerdo con la ficha técnica, la reacción adversa mas frecuente fue la erupción (0,7 %) que se produjo en los 14 días posteriores a la dosis. La mayoria de los casos fueron de intensidad leve a moderada. Además, se notificaron pirexia y reacciones en el lugar de la inyección en una tasa de 0,5 % y 0,3 % dentro de los 7 días posteriores a la dosis, respectivamente.3
ITRI: infección del tracto respiratorio inferior; VRS: virus respiratorio sincitial; ITRI-VRS: infección del tracto respiratorio inferior asociada al virus respiratorio sincitial; IC: intervalo de confianza; N: número;
AAs: acontecimientos adversos; d: días
Consulta los estudios que apoyan los datos de eficacia Beyfortus® (Nirsevimab)
Contenido mínimo de Beyfortus®
PRESENTACIÓN, PRECIO Y CONDICIONES DE PRESCRIPCIÓN Y PRESENTACIÓN
BEYFORTUS® 50 mg SOLUCIÓN INYECTABLE EN JERINGA PRECARGADA, 1 jeringa precargada (CN: 762403) y BEYFORTUS® 100 mg SOLUCIÓN INYECTABLE EN JERINGA PRECARGADA, 1 jeringa precargada (CN: 762405) PVP notificado: 812,67 € PVP IVA notificado: 845,18 €. Financiada por el SNS. Con receta.
Ficha Técnica Beyfortus® 50mg Ficha Técnica Beyfortus® 100 mg
▼ «Este medicamento está sujeto a seguimiento adicional, es prioritaria la notificación de sospechas de reacciones adversas asociadas a este medicamento.»
* El IC del 95% para la eficacia se calcula utilizando un método exacto, asumiendo una distribución binomial del número de hospitalizaciones por ITRI en el grupo de nirsevimab, condicionada al número total en ambos grupos (descrito por Breslow y Day), teniendo en cuenta el tiempo de seguimiento tras la administración/aleatorización.
**Necesidad de soporte de oxígeno.
¶ No corregido por multiplicidad.
Referencias
- Drysdale S.B, et al. N Engl J Med 2023;389:2425-35
- Munro A.P.S, et al. Lancet Child Adolesc Health. 2025;9(6):404–12
- Ficha técnica Beyfortus® CIMA - AEMPS. Disponible en: https://cima.aemps.es/cima/publico/detalle.html?nregistro=1221689001.
[Último acceso el 24 Mar 2025]
MAT-ES-2402220 V2 Junio 2025