- Artículo
- Fuente: Campus Sanofi
- 21 jul 2025
ASCEND-Peds: Estudio de ▼Xenpozyme® en pacientes pediátricos
ASCEND-Peds fue un estudio pivotal y multicéntrico para evaluar la seguridad (64 semanas) y la eficacia (52 semanas).1,2
20 pacientes pediátricos de ASMD tipo A/B o tipo B


Criterios de valoración a las 52 semanas

* Al inicio, se observaron manifestaciones neurológicas en 8 de los 20 pacientes pediátricos, compatibles con
un diagnóstico clínico de ASMD tipo A/B. Los 12 pacientes restantes tenían un diagnóstico clínico compatible con
ASMD tipo B.1
Nota: En este estudio se excluyó a pacientes con anomalías neurológicas agudas o de progresión rápida.2
Con Xenpozyme® se consiguió una reversión rápida* y sostenida de las principales manifestaciones del ASMD en pacientes pediátricos1,2
Eficacia en pacientes pediátricos durante todo el estudio
Xenpozyme® mejoró significativamente la función pulmonar y ayudo a prevenir la posterior progresión de la enfermedad1,3
Mejora en la DLco observada desde la semana 26 respecto al inicio1,2,4 *
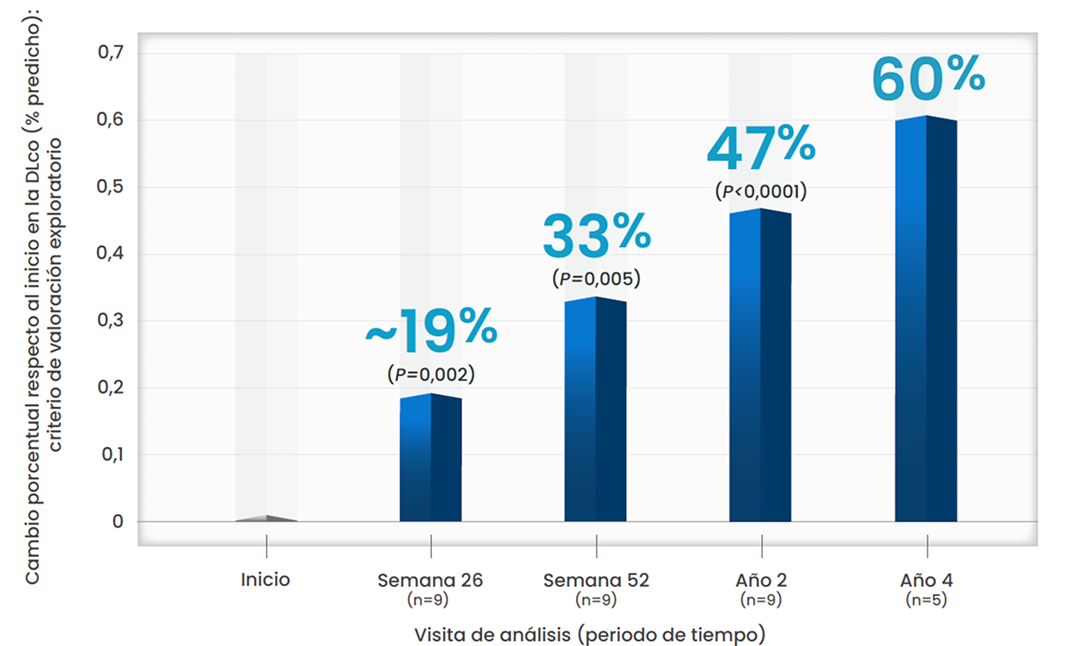
Esta gráfica ha sido creada a partir del texto de las publicaciones. Todos los pacientes pertenecen al estudio ASCEND-Peds
*Este criterio de valoración es exploratorio. Los valores de p proporcionados son únicamente para fines descriptivos.
Xenpozyme® redujo el volumen del bazo y ayudó a prevenir la posterior progresión de la enfermedad.1
Reducción del volumen del bazo observada desde la semana 26 respecto al inicio1,2,4*
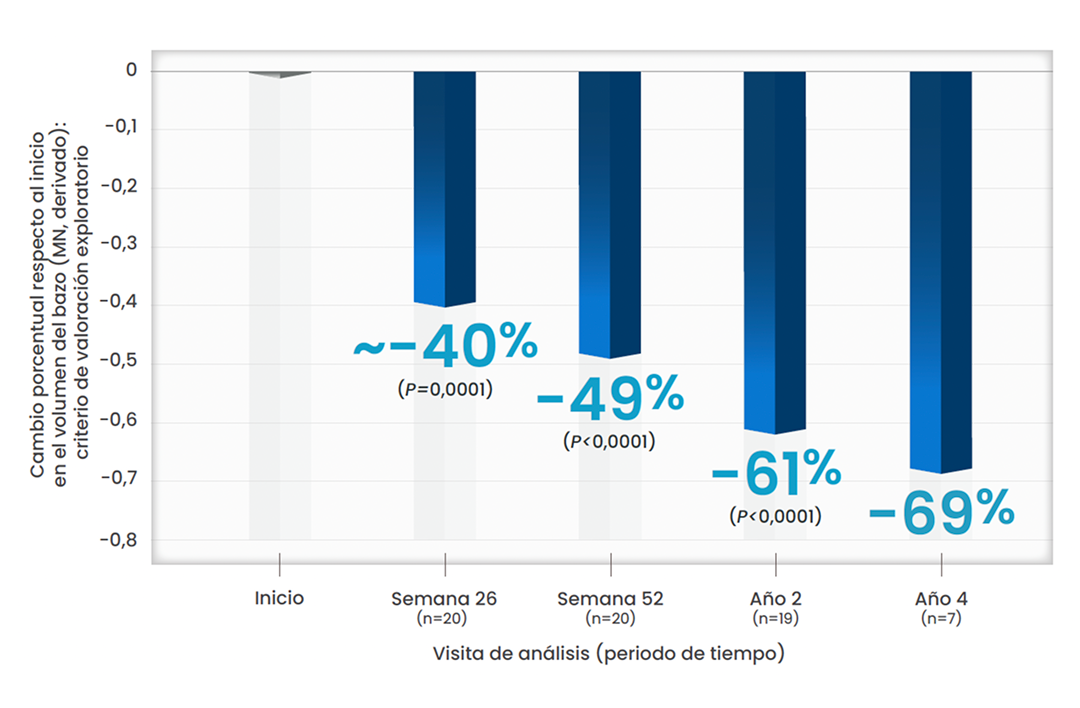
Esta gráfica ha sido creada a partir del texto de las publicaciones. Todos los pacientes pertenecen al estudio ASCEND-Peds
*Este criterio de valoración es exploratorio. Los valores de p proporcionados son únicamente para fines descriptivos.
Xenpozyme® redujo el volumen del hígado y mejoró los marcadores del daño hepático.1,2
Reducción del volumen del hígado observada desde la semana 26 respecto al inicio1,2,4*
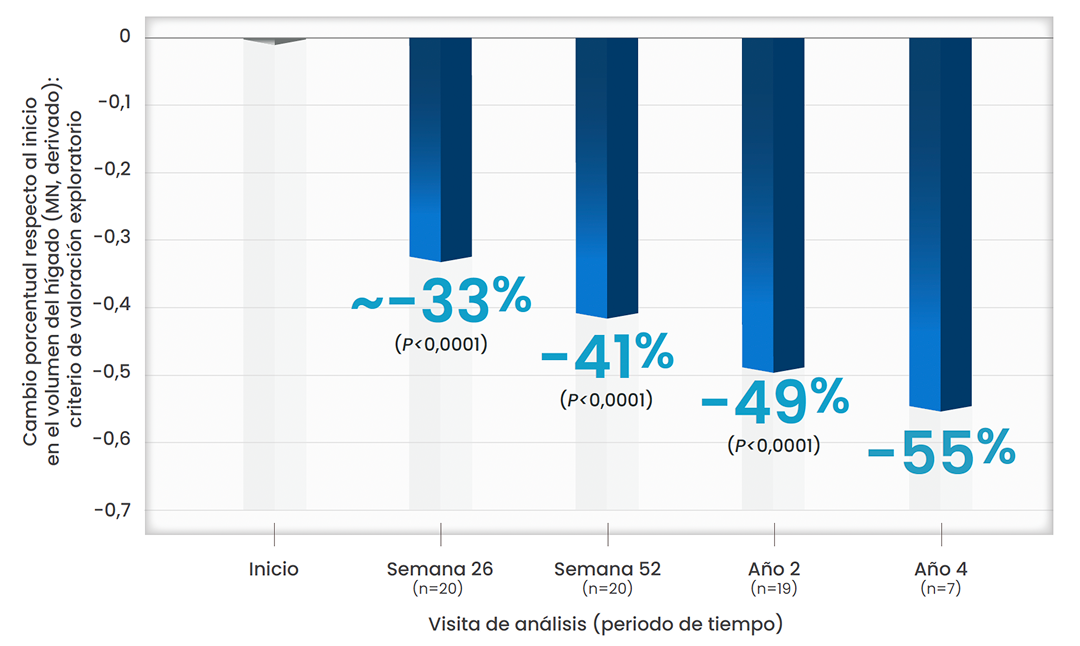
Esta gráfica ha sido creada a partir del texto de las publicaciones. Todos los pacientes pertenecen al estudio ASCEND-Peds
*Este criterio de valoración es exploratorio. Los valores de p proporcionados son únicamente para fines descriptivos.
Pruebas de la función hepática a los dos años
Media +- de la disminución porcentual a los 24 meses5
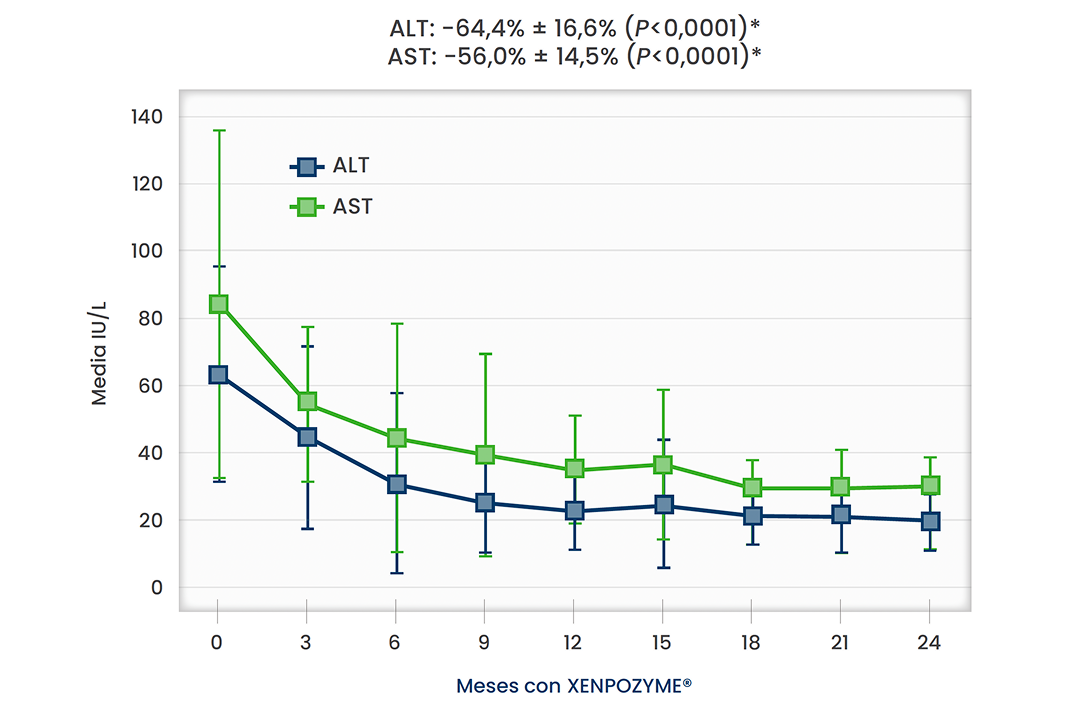
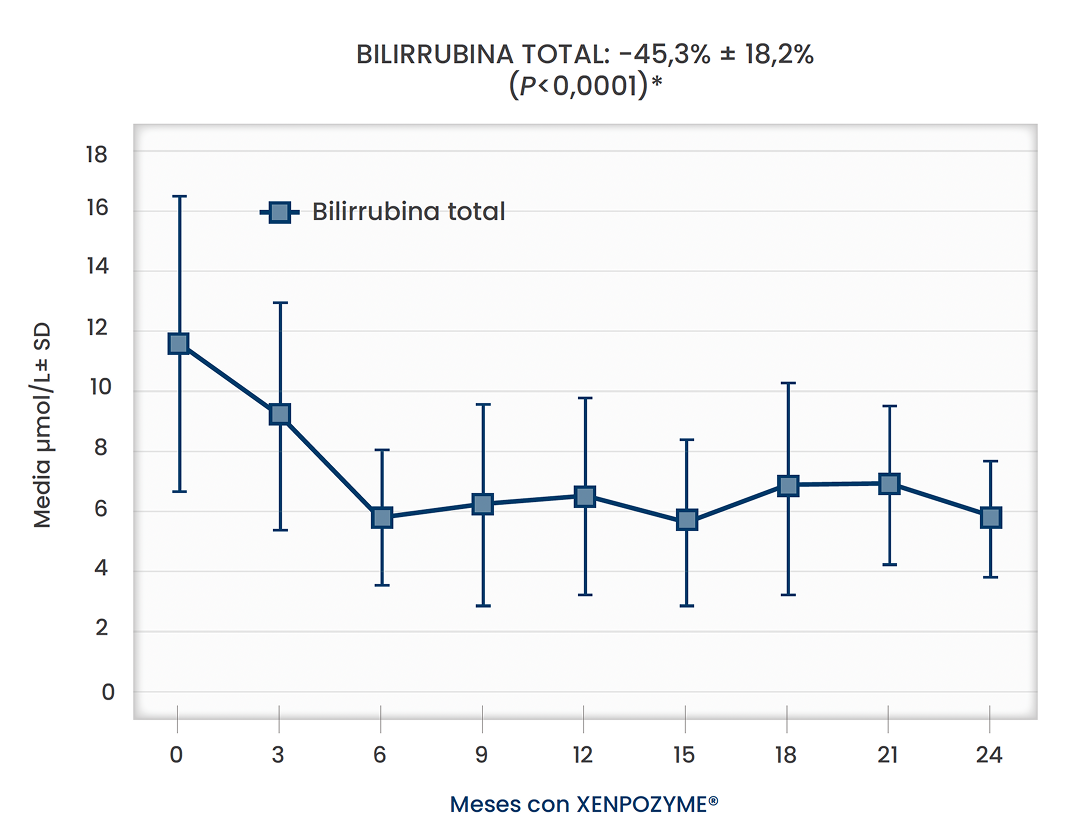
*Todos los valores de p fueron nominales.
Xenpozyme® aumentó el recuento de plaquetas1
Aumento del recuento de plaquetas observado desde la semana 52 respecto al inicio 1,2*
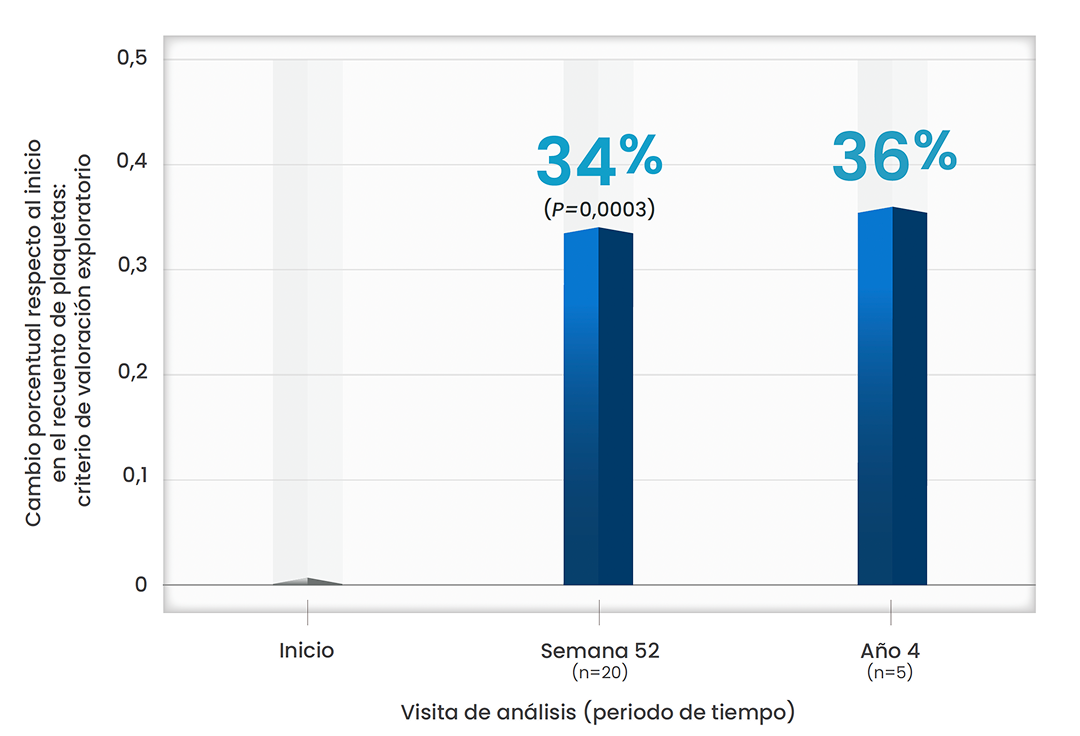
Esta gráfica ha sido creada a partir del texto de las publicaciones. Todos los pacientes pertenecen al estudio ASCEND-Peds.
* Este criterio de valoración es exploratorio. Los valores de p proporcionados son únicamente para fines descriptivos.
Perfil lipídico a los dos años
Perfiles lipídicos aterogénicos normalizados 5
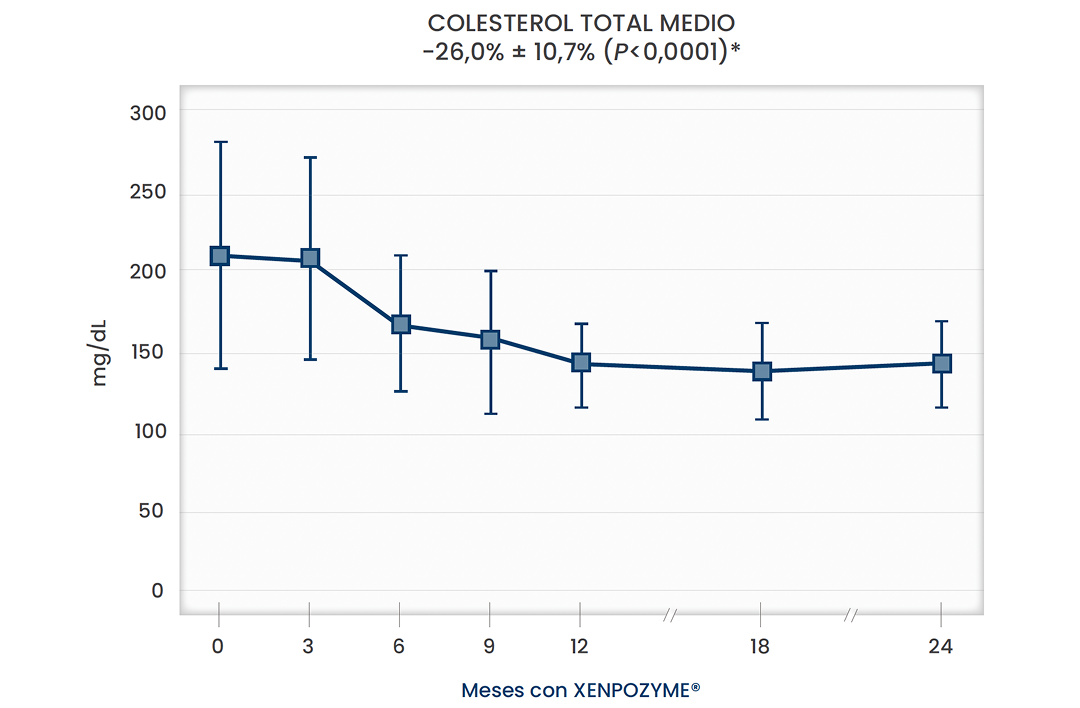
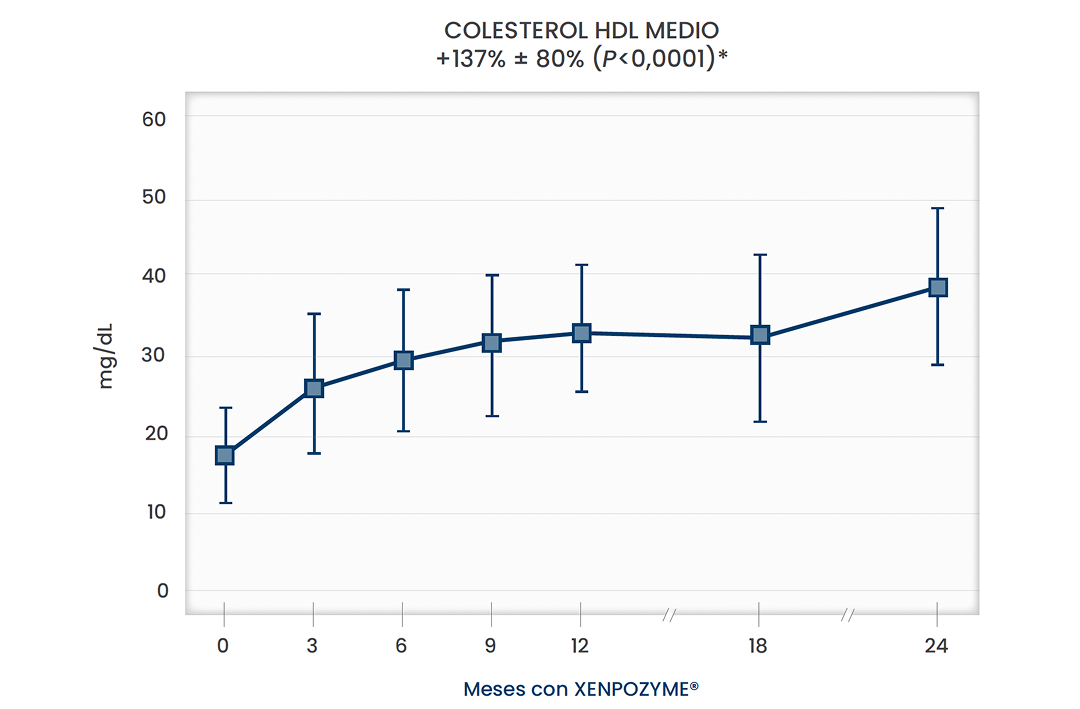
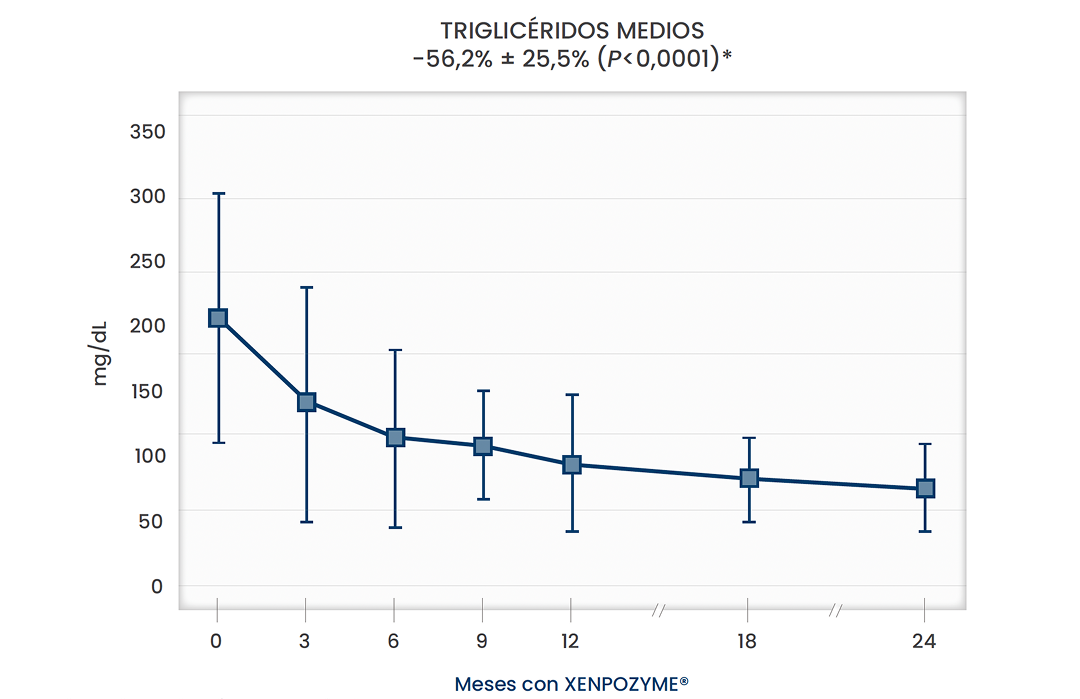
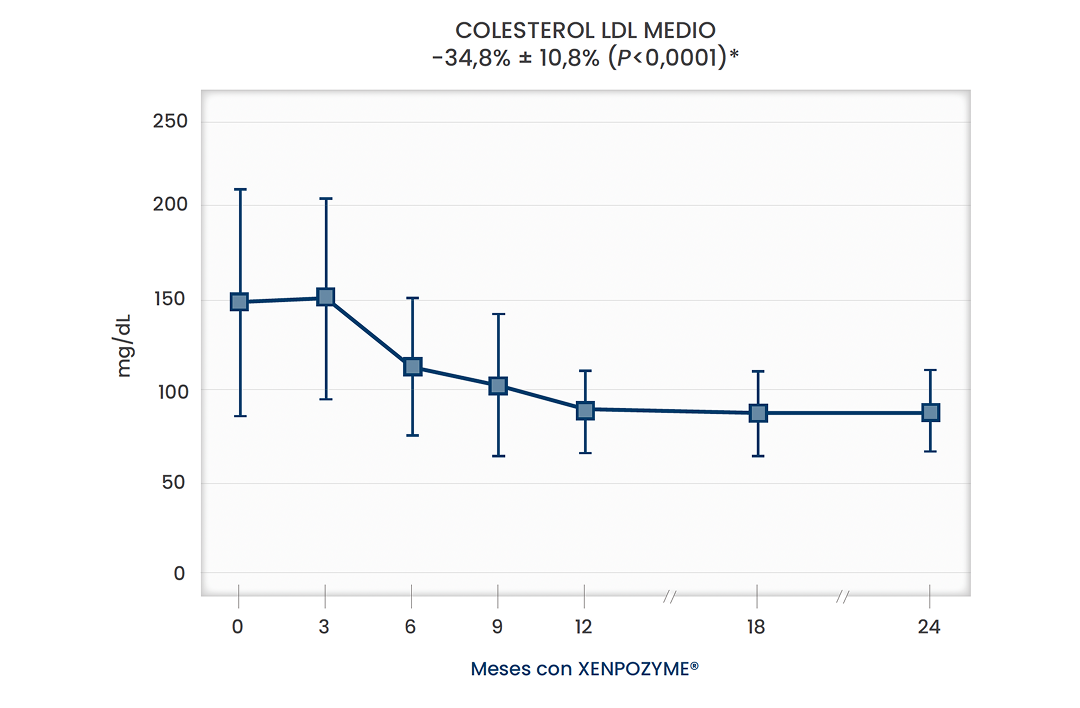
*Todos los valores de p fueron nominales.
Se observó una mejora del z-score de estatura en pacientes pediátricos tratados con Xenpozyme®1,2,4*
Aumento del recuento de plaquetas observado desde la semana 52 respecto al inicio 1,2*
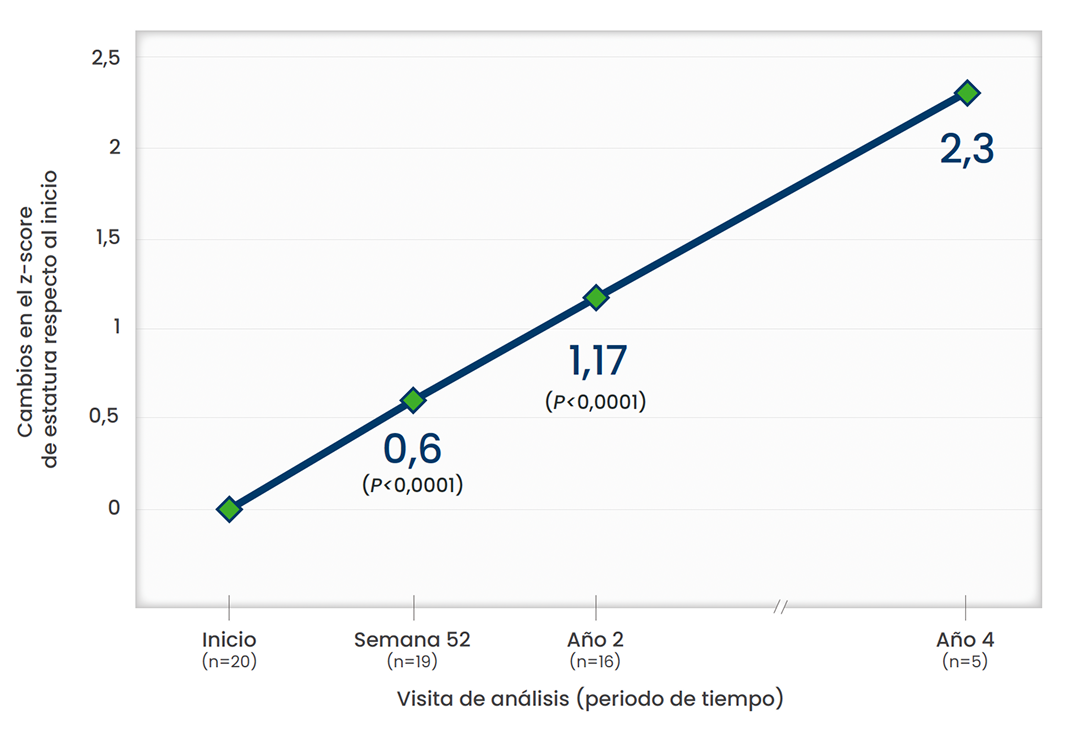
Esta gráfica ha sido creada a partir del texto de las publicaciones. Todos los pacientes pertenecen al estudio ASCEND-Peds.
Z-score de la estatura medida como desviaciones estándar respecto a la media. Un niño con una Z-score de 0 es de estatura media para su edad y sexo.6
* Este criterio de valoración es exploratorio. Los valores de p proporcionados son únicamente para fines descriptivos.
Los datos presentados para la semana 26, la semana 52 y el año 2 son medias MC. Los datos presentados para el año 4 son medias.1,4,6
Xenpozyme® mejoró significativamente la función pulmonar y ayudo a prevenir la posterior progresión de la enfermedad1,3
Mejora en la DLco observada desde la semana 26 respecto al inicio1,2,4 *

Esta gráfica ha sido creada a partir del texto de las publicaciones. Todos los pacientes pertenecen al estudio ASCEND-Peds
*Este criterio de valoración es exploratorio. Los valores de p proporcionados son únicamente para fines descriptivos.
Xenpozyme® redujo el volumen del bazo y ayudó a prevenir la posterior progresión de la enfermedad.1
Reducción del volumen del bazo observada desde la semana 26 respecto al inicio1,2,4*

Esta gráfica ha sido creada a partir del texto de las publicaciones. Todos los pacientes pertenecen al estudio ASCEND-Peds
*Este criterio de valoración es exploratorio. Los valores de p proporcionados son únicamente para fines descriptivos.
Xenpozyme® redujo el volumen del hígado y mejoró los marcadores del daño hepático.1,2
Reducción del volumen del hígado observada desde la semana 26 respecto al inicio1,2,4*

Esta gráfica ha sido creada a partir del texto de las publicaciones. Todos los pacientes pertenecen al estudio ASCEND-Peds
*Este criterio de valoración es exploratorio. Los valores de p proporcionados son únicamente para fines descriptivos.
Pruebas de la función hepática a los dos años
Media +- de la disminución porcentual a los 24 meses5


*Todos los valores de p fueron nominales.
Xenpozyme® aumentó el recuento de plaquetas1
Aumento del recuento de plaquetas observado desde la semana 52 respecto al inicio 1,2*

Esta gráfica ha sido creada a partir del texto de las publicaciones. Todos los pacientes pertenecen al estudio ASCEND-Peds.
* Este criterio de valoración es exploratorio. Los valores de p proporcionados son únicamente para fines descriptivos.
Perfil lipídico a los dos años
Perfiles lipídicos aterogénicos normalizados 5




*Todos los valores de p fueron nominales.
Se observó una mejora del z-score de estatura en pacientes pediátricos tratados con Xenpozyme®1,2,4*
Aumento del recuento de plaquetas observado desde la semana 52 respecto al inicio 1,2*

Esta gráfica ha sido creada a partir del texto de las publicaciones. Todos los pacientes pertenecen al estudio ASCEND-Peds.
Z-score de la estatura medida como desviaciones estándar respecto a la media. Un niño con una Z-score de 0 es de estatura media para su edad y sexo.6
* Este criterio de valoración es exploratorio. Los valores de p proporcionados son únicamente para fines descriptivos.
Los datos presentados para la semana 26, la semana 52 y el año 2 son medias MC. Los datos presentados para el año 4 son medias.1,4,6

Contenido mínimo de Xenpozyme®
PRESENTACIÓN, PRECIO Y CONDICIONES DE PRESCRIPCIÓN Y DISPENSACIÓN:
Xenpozyme 4 mg polvo para concentrado para solución para perfusión – 1 vial (CN 762543.8): PVP notificado: 3.430,91 €, PVP IVA notificado: 3.568,15 €. Medicamento sujeto a prescripción médica. Financiado por el SNS. Uso hospitalario.
Ver ficha técnica de Xenpozyme 4 mg.
Xenpozyme 20 mg polvo para concentrado para solución para perfusión – 1 vial (CN 758015.7): PVP notificado: 3.430,91 €, PVP IVA notificado: 3.568,15 €. Medicamento sujeto a prescripción médica. Financiado por el SNS. Uso hospitalario.
Ver ficha técnica de Xenpozyme 20 mg
▼ «Este medicamento está sujeto a seguimiento adicional, es prioritaria la notificación de sospechas de reacciones adversas asociadas a este medicamento.»
Referencias
ALT= alanina aminotransferasa; ASMD = déficit de esfingomielinasa ácida (Acid Sphingomyelinase Deficiency); AST= aspartato aminotranferasa; DLco = difusión pulmonar de
monóxido de carbono (diffusion capacity of the lungs for carbon monoxide); MN = múltiplos de lo normal.
- Ficha técnica Xenpozyme®. Consultado en julio 2025. Disponible en: https://cima.aemps.es/cima/dochtml/ft/1221659001/FT_1221659001.html#4.11
- Diaz GA, et al. Genet Med. 2021;23(8):1543-1550
- McGovern MM, et al. Orphanet J Rare Dis. 2021;16(1):212.
- Diaz GA, et al. Mol Genet Metab. 2021;135(2):S37.
- Diaz GA, et al. Póster presentado en el 18º Simposio anual WORLD; Febrero 9, 2022; San Diego, CA.
- Martinez-Millana A, et al. PLoS One. 2018;13(12):e0208362.
MAT-ES 2502048 V1 julio 2025