- Artículo
- Fuente: Campus Sanofi
- 4 ago 2025
Fisiopatología y causas de la PTI
En la PTI, la desregulación inmunitaria reduce el recuento de plaquetas a través de múltiples vías. Las células B autorreactivas producen autoanticuerpos que atacan a las plaquetas para que sean destruidas por los macrófagos y dificultan la maduración de los megacariocitos, lo que reduce la producción de plaquetas. Los autoanticuerpos también pueden destruir las plaquetas a través de otros mecanismos.
La actividad del sistema inmunitario también puede provocar niveles elevados de marcadores inflamatorios.1-6
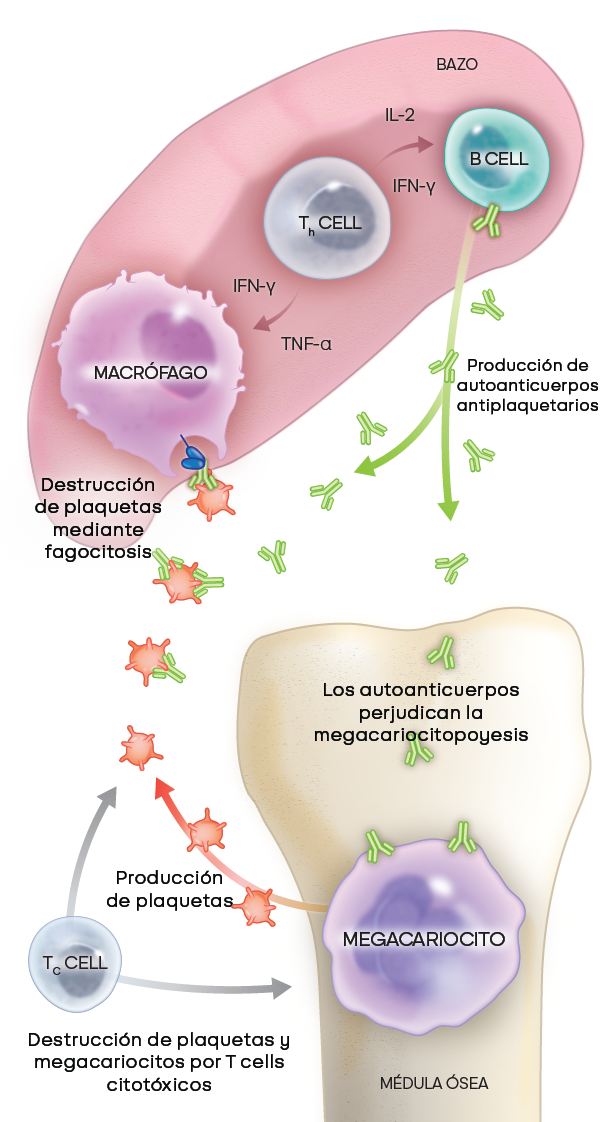
Adaptado de Kashiwagi H, et al. Int J Hematol. 2013;98(1):24-33. © Sociedad Japonesa de Hematología (JSH).1
Los tratamientos diseñados para lograr una modulación inmunológica múltiple tienen como objetivo abordar mejor las múltiples caras de la PTI 7,8.
Vea el vídeo sobre el mecanismo de la enfermedad (MOD) para obtener más información sobre las múltiples caras de la PTI.
La tirosina quinasa de Bruton (BTK) desempeña un papel fundamental en la compleja desregulación inmunitaria9,10
Las células B son responsables de la producción de autoanticuerpos; los macrófagos son esenciales para la fagocitosis; y el inflamasoma NLRP3 desempeña un papel clave en la inflamación sistémica. Todos estos procesos están regulados por la BTK.9,10
- En las células B: la vía BTK es crucial para la proliferación, la diferenciación y la producción de autoanticuerpos
- En los macrófagos: varias vías de señalización dependientes de la BTK impulsan la fagocitosis, la desgranulación y la producción de citocinas inflamatorias
- A nivel sistémico: la BTK impulsa la producción de mediadores de la inflamación como el inflamasoma NLRP3, que puede contribuir a la destrucción de plaquetas y a la inflamación sistémica.
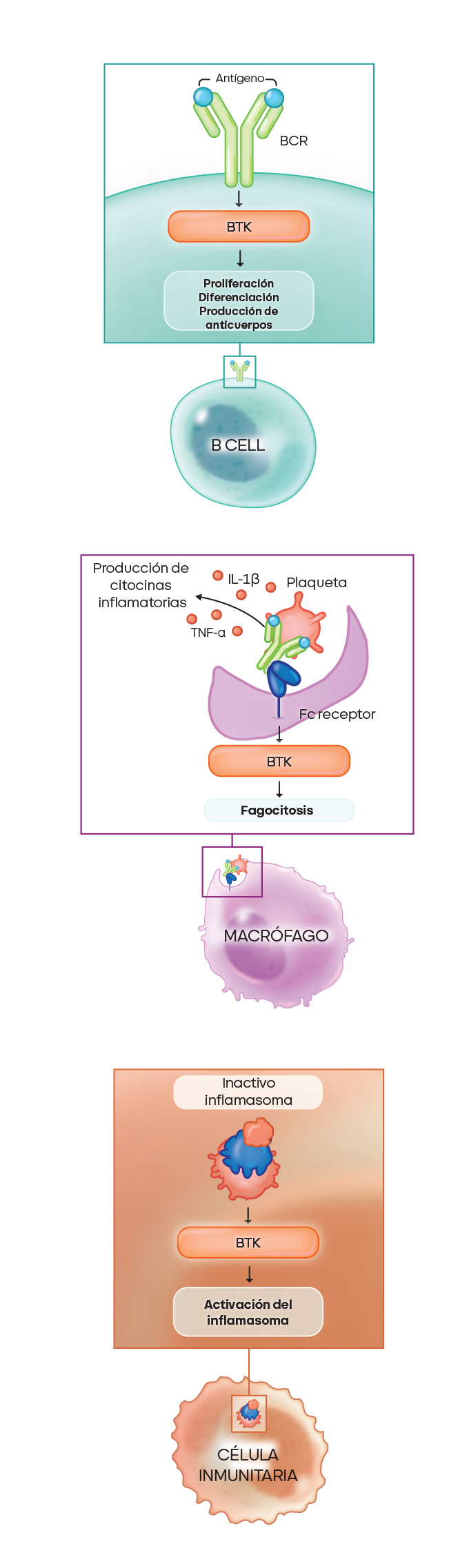
Los pacientes que padecen PTI presentan marcadores inflamatorios elevados, entre los que se incluyen10:
- TNF-α e IFN-γ
- IL-2 e IL-6
- Citoquinas del inflamasoma NLRP3 IL-1β e IL-18
La BTK está implicada en la producción o activación de estos marcadores inflamatorios y es un factor determinante de la inflamación.10
Otras vías de señalización implicadas en la patogénesis de la PTI 8
A medida que se va comprendiendo mejor los mecanismos moleculares que impulsan la patología de la PTI, cada vez está más claro que hay múltiples vías de señalización implicadas en la patogénesis y la manifestación de la enfermedad.8
La PTI es más que un problema de plaquetas.
BCR, receptor de células B; Fc, fragmento cristalizable; IFN, interferón; IL, interleucina; NLRP3, proteína 3 con dominio de unión a nucleótidos, repetición rica en leucina y dominio pirina; TNF, factor de necrosis tumoral.
Causas y fisiopatología de la PTI 1-4,8,11,12
La prevalencia estimada de la PTI es de hasta 9,5 por cada 100 000 personas. Las causas y la fisiopatología de la trombocitopenia inmune (PTI), históricamente denominada púrpura trombocitopénica idiopática o púrpura trombocitopénica inmune, son multifactoriales y desencadenan una amplia gama de síntomas.
La fisiopatología de la PTI es compleja e implica diversas células inmunitarias y diferentes órganos. La destrucción de plaquetas y la inhibición de la trombopoyesis (producción de plaquetas) son factores clave de la enfermedad. Los tratamientos actuales para la PTI tienen como objetivo actuar sobre estos mecanismos de la trombocitopenia inmunitaria.
Nuestro conocimiento de la fisiopatología de la PTI se está ampliando y abriendo nuevas posibilidades de tratamiento para terapias más específicas y un control general de la enfermedad.
¿Cuáles son las causas de la PTI?12-14
La causa de la PTI en adultos puede diferenciarse según se trate de una PTI primaria o secundaria.
En la PTI primaria, las causas subyacentes siguen sin identificarse, por lo que anteriormente se conocía como púrpura trombocitopénica idiopática. Esta es la causa más común de PTI, con aproximadamente el 80 % de los pacientes con PTI diagnosticados con PTI primaria.
Por el contrario, la PTI secundaria está causada por factores conocidos, como determinados medicamentos, infecciones o cánceres.
A menudo se asocia con autoinmunidad persistente y enfermedades autoinmunes subyacentes, como el lupus eritematoso sistémico (LES) y el síndrome antifosfolípido (SAF).
La PTI crónica se caracteriza por la persistencia de los síntomas durante más de 12 meses después del diagnóstico inicial. La PTI crónica es más frecuente en adultos que en niños. Estudios recientes sugieren que factores genéticos, como los polimorfismos en los genes de los receptores de citocinas y los genes que regulan la actividad de las células T, pueden influir en la susceptibilidad a la PTI crónica. Sin embargo, se necesitan más investigaciones para comprender completamente las causas de la PTI crónica.
La PTI es una enfermedad inmunomediada compleja en la que múltiples mecanismos celulares y moleculares contribuyen tanto a la destrucción como a la disminución de la producción de plaquetas, con un papel central de vías de señalización como la BTK en la regulación de la respuesta inmunitaria e inflamatoria. Esta comprensión más profunda de su fisiopatología pone de manifiesto que la PTI trasciende el mero recuento plaquetario, implicando procesos sistémicos que condicionan su evolución clínica. En este contexto, el avance en el conocimiento de estas vías abre la puerta al desarrollo de estrategias terapéuticas más dirigidas y eficaces, orientadas a un control más completo de la enfermedad y a la mejora de los resultados clínicos a largo plazo.

Referencias
1. Kashiwagi H, Tomiyama Y. Pathophysiology and management of primary immune thrombocytopenia. Int J Hematol. 2013;98(1):24-33.
2. Andreescu M. The link between immune thrombocytopenia and the cytokine profile: a bridge to new therapeutical targets. Front Hematol. 2023;2:1191178.
3. Qiao J, Liu Y, Li X, et al. Elevated expression of NLRP3 in patients with immune thrombocytopenia. Immunol Res. 2016;64(2):431-437.
4. Schifferli A, Cavalli F, Godeau B, et al. Understanding immune thrombocytopenia: looking out of the box. Front Med (Lausanne). 2021;8:613192.
5. Wang S, Liu Y, Li G, Feng Q, Hou M, Peng J. Reduced intracellular antioxidant capacity in platelets contributes to primary immune thrombocytopenia via ROS-NLRP3-caspase-1 pathway. Thromb Res. 2021;199:1-9.
6. Nelson VS, Jolink AC, Amini SN, et al. Platelets in ITP: victims in charge of their own fate? Cells. 2021;10(11):3235.
7. Audia S, Bonnotte B. Emerging therapies in immune thrombocytopenia. J Clin Med. 2021;10(5):1004.
8. Mingot-Castellano ME, Bastida JM, Caballero-Navarro G, et al. Novel therapies to address unmet needs in ITP. Pharmaceuticals (Basel). 2022;15(7):779.
9. Zhu S, Gokhale S, Jung J, et al. Multifaceted immunomodulatory effects of the BTK inhibitors ibrutinib and acalabrutinib on different immune cell subsets – beyond B lymphocytes. Front Cell Dev Biol. 2021;9:727531.
10. Neys SFH, Hendriks RW, Corneth OBJ. Targeting Bruton’s tyrosine kinase in inflammatory and autoimmune pathologies. Front Cell Dev Biol. 2021;9:668131.
11. Lambert MP, Gernsheimer TB. Clinical updates in adult immune thrombocytopenia. Blood. 2017;129(21):2829-2835.
12. Matzdorff A, Meyer O, Ostermann H, et al. Immune thrombocytopenia – current diagnostics and therapy: recommendations of a joint working group of DGHO, ӦGHO, SGH, GPOH, and DGTI. Oncol Res Treat. 2018;41(suppl 5):1-30.
13. Pietras NM, Gupta N, Justiz Vaillant AA, Pearson-Shaver AL. Immune Thrombocytopenia. In: StatPearls. Treasure Island (FL): StatPearls Publishing; May 5, 2024.
14. Georgi JA, Middeke JM, Bornhäuser M, Matzdorff A, Trautmann-Grill K. Deciphering the genetic basis of immune thrombocytopenia: current evidence for genetic predisposition in adult ITP. Blood Adv. 2023;7(14):3710-3724.
MAT-ES-2503333 V1 Mayo 2026