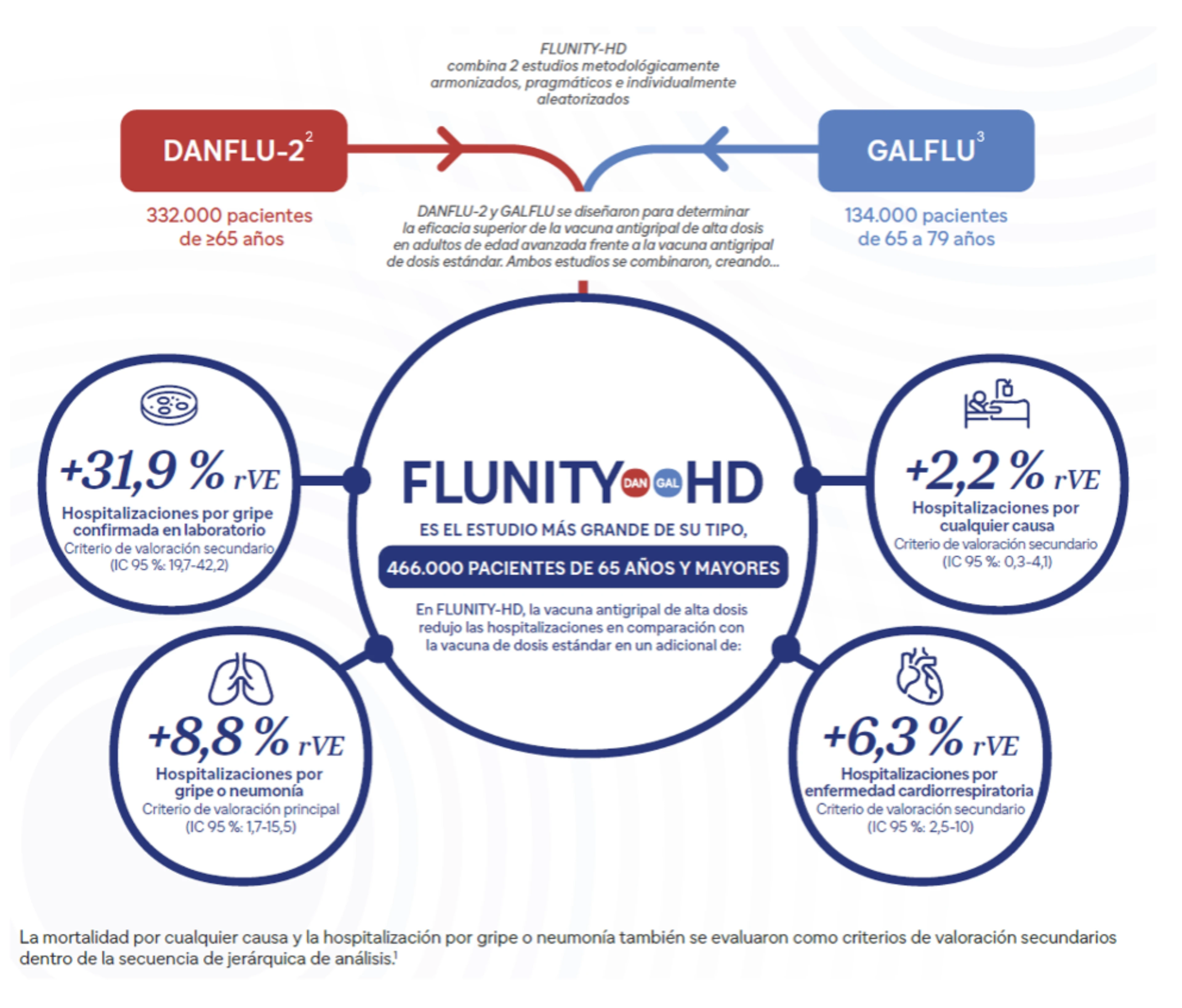
Flunity-HD(1): El mayor estudio de efectividad de vacunas antigripales con aleatorización individual, realizado hasta la fecha.
Flunity-HD(1): El mayor estudio de efectividad de vacunas antigripales con aleatorización individual, realizado hasta la fecha.
Lee más