- Artículo
- Fuente: Campus Sanofi
- 2 mar 2026
Papel de la interleucina-6 (IL-6) en la polimialgia reumática
La PMR es la segunda enfermedad reumática inflamatoria más frecuente después de la artritis reumatoide (AR)1

Las principales características de la polimialgia reumática (PMR), como la inflamación dolorosa, pueden atribuirse, en parte, a determinadas células inmunitarias y citocinas, como la interleucina-6 (IL-6).2,3
La PMR no solo se caracteriza por la inflamación y la rigidez, sino también por el dolor considerable1,4
En la PMR, el dolor y la rigidez se localizan típicamente en la cápsula sinovial y la bursa prerrotuliana, en la cintura escapular, la cintura pélvica y la región cervical.
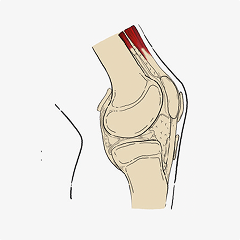
En la cápsula sinovial y la bolsa prerrotuliana
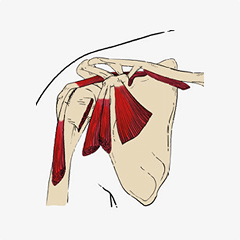
En la cintura escapular
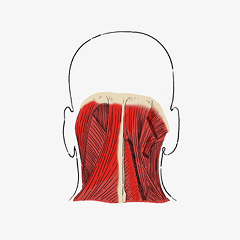
En la nuca
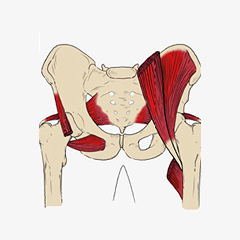
En la cintura pélvica
El dolor debido a la PMR se distingue del dolor mecánico en que el dolor inflamatorio de la PMR mejora con la actividad física2,4
De la clínica a la fisiopatología: red de citocinas e IL-6
Las artritis inflamatorias como la PMR son impulsadas por una red de citocinas proinflamatorias, incluida la IL-6
Solo algunas citocinas* promueven la inflamación5-7
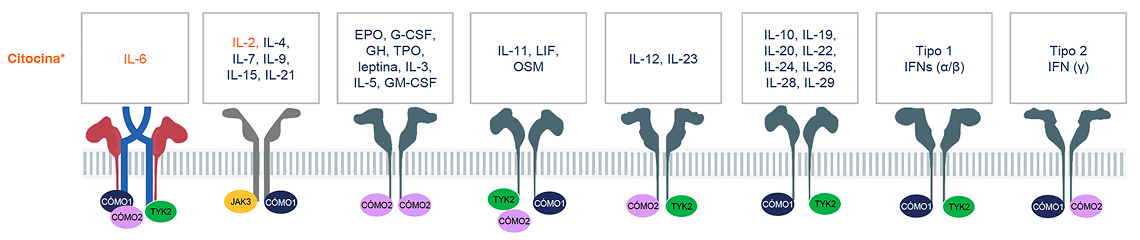
La desregulación de las vías de las citocinas, incluida la IL-6, puede provocar inflamación crónica y trastornos autoinmunes8
Se cree que la IL-6 persistentemente elevada desempeña un papel clave en el desarrollo y la progresión de PMR9
En la PMR, la IL-6 es uno de los principales determinantes de la respuesta de fase aguda y de la inflamación sistémica en AR y la PMR2,10
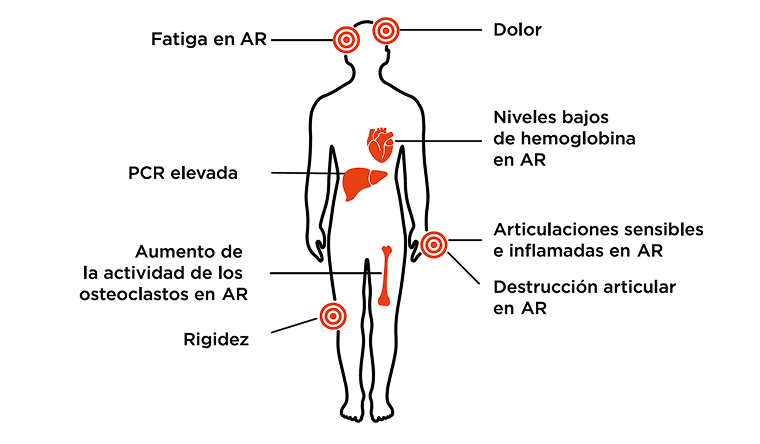
La IL-6 estimula:11
Inflamación sistémica11
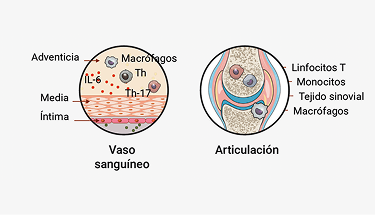
Inflamación local12,13
IL-6 y fisiopatología de la PMR
La IL-6 desempeña un papel clave en el desencadenamiento de la respuesta de fase aguda9
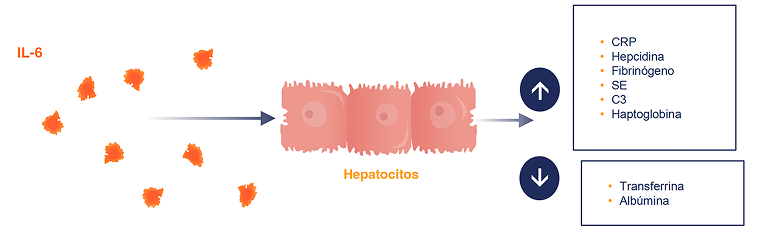
La producción de PCR mediada por IL-6 se asocia con inflamación en PMR3
Las concentraciones de IL-6 presentan correlación con la actividad de la PMR2
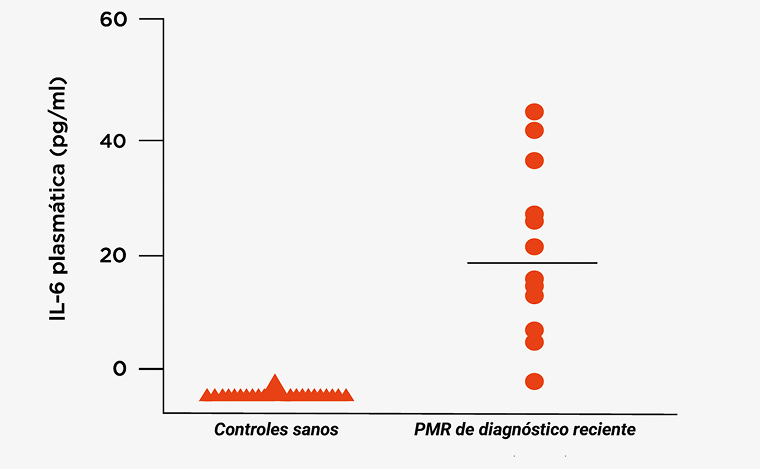
Cada símbolo ▲ y ● representa un paciente individual.
Figura extraída de González-Gay MA, Matteson EL, Castañeda S. Polymyalgia rheumatica. Lancet. 2017; 390:1700-1712.
Las concentraciones elevadas de IL-6 son una de las características de los pacientes con PMR en comparación con los controles sanos3
En un estudio con pacientes con PMR, se demostró la aparición de dolor muscular y rigidez al incrementarse las concentraciones plasmáticas de IL-63
La elevación de IL-6 no solo es sistémica, sino también local, en el líquido sinovial y estructuras periarticulares implicadas en la clínica típica de la PMR.13-15
La sinovitis observada en la PMR es un tipo de inflamación que se acompaña de un aumento de las concentraciones de IL-6 en el líquido sinovial13-15
En los pacientes con PMR, las concentraciones persistentemente elevadas de IL-6 se asocian a un aumento del riesgo de recaída1,16
En algunos casos, el grado de elevación de la concentración de IL-6 parece presentar correlación con la intensidad del dolor17
IL-6 persistentemente elevada y evolución de la enfermedad
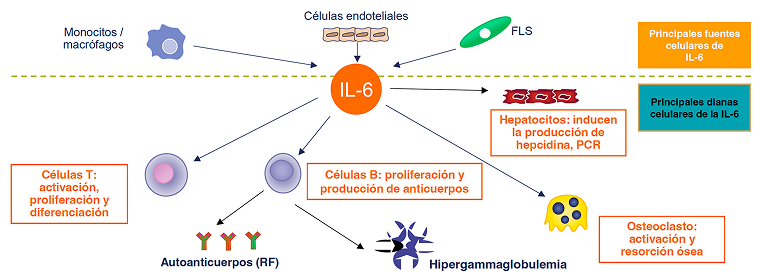
El aumento de los niveles séricos de IL-6 afecta a múltiples tipos de células implicadas en la patogénesis de PMR11
IL-6 y manifestaciones clínicas más allá de la inflamación articular
La IL-6 puede desempeñar un papel en el dolor, la fatiga, el sueño y el estado de ánimo
Dolor18-20
• Sensibilización al dolor periférico y central
Sueño20-24
• Elevada después de la privación del sueño
Fatiga18,21,24
• Activa el eje HPA, que está implicado en el trastorno de fatiga crónica
• Asociado con anemia y fatiga
Estado de ánimo18,25
• Aumentada en depresión20
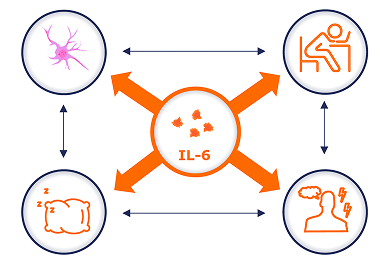
El dolor, el estado de ánimo, el sueño y la fatiga están altamente correlacionados entre sí. La IL-6 es uno de los varios factores que han sido implicados en estas manifestaciones18,26
Tratamiento, limitaciones de los GC y racional del inhibidor de IL-6R
En las guías actuales se establecen los glucocorticoides (GC) como tratamiento de referencia; sin embargo, sigue habiendo aspectos no resueltos, como la duración del tratamiento, las recaídas y los riesgos asociados con el aumento de las toxicidades relacionadas con los GC.1,16,27,28
Muchos pacientes necesitarán una estrategia de tratamiento de la PMR que minimice el uso de GC.27
La IL-6 desempeña un papel clave en la PMR29,30
- ↑ aumento en PMR29
- ↑ se asocia con recaída7,30,31
- ↑ asocia con la necesidad de dosis más altas de esteroides7,30,31
La inhibición de IL-6R da como resultado32
- ↓ en los síntomas de la enfermedad
- ↑ en las tasas de remisión
- ↓ en la inflamación y la dosis acumulada de esteroides
Continúa leyendo
Tratamiento estándar de la PMR con glucocorticoides. ¿Existe una dosis “segura”?

Contenido mínimo de Kevzara®
PRESENTACIÓN, PRECIO Y CONDICIONES DE PRESCRIPCIÓN Y DISPENSACIÓN:
KEVZARA® 200 mg solución inyectable en jeringa precargada, envase de 2 jeringas precargadas (CN 716173).
KEVZARA® 200 mg solución inyectable en pluma precargada, envase de 2 plumas precargadas (CN 716176).
PVP notificado: 1.033,06 € PVP IVA notificado: 1.074,38 €
Medicamento sujeto a prescripción médica. Diagnóstico hospitalario. Dispensación hospitalaria sin cupón precinto.
CONSULTE LA FICHA TÉCNICA COMPLETA ANTES DE PRESCRIBIR ESTE MEDICAMENTO.
Kevzara 200mg Jeringa
Kevzara 200mg Pluma
Kevzara está financiado en España de acuerdo con los criterios establecidos por el SNS.
Notas
ACPA: anticuerpos antipéptido cíclico citrulinado; AR: artritis reumatoide; FR: factor reumatoide; GC: glucocorticoides; IL-6: interleucina-6; IL-6R: receptor de interleucina-6; PMR: polimialgia reumática; sIL-6R: receptor soluble de interleucina-6; VSG: velocidad de sedimentación globular.
Referencias
- Acharya S, Musa R. Polymyalgia Rheumatica. NCBI Bookshelf. StatPearls [Internet]. Treasure Island (Fl): StatPearls Publishing; 2022.
- González-Gay MA, Matteson EL, Castañeda S. Polymyalgia rheumatica. Lancet. 2017; 390:1700-1712.
- Roche NE, Fulbright JW, Wagner AD, et al. Correlation of interleukin-6 production and disease activity in polymyalgia rheumatica and giant cell arteritis. Arthritis & Rheumatism. 1993;36(9):1286- 1294.
- Mackie SL. Polymyalgia rheumatica: pathogenesis and management. Clinical Medicine. 2013;13(4):398-400. 10. Guggino G, Ferrante A, Macaluso F, et al. Pathogenesis of polymyalgia rheumatica. Reumatismo. 2018;70(1):10-17.
- Kreiner F, et al. Athritis Rheum. 2010; 62(12):3768-3775
- Galbo H, et al. Arthritis Res Ther. 2016; 18(1):174
- Martinez-Taboada VM, et al. Cytokine. 2008; 44(2):207-220
- Hunter CA, et al. Nat Immunol. 2015; 16(5):448-457
- Dayer J-M, et al. Rheumatology (Oxford). 2010; 49:15-24
- Salvarani C, Cantini F, Niccoli L, et al. Acute-phase reactants and the risk of relapse/ recurrence in polymyalgia rheumatica: a prospective followup study. Arthritis Rheum. 2005 Feb 15;53(1):33-8. doi: 10.1002/art.20901.
- Guggino G, Ferrante A, Macaluso F, et al. Pathogenesis of polymyalgia rheumatica. Reumatismo. 2018;70(1):10-17.
- Carvajal Alegría G, Boukhal S, Cornec D, et al. The pathophysiology of polymyalgia rheumatica, small pieces of a big puzzle. Autoimmun Rev. 2020;19(11):102670.
- Jiemy WF, Zhang A, Boots AMH, et al. Expression of interleukin-6 in synovial tissue of patients with polymyalgia rheumatica. Ann Rheum Dis. 2023;82(3):440-442.
- Zen-nyoji A, Shimizu H, Ohtani K, et al. Increased RAHA titer and interleukin-6 levels in the synovial fl uid in a patient with polymyalgia rheumatica. Intern Med. 1993;32(6):484-486.
- Lundberg IE, Sharma A, Turesson C, Mohammad AJ. An update on polymyalgia rheumatica. J Intern Med. 2022 Nov;292(5):717-732.
- Buttgereit F, Dejaco C, Matteson EL, et al. Polymyalgia rheumatica and giant cell arteritis: a systematic review. JAMA. 2016;315(22):2442-2458.
- Sebba A. Pain: a review of interleukin-6 and its roles in the pain of rheumatoid arthritis. Open Access Reumatismo. 2018;70(1):10-17.
- Choy E, et al. Rheumatology (Oxford). 2018; 57:1885-1895
- Vázquez E, et al. Arthritis Rheum. 2012; 64:2233-2242
- Manzo, et al. Reumatología. 2020; 58(6):381-389.
- Rohleder N, et al. Ann N Y Acad Sci. 2012; 1261:88-96
- Vgontzas AN, et al. J Clin Endocrinol Metab. 1999; 84:2603-2607
- Vgontzas AN, et al. Neuroinmunomodulación. 2005; 12:131-140
- Manzo, et al. Reumatología. 2020; 58(4):196-201
- Girotti M, et al. Psiconeuroendocrinología. 2013; 38:1158-1169
- Irwin MR, et al. Sueño. 2012; 35:537-543
- Floris A, Piga M, Chessa E, et al. Long-term glucocorticoid treatment and high relapse rate remain unresolved issues in the real life management of polymyalgia rheumatica: a systematic literature review and meta-analysis. Clinical Rheum. 2022;41:19-31.
- Mazzantini M, Torre C, Miccoli M, et al. Adverse events during long term low-dose glucocorticoid treatment of polymyalgia rheumatica: a retrospective study. Journal Rheumatol. 2012;39(3):552-557.
- Dasgupta B, et al. Br J Rheumatol. 1990; 29(6):456-458
- Pulsatelli L, et al. Arthritis Rheum. 2008; 59(8):1147-1154
- Salvarani C, et al. Arthritis Rheum. 15 de febrero de 2005; 53(1):33-8
- Bonelli M, et al. Ann Rheum Dis . 2022; 81(6):838-844.
MAT-ES-2503754 - V1 Febrero 2026